
- •КЛАССИФИКАЦИЯ
- •ПЕРВАЯ ПОПЫТКА КЛАССИФИКАЦИИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
- •КЛАССИФИКАЦИЯ ПО ТИПУ ХИМИЧЕСКИХ ПРЕВРАЩЕНИЙ
- •КЛАССИФИКАЦИЯ ПО ЧИСЛУ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ,
- •КЛАССИФИКАЦИЯ ПРОСТЫХ ВЕЩЕСТВ
- •КЛАССИФИКАЦИЯ БИНАРНЫХ ВЕЩЕСТВ
- •КЛАССИФИКАЦИЯ ОКСИДОВ
- •КЛАССИФИКАЦИЯ МНОГОЭЛЕМЕНТНЫХ СОЕДИНЕНИЙ
- •КИСЛОТА И ОСНОВАНИЕ
- •КИСЛОТА И ОСНОВАНИЕ
- •КИСЛОТА И ОСНОВАНИЕ
- •«ЖЕСТКИЕ» И «МЯГКИЕ» КИСЛОТЫ И ОСНОВАНИЯ
- •ЖЁСТКИЕ КИСЛОТЫ ЛЬЮИСА:
- •ЖЁСТКИЕ ОСНОВАНИЯ ЛЬЮИСА:
- •ПРИНЦИП «ЖЕСТКИХ» И «МЯГКИХ» КИСЛОТ И ОСНОВАНИЙ (ПРИНЦИП «ЖМКО»)
- •КЛАССИФИКАЦИЯ КИСЛОТ
- •КЛАССИФИКАЦИЯ КИСЛОТ
- •КЛАССИФИКАЦИЯ ОСНОВАНИЙ
- •КЛАССИФИКАЦИЯ СОЛЕЙ
- •НОМЕНКЛАТУРА
- •ПРАВИЛА ДЛЯ СОСТАВЛЕНИЯ НАЗВАНИЙ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
- •НАЗВАНИЯ И ОБОЗНАЧЕНИЯ ЭЛЕМЕНТОВ И ИЗОТОПОВ
- •ЗАПИСЬ СИМВОЛОВ ИОНОВ
- •НАЗВАНИЯ КАТИОНОВ (правила ИЮПАК)
- •• многоэлементные катионы:
- •НАЗВАНИЯ АНИОНОВ (правила ИЮПАК)
- •• многоэлементные анионы:
- •НАЗВАНИЯ ПРОСТЫХ ВЕЩЕСТВ
- •МНОГОЭЛЕМЕНТНЫЕ СОЕДИНЕНИЯ
- •СОЕДИНЕНИЯ ДВУХ НЕМЕТАЛЛОВ ИЛИ МЕТАЛЛ-НЕМЕТАЛЛ
- •СОЕДИНЕНИЯ С НЕСКОЛЬКИМИ КАТИОНАМИ ИЛИ АНИОНАМИ
- •ПСЕВДОГАЛОГЕНИДЫ
- •ОКСИДЫ (O2 ), ПЕРОКСИДЫ (O22 ), НАДПЕРОКСИДЫ (O2 ), ОЗОНИДЫ (O3 ):
- •ВОДОРОДНЫЕ СОЕДИНЕНИЯ:
- •ГИДРОКСИДЫ (ОСНОВАНИЯ):
- •КИСЛОТЫ:
- •КИСЛОРОДСОДЕРЖАЩИЕ КИСЛОТЫ:
- •КИСЛОРОДСОДЕРЖАЩИЕ КИСЛОТЫ:
- •КИСЛОРОДСОДЕРЖАЩИЕ КИСЛОТЫ:
- •КИСЛОРОДСОДЕРЖАЩИЕ КИСЛОТЫ:
- •КИСЛОРОДСОДЕРЖАЩИЕ КИСЛОТЫ:
- •ЗАМЕЩЕННЫЕ КИСЛОТЫ
- •ДРУГИЕ ЗАМЕЩЕННЫЕ КИСЛОТЫ
- •НАЗВАНИЯ СРЕДНИХ (НОРМАЛЬНЫХ) СОЛЕЙ
- •НАЗВАНИЯ СРЕДНИХ (НОРМАЛЬНЫХ) СОЛЕЙ
- •НАЗВАНИЯ СРЕДНИХ (НОРМАЛЬНЫХ) СОЛЕЙ
- •НАЗВАНИЯ СРЕДНИХ (НОРМАЛЬНЫХ) СОЛЕЙ
- •НАЗВАНИЯ СРЕДНИХ (НОРМАЛЬНЫХ) СОЛЕЙ
- •НАЗВАНИЯ СРЕДНИХ (НОРМАЛЬНЫХ) СОЛЕЙ ЗАМЕЩЕННЫХ КИСЛОТ
- •НАЗВАНИЯ СРЕДНИХ (НОРМАЛЬНЫХ) СОЛЕЙ ЗАМЕЩЕННЫХ КИСЛОТ
- •НАЗВАНИЯ КИСЛЫХ СОЛЕЙ
- •Формула
- •НАЗВАНИЯ ОСНόВНЫХ СОЛЕЙ
- •НАЗВАНИЯ КРИСТАЛЛОГИДРАТОВ
- •КВАСЦЫ и ШЁНИТЫ
- •ТРИВИАЛЬНЫЕ И МИНЕРАЛОГИЧЕСКИЕ НАЗВАНИЯ
- •ТРИВИАЛЬНЫЕ И МИНЕРАЛОГИЧЕСКИЕ НАЗВАНИЯ
- •ТРИВИАЛЬНЫЕ И МИНЕРАЛОГИЧЕСКИЕ НАЗВАНИЯ
- •Презентация: «Классификация неорганических соединений». Автор: М.А. Ильин. Файл: «Классификация

КЛАССИФИКАЦИЯ
НЕОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
Автор: М.А. Ильин

ПЕРВАЯ ПОПЫТКА КЛАССИФИКАЦИИ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Антуан Лоран Лавуазье 1787 г.
•простые вещества;
•оксиды
(продукты горения простых веществ);
• кислоты и основания
(продукты взаимодействия оксидов с водой)
• соли
(продукты взаимодействия кислот и оснований)

КЛАССИФИКАЦИЯ ПО ТИПУ ХИМИЧЕСКИХ ПРЕВРАЩЕНИЙ
перенос разного рода частиц в химических превращениях (протоны, электроны, электронные пары , части молекул)
•КИСЛОТЫ (HNO3, H2SO4, H3PO3, H3AsO4 и др.)
•ОСНОВАНИЯ (NaOH, NH3, Ca(OH)2, Fe(OH)3 и др.)
•СОЛИ (NaNO3, (NH4)2SO4, KHSO4, Na2HPO3 и др.)
•ОКИСЛИТЕЛИ (Cl2, KMnO4, H2O2, HNO3 и др.)
•ВОССТАНОВИТЕЛИ (Na, H2, CO, H2O2, K2S2O4 и др.)
•КОМПЛЕКСООБРАЗОВАТЕЛИ (Ni2+, Cu2+, Fe3+, Ti4+, Pt4+ и др.)
•ЛИГАНДЫ (NH3, OH , CO, CN и др.)
•КООРДИНАЦИОННЫЕ СОЕДИНЕНИЯ ([Cu(NH3)6]Cl2, K2[PtCl6] и др.)
•РАДИКАЛЫ (NO, NO2, O2 и др.)
•АССОЦИАТЫ (N2O4, Cl2O6 и др.)
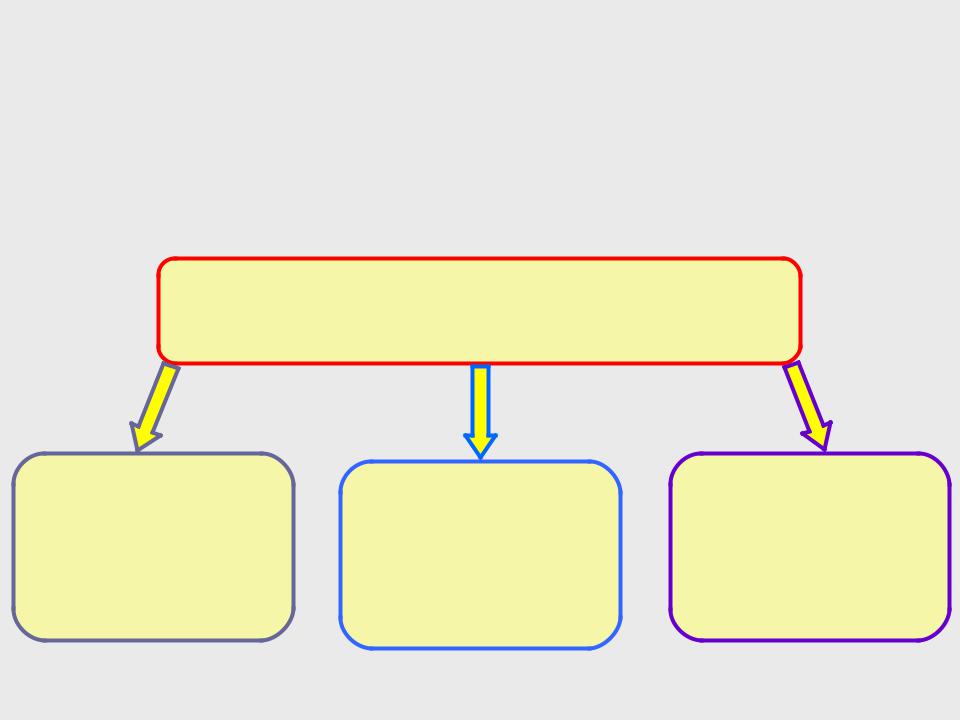
КЛАССИФИКАЦИЯ ПО ЧИСЛУ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ,
ВХОДЯЩИХ В СОСТАВ СОЕДИНЕНИЯ
Неорганические соединения
Одноэлементные |
Двухэлементные |
Многоэлементные |
|
(простые) |
|||
(бинарные) |
соединения |
||
вещества |
|||
соединения |
|||
(Ca3(PO4)2, H2[PtCl6] ) |
|||
(H2, O3, S8 ) |
|||
(NH3, NaCl, Fe2O3 ) |
|||
|
|

КЛАССИФИКАЦИЯ ПРОСТЫХ ВЕЩЕСТВ
• классификация на s-, p-, d- и f-элементы
• классификация на металлы и неметаллы
Одноэлементные (простые) Неметаллы Благородные
(He, Ne)
вещества
Активные (F2, O2 )
Металлы
Среднеактивные (N2, Si)
Активные |
Благородные |
(Na, Ca) |
(Au, Rh) |
Среднеактивные
(Fe, Ni)

КЛАССИФИКАЦИЯ БИНАРНЫХ ВЕЩЕСТВ
Двухэлементные
(бинарные)
соединения
Интерметаллиды |
Соединения |
(Cu3Au, Tl2Hg5 ) |
металл-неметалл |
Соединения неметаллов |
|
(S2Cl2, BN) |
Ионные |
|
|
|
(бинарные соли) |
|
(NaBr, SnCl2 ) |
Ковалентные (SnCl4, TiCl4 )

КЛАССИФИКАЦИЯ ОКСИДОВ
ОКСИДЫ
|
|
Солеобразующие |
Несолеобразующие |
|
|
|
|
|
(безразличные) |
|
|
|
|
(NO, CO, N2O) |
Кислотные |
Амфотерные |
|||
(N O |
, SO |
, CO ) |
(Al2O3, ZnO) |
|
2 |
5 |
2 |
2 |
|
Основные (CaO, Na2O, CuO)

КЛАССИФИКАЦИЯ МНОГОЭЛЕМЕНТНЫХ СОЕДИНЕНИЙ
Кислоты |
|
|
Многоэлементные |
Кластеры |
|
|
|
|
соединения |
|
|||
(H SO , HNO |
|
) |
(Fe2(CO)9, Os3(CO)12 |
) |
||
3 |
|
|||||
2 |
4 |
|
|
|
|
|
Основания |
Клатраты |
(LiOH, Cu(OH)2 ) |
(CH4·7H2O) |
Соли |
Комплексные соединения |
(KNO3, (NH4)H2PO4 ) |
(Na3 [RhCl6 ], [Cu(NH3)4]Cl2 ) |

КИСЛОТА И ОСНОВАНИЕ
Сванте Аррениус:
Кислота – вещество, диссоциирующее в воде с образованием Н+ (HCl, HCOOH, H3PO4, KH2PO4, H2O)
Основание – вещество, диссоциирующее в воде с образованием ОН
(NaOH, Fe(OH)2, Al(OH)3, Mg(OH)Cl, H2O)
HA H+ + A |
или BOH B+ + OH |
важнейшие количественные характеристики:
– степень диссоциации |
число распавшихся молекул |
|
общее число молекул |
||
|
– константа диссоциации K [H ][A ]
[HA]

КИСЛОТА И ОСНОВАНИЕ
Йоханнес Бренстед:
Кислота – частица-донор Н+ (H3O+, HCOOH, NH4+, HSO4 , H2O) Основание – частица-акцептор Н+ (OH , NH3, CO32 , HSO4 , H2O)
сопряженные пары кислота-основание:
HCl H+ + Cl |
|
|
|
|
|
|
|
|
|
|
|
кис |
|
-та |
|
|
|
осн-е |
|
||||
|
+ H |
+ |
H2O + H2O |
H3O+ + OH |
|||
H2SO4 HSO4 |
|
кис-та |
|
|
осн-е |
||
HSO4 SO42 + H+
[Al(H2O)6]3+ [Al(H2O)5(OH)]2+ + H+
зависимость от растворителя: CH3COOH + H2O CH3COO + H3O+ CH3COOH + H2SO4 CH3COOH2+ + HSO4
