
- •Тема 17. Металлические материалы и изделия
- •17.1. Строение металлов
- •17.2. Свойства металлов
- •17.3. Строение железоуглеродистых сплавов
- •17.4. Производство чугуна и стали
- •17.4.1. Производство чугуна
- •17.4.2. Производство стали
- •17.5. Термическая обработка стали
- •17.6. Химико-термическая обработка стали
- •17.7. Коррозия металлов и меры защиты от нее
- •17.8. Основные виды металлов, применяемых в строительстве
- •17.8.1. Стали
- •17.8.2. Чугуны
- •17.8.3. Цветные металлы и сплавы
17.3. Строение железоуглеродистых сплавов
В результате совместной кристаллизации нескольких элементов могут образоваться сплавы следующих типов: механическая смесь, твердый раствор и химическое соединение. Возможность возникновения того или иного типа сплава определяется характером взаимодействия элементов в процессе кристаллизации.
Температуру, при которой металл переходит из жидкого состояния в твердое состояние, называют температурой первичной. Геометрическое место точек первичной кристаллизации называется линией ликвидуса. Кроме первичной кристаллизации, возможна и вторичная кристаллизация (перекристаллизация в твердой фазе) − изменение кристаллического строения металлов в твердом состоянии. Геометрическое место точек вторичной кристаллизации называется линией солидуса.
При быстром отводе тепла некоторые металлы способны определенное время находиться в жидком состоянии при температуре ниже границы первичной кристаллизации (рис. 5 – второй график). Это явление объясняют следующим образом. В результате быстрого отвода тепла образуется много центров кристаллизации и происходит их интенсивный рост, что приводит к выделению значительного количества теплоты, способной некоторое время поддерживать металл в жидком состоянии и даже повышать его температуру.
Металлы обладают свойствами аллотропии, т. е. способностью одного и того же химического элемента при различной температуре иметь разную кристаллическую структуру. Аллотропические превращения сопровождаются выделением или поглощением теплоты. Железо имеет четыре аллотропические формы: α-Fe; β-Fe; γ-Fe; δ-Fe. Практическое значение имеют только α-Fe и γ-Fe, так как β-Fe и δ-Fe отличаются от α-Fe только величиной межатомного расстояния, а для β-Fe характерно отсутствие магнитных свойств.
Критические температуры аллотропии железа представлены на диаграмме охлаждения чистого железа (рис. 6) как температуры горизонтальных участков, свидетельствующих о том, что фазовые превращения происходят с выделением теплоты.


15390С


Температура
δ
13900С

γ
9100С
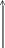
β
7680С

α

Время

Рис. 6. Диаграмма охлаждения чистого железа
Механические смеси образуются путем срастания кристаллов между собой при раздельной кристаллизации компонентов. В механической смеси каждый из компонентов сохраняет свои специфические свойства. Структура сплава в этом случае будет состоять из кристаллов веществ А и Б, связь между которыми осуществляется по границам зерен. Значения свойств сплава будут средними между свойствами элементов, которые его образуют.
Твердые растворы образуются в результате проникновения в кристаллическую решетку основного металла атомов другого металла или неметалла. В зависимости от характера размещения атомов различают твердые растворы замещения и внедрения. При образовании твердого раствора замещения атомы одного из компонентов, например Б, частично замещают атомы компонента А в узлах его кристаллической решетки. Твердый раствор внедрения образуется, когда атомы одного из компонентов размещаются в междоузлиях кристаллической решетки другого. Твердые растворы замещения могут образоваться при совместной кристаллизации металлов, а твердые растворы внедрения – при совместной кристаллизации металла с неметаллом. Твердые растворы принято обозначать буквами греческого алфавита α, β, γ и т. п.
В растворе внедрения атомы растворимого элемента внедряются между атомами металла, искажая его решетку. К таким элементам относятся углерод, водород, азот, бор и другие, концентрация которых в твердом растворе может составлять 1…2 %. В растворе замещения атомы растворимого элемента занимают места атомов растворителя в кристаллической решетке. При этом размеры атомов основного металла и примеси должны отличаться не более чем на 15 %. Хорошо замещаются атомы Fe и Сг, Сu и Ni, Ti и V.
Химические соединения образуются при химическом взаимодействии компонентов, при этом атомы располагаются в строгом порядке и количественном соотношении. Например, в сплавах железа с углеродом образуется карбид железа, называемый цементитом: 3Fe + C = Fe3C. В сплавах алюминия с медью образуется интерметаллическое соединение СuА12. Как Fe3C, так и СuА12 – твердые, прочные, но очень хрупкие вещества. Наличие их в сплаве ведет к его упрочнению с одновременным понижением пластичности и ударной вязкости.
Строение сплава определяет его свойства, поэтому важно знать, как это строение будет меняться при изменении температуры и состава сплава. Зависимость между строением сплава, его составом и температурой описывается при помощи диаграмм состояния.
Диаграммы состояния строятся экспериментально по критическим точкам, полученным на кривых охлаждения сплавов данной системы. Поскольку критические точки стремятся получить при очень медленном нагреве или охлаждении сплава, т. е. для равновесного состояния, то диаграммы состояния также называются еще и диаграммами равновесия.
По диаграмме состояния конкретного сплава можно определить температуры кристаллизации и превращений в твердом состоянии и структуру при заданной температуре, что позволяет примерно оценить механические, физические и химические свойства сплава и правильно назначать режимы термической обработки, обработки давлением, сварки и т. п. Диаграммы состояний многих технических сплавов имеют сложный вид, но в большинстве случаев они могут быть сведены к нескольким простейшим диаграммам.
Диаграмма состояния «железо-углерод» (рис. 7) описывает равновесное состояние железоуглеродистых сплавов в зависимости от содержания углерода и температуры. По ней судят о структуре медленно охлажденных сплавов, а также о возможности изменения их микроструктуры в результате термической обработки, определяющей эксплуатационные свойства сплавов.

Рис. 7. Диаграмма состояния «железо-углерод»: а – диаграмма; I – жидкий сплав; II – жидкий сплав и кристаллы аустенита; III – жидкий сплав и цементит; IV – аустенит; V – цементит и аустенит; VI – аустенит, цементит, ледебурит; VII – цементит и ледебурит; VIII – феррит и аустенит; IX – феррит и перлит; X – цементит и перлит; XI – перлит, цементит, ледебурит; XII – цементит, ледебурит; б –ориентировочные отношения структурных составляющих в различных областях диаграммы
Основные структуры, составляющие диаграмму «железо-углерод» − феррит, цементит, аустенит, перлит, ледебурит, графит.
Феррит − твердый раствор углерода в α-Fe. Предельное содержание углерода при 723 °С ≈ 0,02 %, при 20 °С ≈ 0,006 %. Феррит по свойствам близок к чистому железу, он мягок, пластичен, его твердость HВ = 60…80.
Цементит (Fe3С) – химическое соединение, содержащее 6,67 % углерода. Является составной частью эвтектической смеси, а также самостоятельной структурной составляющей. Образует твердые растворы путем замещения атомами других металлов, неустойчив, распадается при термической обработке. Цементит очень тверд (НВ = 800) и хрупок.
Аустенит – твердый раствор углерода в γ-Fe. Атомы углерода внедряются в кристаллическую решетку, причем насыщение может быть различным в зависимости от температуры и примесей. Устойчив только при высокой температуре, а с примесями Mn, Cr при обычных и даже низких температурах. Твердость аустенита НВ = 170…200.
Перлит − эвтектоидная смесь феррита и цементита; образуется в процессе распада аустенита при 723 оС и содержании углерода 0,83 %. Примеси Si и Mn способствуют образованию перлита и при меньшем содержании углерода. Структура перлита может быть пластинчатой и глобулярной (зернистой). Механические свойства перлита зависят от формы и дисперсности частичек цементита. Прочность пластинчатого перлита несколько выше, чем зернистого.
Ледебурит – эвтектическая смесь аустенита и цементита, образующаяся при 1130 °С и содержании углерода 4,3 %. Структура неустойчивая: при охлаждении аустенит, входящий в состав ледебурита, распадается на вторичный цементит и перлит. Ледебурит очень тверд (НВ = 700), хрупок.
Графит – мягкий и хрупкий компонент чугуна, состоящий из разновидностей углерода. Встречается в серых и ковких чугунах.
Рассматриваемую диаграмму правильнее считать не железоуглеродистой, а железоцементитной, так как свободного углерода в сплавах не содержится. Но содержание углерода пропорционально содержанию цементита, то практически удобнее все изменения структуры сплавов связывать с различным содержанием углерода.
Все линии на диаграмме (см. рис. 24) соответствуют критическим точкам, т. е. тем температурам, при которых происходят структурные изменения в сплавах. Линия ACD – линия начала кристаллизации сплава (линия ликвидуса), линия AECF – линия конца кристаллизации сплава (линия солидуса). Область AESG на диаграмме соответствует аустениту. Линия GS – начало выделения феррита, а линия SE – вторичного цементита. Линия PSK соответствует окончательному распаду аустенита и выделению перлита. В области ниже линии PSK никаких изменений структуры не происходит. Расположение линий GSK и PSK следует учитывать при термической обработке. Линию GSC называют линией верхних критических точек, линию PSK – нижних критических точек.
В зависимости от содержания углерода, %, железоуглеродистые сплавы получают следующие названия:
− при содержании углерода до 0,83 % – доэвтектоидные стали;
− при содержании углерода, равного 0,83 % – эвтектоидные стали;
− при содержании углерода 0,83…2,14 % – заэвтектоидные стали;
− при содержании углерода 2,14…4,30 % – доэвтектические чугуны;
− при содержании углерода 4,30…6,67 % – заэвтектические чугуны.
С увеличением содержания углерода в железоуглеродистых сплавах меняется и структура, увеличивается содержание цементита и уменьшается количество феррита. Чем больше углерода в сплавах, тем выше их твердость и прочность, но ниже пластические свойства. Механические свойства сплавов зависят также от формы и размера частиц структурных составляющих. Твердость и прочность стали тем выше, чем тоньше и мельче частицы феррита и цементита.
