
- •Предисловие.
- •Тема 1. Способы выражения концентрации растворов.
- •Задачи с массовой долей.
- •Посчитать массовую долю если даны массы веществ.
- •Масса по массовой доле.
- •Массовая доля / масса, если даны масса, объем и плотность.
- •Массовая доля и моли
- •Массовая доля и разбавление
- •Задачи с молярной концентрацией.
- •Молярная концентрация и моли
- •Молярная концентрация и объем растворённого газа
- •Молярная концентрация и масса
- •Задачи про моляльность.
- •Моляльность
- •Моляльность и масса
- •Вопросы без расчетов.
- •Вопросы про размерность
- •Разная теоретическая фигня.
- •Формульные вопросы
Не посвящается никому. Ибо нефиг.
Предисловие.
Будучи огорчен качеством преподавания химии в РНИИМУ, и тем более, способом последующего контроля качества образования – тестами, я решил оказать посильную помощь студентам в сдаче оных. Пособие представляет собой краткую, насколько возможно, инструкцию, как минимально загрузив голову таки сдать этот окаянный тест. Я исследовал большое их количество, обобщил результаты.
Тема специфична. Требуются навыки счёта, желательно в уме, но можно и на калькуляторе, главное быстро. Поскольку навыки счёта у студента РНИМУ, как правило, прокачаны плохо, будет сложно. Дорогой любитель химии, обрати пристальнейшее внимание на введение. Приведенные формулы желательно выучить. Не то, чтобы они такие уж необходимые, просто так намного легче решить тест. Вначале я изложил основную концепцию, дальше разобрал кучу примеров. Примеры были мной разделены на разновидности, в соотвествии моими представлениями о типах задач. На каждый вид вопросов я постарался дать ответ, в меру научный, чтобы все-таки не слишком уйти от своих химических корней, но и достаточно ясный, чтобы он мог быть воспринят среднестатистическим студентом. Теперь я представляю свой труд для использования широкой общественностью, надеюсь, моё творение сможет послужить к чьей-нибудь пользе.
Конечно, многим хотелось бы иметь готовые ответы и не париться. Думаю, что за годы работы eois общественность накопила некоторый объем ответов, он постепенно совершенствуется, доля верных ответов растет, уже в 2016 она была больше 70%. Однако, в отношении химии мне это кажется неудачным путем. Объясню, почему такое желание глупо. Во-первых, вопросов большое количество, и они, как назло, очень похожи. Это делает трудным списывание с правильных ответов, и, одновременно, делает тесты уязвимыми к методичкам вот такого плана, с разбором вопросов на группы и злой иронией по этому поводу. Во-вторых, некоторые персонажи, как Карина, например, почему-то борются со списыванием, что делает этот процесс не самым простым трюком. А глядя на всё это глобально, по-моему, все же лучше что-то понимать и мыслить, чем списывать.
Заранее благодарен за адекватные комментарии, дополнения и исправления к тексту. Текст создан исключительно из гуманных соображений и распространяется безвозмездно.
Удачи, ни пуха, ни пера, дорогие любители химии.
Алексей «Леша-химик» Федоров,
11.08.2017.
Тема 1. Способы выражения концентрации растворов.
Введение:
Договоримся об основных понятиях.
Раствор — система, состоящая из растворенного вещества и растворителя.
Растворенным веществом может быть что угодно (соль, сахар, мочевина, кислота, щелочь и так далее).
Растворителем всегда будет вода. Следует отличать растворитель и растворенное вещество! У них разные массы и моли, да и вообще, это разные вещества.
Тест по этой теме по большей части состоит из задач. Для успешной сдачи теста требуется:
Уметь читать и понимать (!) условия задач. Это самое сложное, как нам кажется.
Знать формулы, понимать, что означают буквы в них
Уметь математику. Запасите калькулятор. Успокойтесь, дышите глубже.
Еще раз, схематично и в виде метафоры, пример.
Рассчитайте количество хуиты, происходящей в вашей никчёмной жизни если известно, что ВКонтакте 100500 тупых мемов, при этом у вас 10 анатомии.
Это условия, из них извлечем цифры
Рассчитайте количество хуиты, происходящей в вашей никчемной жизни, если известно, что вконтакте 100500 тупых мемов, при этом у вас 10 анатомии.


ВК = 100500 тупых мемов Ат = 10 анатомий
Ху—?


Это дано. В школе учили так писать.
Сейчас это не обязательно, но помогает
понять, что происходит
Ху = ВК * Ат
Это формула. В этом примере она от балды, дальше будут реальные
ВК = 100500 тупых мемов Ат = 10 анатомий
Ху—?
Ху = ВК * Ат

Ху = 100500*10 = 1005000 хуиты

Ху = 100500*10 = 1005000 хуиты
Ху = 100500*10 = 1005000 хуиты
Это расчёты и ответ, чего и требуется
П

Ху = 100500*10 = 1005000 хуиты
Это расчёты и ответ, чего и требуется
Ху = 100500*10 = 1005000 хуиты
Это расчёты и ответ, чего и требуется
редполагается, что читать и считать более-менее вы умеете, а научить понимать мы не можем. Поэтому остановимся более подробно на формулах. На серьезных формулах, уже без шуток. Обратите внимание на размерности, граммы, литры и т. д. Это важно. Доступны следующие формулы:Массовая доля

Здесь ω – массовая доля в %
mрастворенное вещество — масса растворенного вещества, в граммах
mраствор — масса раствора (неожиданно, правда?), в граммах
100% = 100
Формула имеет вариацию
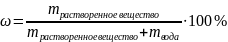
mвода — масса воды (ух, какая неожиданность), в граммах.
Молярная концентрация
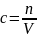
Здесь с — молярная концентрация (также называется молярность), выраженная в моль/литр. Может использоваться обозначение М, например с = 0,01 моль/л, то же самое, что с = 0,01 М (читать как молярность равна 0,01 моль на литр).
n — количество молей растворенного вещества, выраженное в моль.
V — объем раствора, выраженный в литрах. Внимание! Должны быть именно литры. Если в условиях даны миллилитры, то надо переводить. Для этого цифру в мл делят на 1000, например 500 мл = 0,5 литра.
Моляльность

Здесь b — моляльность, выраженная в моль/кг
n — количество моль растворенного вещества
mвода — масса воды (ух, какая неожиданность еще раз), в килограммах. Внимание! Именно килограммы, если даны граммы, то нужно переводить. Перевод аналогичен мл-литры.
Олдскул
Разговор о формулах будет неполным, если мы не приведем еще школьные формулы, а то вдруг кто-то не помнит.
Моли через массу

Здесь n — количество молей, моль
m — масса любого вещества, в граммах. Обычно имеется в виду растворенное вещество.
M — молярная масса этого же вещества
Моли через объем (внимание! Только для газов)
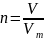
Здесь n — количество молей, моль
V — объем газа, в литрах. Внимание! Только объем газа! Объем раствора не вставлять!!!
Vm — молярный объем, 22,4 литра/моль, константа, короче.
Масса раствора через объем и плотность
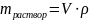
Здесь mраствор — масса раствора (неожиданно, правда?), в граммах.
V — объем раствора в мл.
ρ — плотность, в граммах/мл., эта странная загогулина читается как буква «ро».
Преобразования
Отдельно
рассмотрим вопрос, что делать, когда из
формулы надо что-то выразить. Например,
из формулы
 надо выразить V. В таком
случае нам кажется удобным использовать
способ, предложенный одной блондинкой.
Мысленно заменим буквы на цифры 6, 3 и 2:
надо выразить V. В таком
случае нам кажется удобным использовать
способ, предложенный одной блондинкой.
Мысленно заменим буквы на цифры 6, 3 и 2:
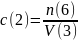 .
Ведь 6 делить на 3 равно 2, же есть? Чтобы
выразить 3, очевидно надо 6 делить на 2:
.
Ведь 6 делить на 3 равно 2, же есть? Чтобы
выразить 3, очевидно надо 6 делить на 2:
 ,
а теперь, убрав цифры, вернемся к
цивильному виду:
,
а теперь, убрав цифры, вернемся к
цивильному виду:
 .
.
Типичные вопросы:
