
- •Лабораторная работа №4
- •Методика выполнения работы
- •Экспериментальные и расчётные величины
- •Обработка экспериментальных данных
- •1) Виды перегонки, схемы.
- •1. Ректификация
- •2. Перегонка при давлении, отличающемся от атмосферного
- •3. Химическое связывание
- •4. Образование тройных азеотропов
- •5. Азеотропная ректификация
- •6. Экстрактивная ректификация
- •3) Насадочные колонны( кольца паля, рашига и тд.) Плюсы, минусы.
Экспериментальные и расчётные величины
|
Исходная смесь |
|||||
|
VF, л |
TF, °С |
xF, мол. доли |
|
nF, кмоль |
mF, кг |
|
9,2 |
112 |
43,39 |
18,2 |
0,236 |
10,13 |
|
Кубовый остаток |
||
|
Tw, °С |
xw, мол. доли |
|
|
124 |
23,22 |
8,07 |
|
Дистиллят (средний состав) |
|||||
|
ρP, кг/м3 |
|
|
|
|
|
|
1003 |
1,3421 |
96,99 |
90,34 |
74,98 |
91,17 |
Обработка экспериментальных данных
 (рассчитано с помощью пакета прикладных
программ Matlab)
(рассчитано с помощью пакета прикладных
программ Matlab)
Масса исходной смеси:
mF = VF*ρF = 9,6*1101,45=10,13 кг
M=MH2O*x+MC2H6O2*(1-x)
MF= 18*0,4339+62*(1-0,4339) = 42,908 кг/кмоль
Mw= 18*0,2332+62*(1-0,2332) = 51,78 кг/кмоль
MP=18*0,9699+62*(1-0,9699) = 19,32 кг/кмоль
Количество исходной смеси:
nF
=
 = 0,236 кмоль
= 0,236 кмоль
Мольное количество кубовой жидкости:
nw=
 = 0.173 кмоль
= 0.173 кмоль
Масса кубовой жидкости:
mW = nw*MW = 0,173*51,78 = 8,958 кг
Средний мольный состав дистиллята:
 =
=
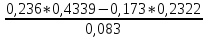 = 74,98
= 74,98
 =
= = 96,99
= 96,99
Погрешность определения состава дистиллята:
Δ%=
 =
=
 = 22,69 %
= 22,69 %
Определение количества теплоты QT, необходимой для разделения смеси вода-этиленгликоль на основании теплового баланса системы:

Значения удельных теплоёмкостей при известном содержании низкокипящего компонента в исходной смеси, дистилляте и кубовом остатке определяются по правилу аддитивности:
 = 4,1829*0,182+2,521*(1-0,182) = 2,823
= 4,1829*0,182+2,521*(1-0,182) = 2,823

 = 4,184*0,9034+2,534*(1-0,9034) = 4,025
= 4,184*0,9034+2,534*(1-0,9034) = 4,025
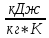
 = 4,1855*0,0807+2,549*(1-0,0807) = 2,682
= 4,1855*0,0807+2,549*(1-0,0807) = 2,682

Теплоёмкости
воды и этиленгликоля находят при средних
температурах
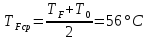 ,
,
 ,
,

Расчёт величин удельных энтальпий исходной смеси и кубового остатка:
 = 2,823*112 = 316,176 кДж/кг
= 2,823*112 = 316,176 кДж/кг
 = 2,682*124 = 332,568 кДж/кг
= 2,682*124 = 332,568 кДж/кг
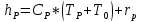 ,
,
где
 ,
,
 – средняя температура дистиллята.
– средняя температура дистиллята.
Значение удельной теплоты парообразования определяется по правилу аддитивности:
 = 2090,73
= 2090,73

 = 4,025*118+2090,73 = 2565,68 кДж/кг
= 4,025*118+2090,73 = 2565,68 кДж/кг
Удельные
теплоты парообразования находят при
средней температуре TP
=
 = 118 °C
= 118 °C
 = 10,13*316,176 = 3202,863 кДж
= 10,13*316,176 = 3202,863 кДж
 = 1,605*2565,68 = 4117,403 кДж
= 1,605*2565,68 = 4117,403 кДж
 = 8,958*332,568 = 2979,144 кДж
= 8,958*332,568 = 2979,144 кДж

3202.863+ = 4117,403+2979,144+0,07*
= 4117,403+2979,144+0,07*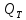
 = 4186,757 кДж
= 4186,757 кДж
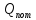 = 293,073 кДж
= 293,073 кДж
|
Исходная смесь |
Дистиллят |
||||||
|
mF, кг |
|
cF,
|
HF, кДж |
mP, кг |
|
HP, кДж |
|
|
10,13 |
18,2 |
2,823 |
3202,863 |
1,605 |
90,34 |
4117,403 |
|
|
Кубовый остаток |
Тепловые потери |
Количество подведенной теплоты |
||
|
mw, кг |
|
Hw, кДж |
Qпот, кДж |
QT, кДж |
|
8,958 |
8,07 |
2979,144 |
293,073 |
4186,757 |
Вывод: в ходе работы было проведено практическое ознакомление с устройством и принципом работы установки простой перегонки на примере разделения жидкой бинарной смеси вода-этиленгликоль; сравнение экспериментально полученных значений количества и качества (состава) дистиллята с величинами, рассчитанными теоретически(погрешность составила 22,69%); определение количества подведённой к системе теплоты, необходимой для разделения бинарной смеси, равного 4186,757 кДж.
Ответы на контрольные вопросы.

 ,
масс. доли
,
масс. доли ,
масс. доли
,
масс. доли
 ,
мол. доли
,
мол. доли ,
масс. доли
,
масс. доли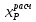 ,
мол. доли
,
мол. доли ,
масс. доли
,
масс. доли ,
,

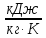

 ,
,