
- •Основные показатели термодинамических процессов идеальных газов в закрытых термодинамических системах Изобарный процесс
- •Изображение изобарного процесса на Рv-диаграмме
- •Изображение изобарного процесса на тs-диаграмме
- •Изохорный процесс
- •И зображение изохорного процесса на Pv-диаграмме
- •Изображение изохорного тп на тs–диаграмме
- •Изотермический процесс
- •И зображение изотермического процесса на Pv-диаграмме
- •И зображение изотермического процесса на ts-диаграмме
- •Адиабатный процесс
- •В заимное расположение адиабаты (I) и изотермы (II)
- •И зображение адиабатного процесса на ts-диаграмме
- •Политропный процесс
Изображение изохорного тп на тs–диаграмме
Соответственно, количество тепла на ТS–диаграмме изохорного ТП определяется площадью под изохорой 1-2, то есть S1-2-3-4-1 .
Долю поступающего (отводимого) в рабочее тело тепла, затраченного на изменение внутренней энергии Du, определим, принимая во внимание 1-й закон термодинамики:
 . (7.2.10)
. (7.2.10)
Следовательно, доля тепла на совершение работы деформирования будет:
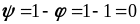 . (7.2.11)
. (7.2.11)
Изотермический процесс
Изотермический процесс, характеризующийся условиями T = const и dT = 0, может протекать, например, в цилиндре поршневого двигателя, в котором по мере подвода (отвода) тепла к газообразному рабочему телу поршень двигателя перемещается по такому закону, при котором объём рабочего тела увеличивается (уменьшается) настолько, что его Т остаётся неизменной.
В этом случае из уравнения Клапейрона получаем:
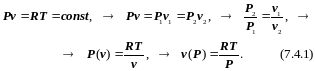
Из (7.4.1) видно, что объём рабочего тела при T = const изменяется обратно пропорционально его Р (закон Бойля-Мариотта). Графиком процесса является изотерма (изотерма (греч.) – линия одинаковой температуры; изо – равный, одинаковый, терм – тепло), представляющая собой на Рv-диаграмме равнобокую гиперболу, для которой координатные оси Р и v служат асимптотами (см. рис. 7.4.1).
И зображение изотермического процесса на Pv-диаграмме
На графике процесс 1-2 является прямым и обеспечивается поступлением тепла в рабочее тело. Процесс же 1-3 является обратным. В этом случае рабочее тело отдаёт тепло в ОС.
Работа деформирования газообразного рабочего тела в изотермическом процессе 1-2 будет:
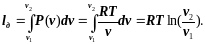 (7.4.2)
(7.4.2)
Принимая во внимание (7.4.1), формулу (7.4.2) можно представить в следующих видах:
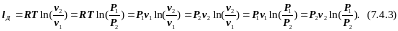
На Рv-диаграмме lд в процессе 1-2 соответствует площади S1-2-4-5-1.
Располагаемая работа в изотермическом процессе 1-2 определяется как
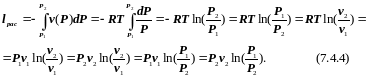
Сравнивая (7.4.3) и (7.4.4), видим, что в изотермическом процессе располагаемая работа равна работе деформирования рабочего тела, то есть в этом процессе вся работа деформирования превращается в полезную работу. Этот факт предопределил применение изотермы в цикле Карно, который является циклом идеальной тепловой машины. Соответственно, на Рv-диаграмме lрас в процессе 1-2 соответствует площади S1-2-6-7-1.
Применительно к изотермическому процессу уравнение (5.3.7) имеет вид du = CV,удdT = 0. Нулю также равняется и изменение энтальпии рабочего тела в этом процессе di = CP,удdT= 0. Принимая во внимание первый вид дифференциального уравнения 1-го закона термодинамики, получаем:
dqТ = du + dlд = 0 + dlД = dlд.
Из данного выражения видно, что в изотермическом процессе всё подводимое (отводимое) к рабочему телу тепло затрачивается на совершение работы его деформирования.
Полученная взаимосвязь между dqТ и dlД позволяет определить изменение энтропии в изотермическом процессе:
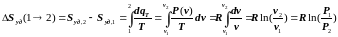 .(7.4.5)
.(7.4.5)
Аналогичный
результат получается и при использовании
для вычисления DSуд(12)
формулы (6.4.3), так как при изотермическом
процессе
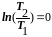 :
:
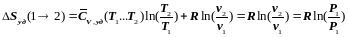
В связи с тем, что в изотермическом процессе теплоёмкость вещества равна бесконечности (см. 4.1), то определить количество тепла, подведённого (отведённого) к рабочему телу в этом процессе при помощи теплоёмкости, нельзя. Это можно сделать только через изменение энтропии в этом процессе. Используя уравнение (6.2.10) и учитывая (7.4.5), получаем:
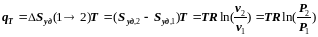 . (7.4.6)
. (7.4.6)
