
- •Этапы получения сверхпродуцентов методами ги
- •Ферменты, используемые в ги: днк-полимераза 1, концевая днк-трансфераза, поли-(а)-полимераза:
- •Пцр, принципы метода.
- •Методы сайт-направленного мутагенеза с использованием пцр.
- •Создание и скрининг генетических библиотек.
- •Конструирование векторов для клонирования на основе плазмид. Векторы, позволяющие проводить прямой отбор гибридных молекул днк.
- •Конструирование векторов для клонирования на основе фага .
- •Клонирование в космидах, фазмидах.
- •Регуляция экспрессии лактозного оперона.
- •Обращенно-фазовая и гидрофобная хроматография белков
- •Ионообменная хроматография белков.
- •Электрофорез белков: электрофорез с использованием додецилсульфата натрия
- •Место мхах в процессе наработки рекомбинантного белка.
- •Хелатирование
- •Несколько слов о мхах
- •Принципы мхах
- •Хелатирующие группы
-
Создание и скрининг генетических библиотек.
Библиотека генов, геномная библиотека – набор клонированных фрагментов ДНК, в совокупности составляющих индивидуальный геном, то есть это все участки одного генома, которые были проклонированы и засунуты в любые генетические конструкции.
Цели создания: поиск и клонирование конкретных генов, установление и изучение структуры генома.
Общий принцип конструирования библиотеки:

Например, у нас есть плазмидный генетический вектор, в котором есть сайты рестрикции для клонирования ДНК. Потом берем ДНК с нужным нам геном, режем ее рестриктазой и той же рестриктазой режем вектор – лигируем и получаем рекомбинантный вектор с интересующим нас геном.
Можно делать то же самое, только с тотальной геномной ДНК:
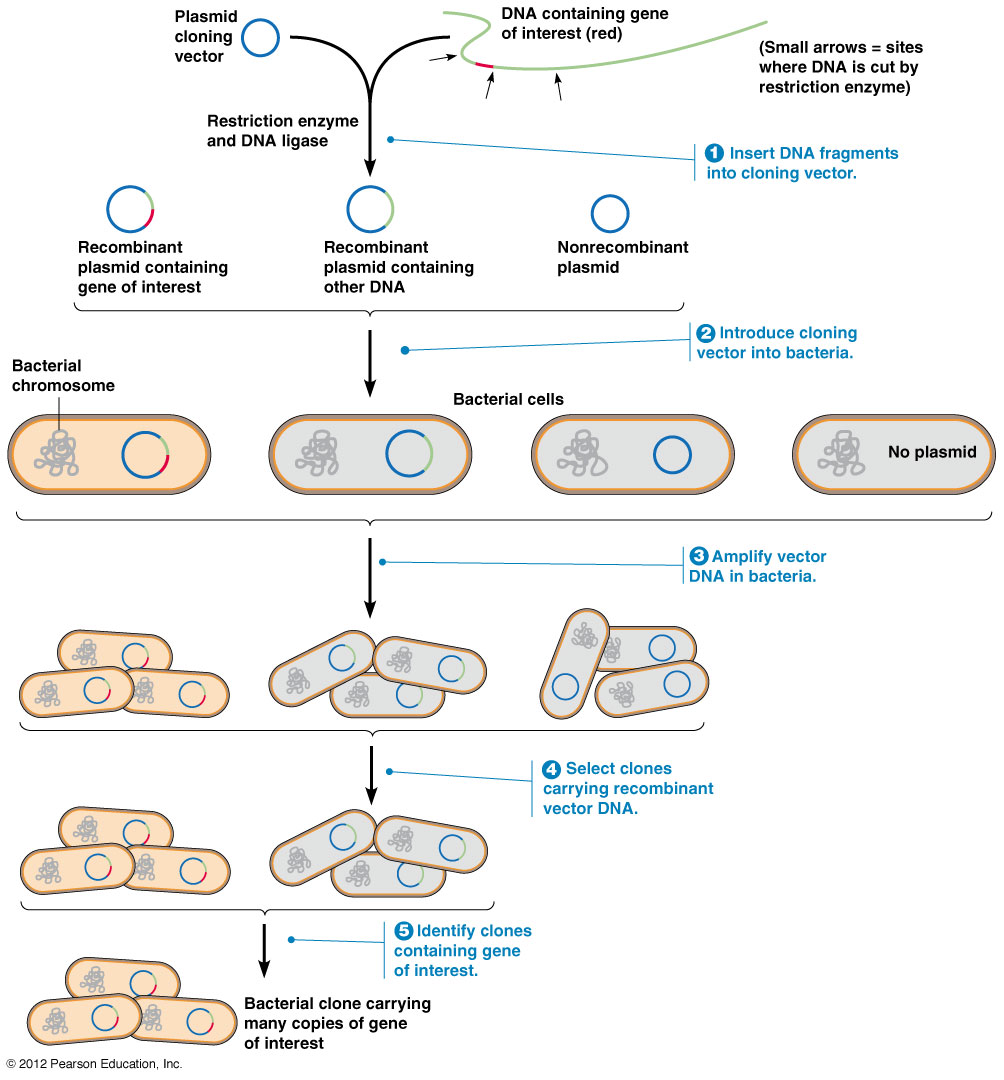
Эту тотальную ДНК мы так же режем рестриктазами, как и вектора, а потом производим лигирование, далее производим ОТБОР – селекцию клонов, ведь куда-то плазмида не попадет, куда-то попадет вектор без участка исследуемого генома или нашего гена.
Это осуществляют следующим образом:

В нашем векторе есть генетические маркеры – гены устойчивости к антибиотику. В этом примере усточивость к ампицилину (ген ApR) данного клона указывает на наличие плазмиды (однако необязательно с целевым геном), а НЕусточипость к тетрациклину (ген TcR) данного клона указывает на то, что вставка целевого гена в вектор произошла успешно (стрелки это сайты рестрикции, поэтому рестриктазы его разрушают). Таким образом, клон, который устойчив к ампициллину, но не устойчив к тетрациклину – это наш целевой клон. Чтобы отобрать такие клоны используют РЕПЛИКАТОР (метод называется репликацией) – клеточную суспензию загружают в углубления, а потом на две чашки петри отпечатывают бактериальную суспензию (на одной чашке только ампициллин, а на другой два антибиотика) – мы берем бактерии с первой чашки, так как на второй нужные клоны умерли. Это непрямой отбор, поэтому он недостаточно удобен.
Прямой отбор может быть осуществлен следующим образом:

Селективный маркер тут представлен ген lacz alpha, кодирущий ФРАГМЕНТ гена бета-галактозидазы (то есть он не активен, называется омега-фрагмент). Когда мы добавляем к омега-фрагменту альфа-фрагмент – ферментативная активность восстанавливается. Соответственно, если мы ген вставили нормально, то фермент работать не будет работать в специальном штамме, где есть этот альфа-фрагмент.
Далее производится отбор синее/белое:

Если в клетку попала плазмида без вставки, то фермент у нее работает, следовательно, под его действием образуется синий окрашенный продукт – мы видим синие колонии. Если вставку сделать удалось, то колония белая. Соответственно, клетки без плазмид вообще мы уже отобрали посредством культивирования с антибиотиком.
Скрининг библиотек (анализ):
Скрининг с помощью гибридизации (ищем ДНК)
Иммунологический скрининг (ищем белок антителами)
Скрининг по активности белка
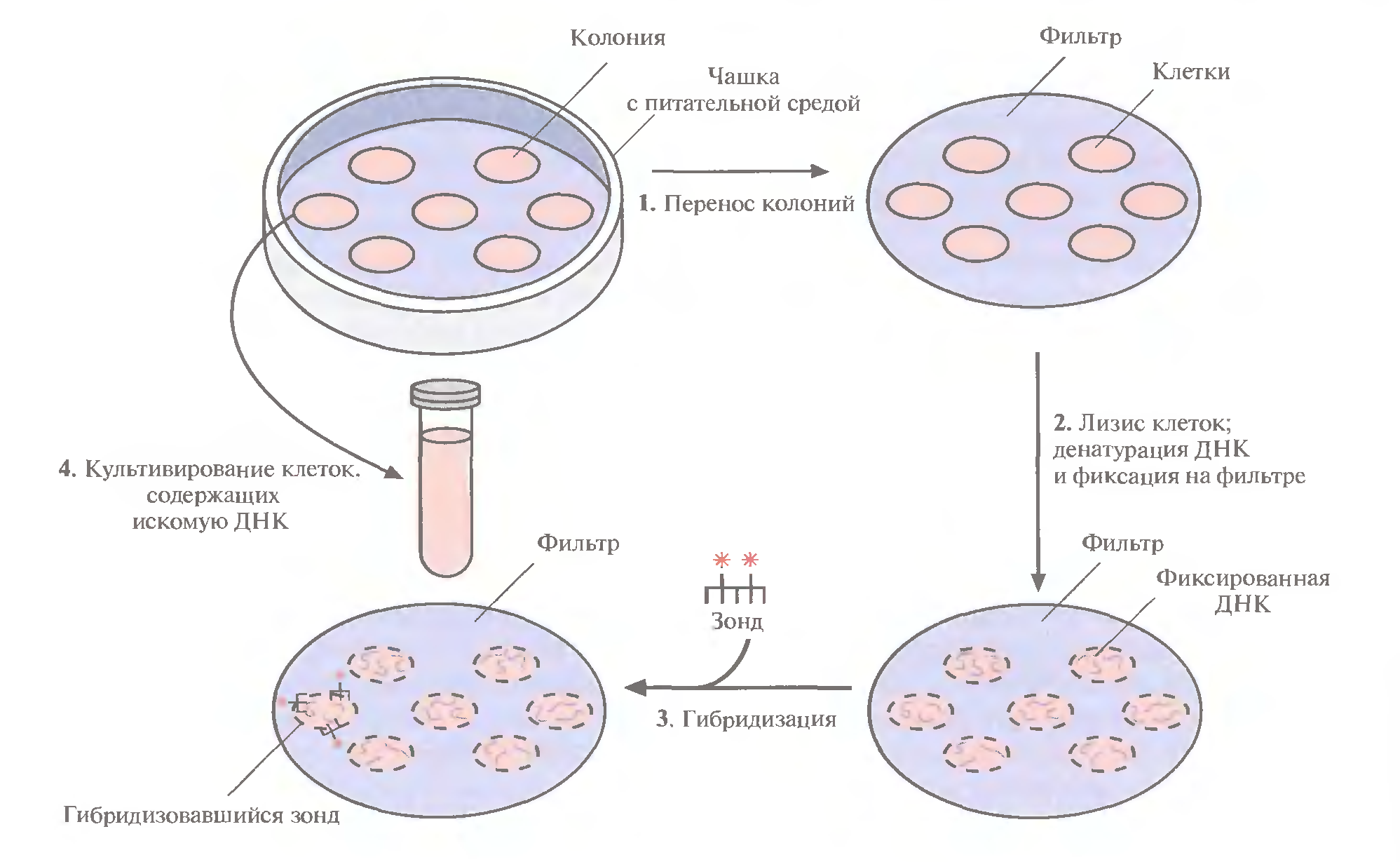
Тут показан скрининг с помощью гибридизации: мы знаем искомую последовательность ДНК, поэтому создаем олигонуклеотидный зонд, который еще и помечен (радиоактивная или флуоресцентная метка).
Если мы не знаем целевую последовательность, то это создает проблему, которую можно решить так:
-
Если ожидается, что гомология высокая, то в качестве зонда может быть выбран олиго- или полинуклеотид с последовательностью родственного гена. На основании сравнения группы родственных генов в качестве зонда может быть выбран участок с высококонсервативной последовательностью.
-
Если известна последовательность или часть последовательности целевого белка, то на ее основе может быть сконструирован вырожденный зонд. На основании сравнения группы родственных белков может быть выбран участок с высококонсервативной последовательностью и на его основе сконструирован вырожденный зонд:

Однако нельзя на основании а/к последовательности определить нуклеотидную последовательность точно. Поэтому создают набор зондов и их используют – это не работает для всех последовательностей, потому что количество вариантов может быть слишком большим.
Следующий подход – иммунологический скрининг:
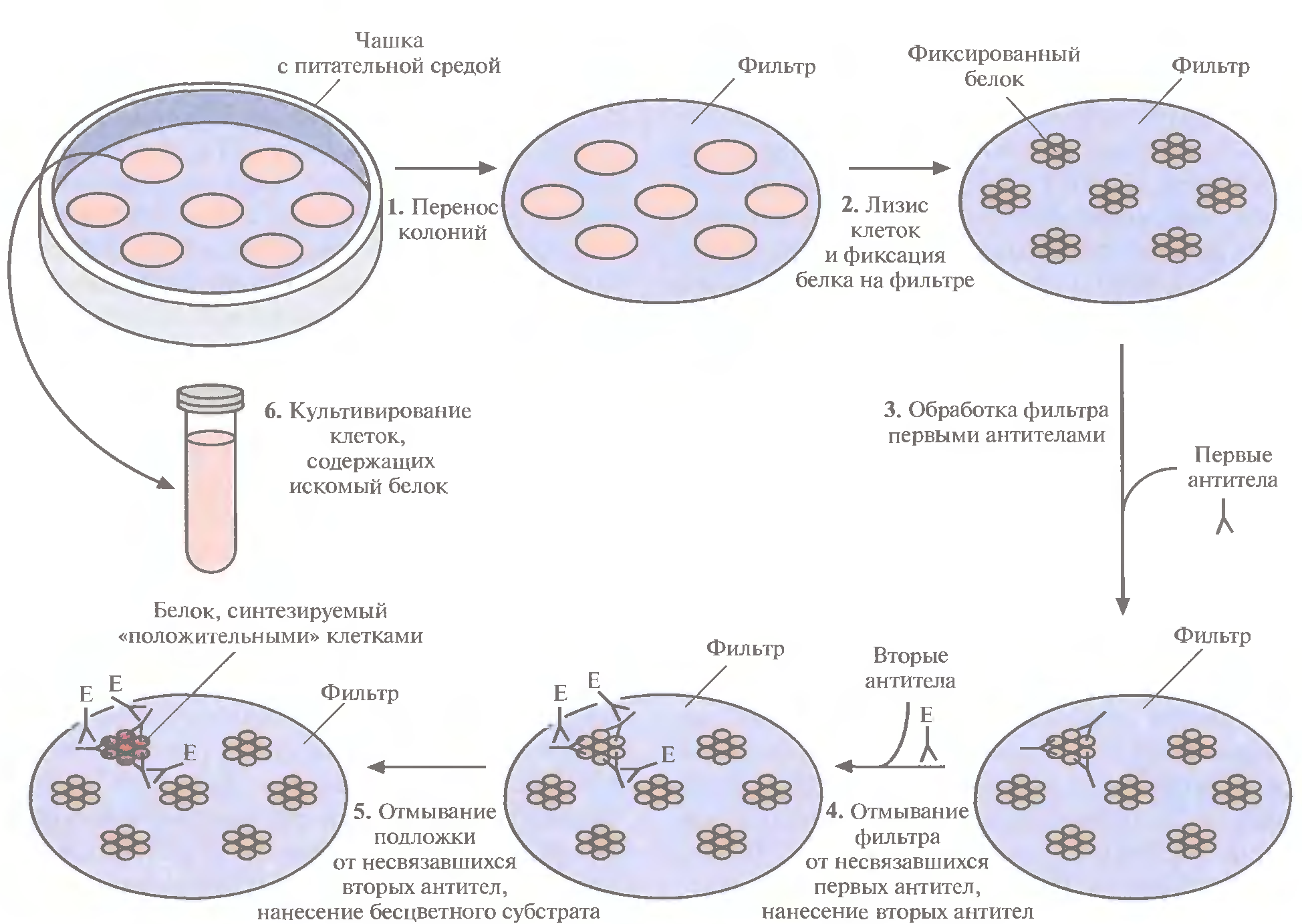
Тут вторичные антитела (которые цепляют первичные) несут метку – ферментативную или радиоактивную.
Поиск белков по активности:

Тут мы сразу видим, что белок принял правильную пространственную структуру, то есть он активен.
В этом примере в среду добавляется молоко, казеин образует мицеллы, и среда становится мутной. Протеаза же разрушает белок и вокруг колоний с протеазами образуются прозрачные участки.

В этом примере в среду добавляется ДНК. Потом чашки обрабатываются соляной кислотой, которая должна осадить ДНК. Однако если в нашей колонии работает ДНКаза, то образуется прозрачный участок на чашке (чтобы лучше эту зону увидеть, можно покрасить зеленым красителем).

В этом примере отбирается наличие липаз. В среду добавляется жир, масло (часто оливковое) + индикатор спиртовой синий, который в кислой среде становится синим, реагируя на образование жирных кислот в ходе работы липазы. Соответвенно, синий цвет – это признак работающей липазы.

В этом примере отбирается наличие амилаз. В среду добавляется крахмал – если он гидролизуется под действием амилаз, то это легко увидеть, если добавить на чашку раствор Люголя. Прозрачные зоны указывают на активность амилаз.
