
ик спектроскоп
.pdfГосударственное бюджетное образовательное учреждение высшего профессионального образования
«САНКТ-ПЕТЕРБУРГСКАЯ ГОСУДАРСТВЕННАЯ ХИМИКО-ФАРМАЦЕВТИЧЕСКАЯ АКАДЕМИЯ»
МИНИСТЕРСТВа ЗДРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ Российской Федерации
КАФЕДРА АНАЛИТИЧЕСКОЙ ХИМИИ
Ю. А. Скорик, А. С. Березин, А. А. Екимов
Методические рекомендации по самостоятельному изучению темы
«ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ»
САНКТ-ПЕТЕРБУРГ «Изд-во СПХФА»
2012
УДК 535.33 М54
Рецензенты:
доц., д.х.н. Булатов А. В. (кафедра аналитической химии СПбГУ), проф., д.х.н. Яковлев И. П. (кафедра органической химии СПХФА)
М54 Методические рекомендации по самостоятельному изучению темы «Инфракрасная спектроскопия»/ сост. : Ю. А. Скорик, А. С. Березин, А. А. Екимов. — СПб. : Изд-во СПХФА, 2012. — 40 с.
ISBN 978-5-8085-0318-2
Методические рекомендации посвящены применению ИК спектроскопии для идентификации органических соединений и предназначены для внеаудиторной самостоятельной работы студентов бакалавриата факультета промышленной технологии лекарств по направлениям химическая технология и биотехнология, а также для студентов фармацевтического факультета СПХФА.
В методических рекомендациях рассмотрены теоретические основы методаИКспектрскопии,приводятсяпримерырешениятиповыхзадач,которые носят ситуационный характер и имеют профессиональную направленность. Используя логику рассуждений обучающих задач, студент самостоятельно учится правильному логическому подходу, необходимому для выполнения самостоятельной работы. Через решение спектральных задач студент получает начальный запас знаний и практических навыков использования ИК спектроскопии в анализе органических соединений.
Рекомендованы методической комиссией факультета промышленной технологии лекарств
ISBN 978-5-8085-0318-2 |
© Санкт-Петербург государственная |
|
химико-фармацевтическая академия, 2012 |
ВВЕДЕНИЕ
В настоящее время инфракрасная (ИК) спектроскопия является одним из основных методов исследования веществ различной химической природы, в том числе и лекарственных субстанций.
Впервые метод стал фармакопейным с 1968 г (ГФ X), где он был рекомендован для контроля качества трех лекарственных веществ: фторотана, оксациллина и метициллина, а в разделе «Общие методы физикохимического, химического и биологического исследования» фармакопеи помещен материал, касающийся вопросов теоретического и практического использования ИК спектроскопии в анализе. Со времени выхода десятого издания фармакопеи число препаратов, при исследовании которых рекомендуется данный метод, значительно выросло, что можно проследить на примере дополнений к фармакопее, издаваемых ежегодно, и отдельно выпускаемых фармакопейных статьях. Так, Международная фармакопея (2008) рекомендует этот метод в анализе половины описанных в ней лекарственных веществ.
ИК спектроскопия занимает важное место в исследовании молекулярной структуры химических соединений, так как любая молекула имеет свой, только ей присущий ИК спектр, состоящий из набора полос поглощения разной частоты и интенсивности. Этот метод широко используется для установления структуры новых биологически активных веществ, получаемых путем химического синтеза или выделяемых из природных объектов (животное или растительное сырье, продукты жизнедеятельности микроорганизмов); при испытании на подлинность и определении доброкачественности лекарственных средств; в контроле технологических процессов в промышленном производстве лекарственных субстанций; для изучения кинетики химических реакций; для выявления природы межмолекулярных взаимодействий. В ряде случаев метод может использоваться для количественного анализа. Достоинством ИК спектроскопии является возможность исследования практически любого неорганического или органического вещества в любом агрегатном состоянии — газе, жидкости, растворах, кристаллах или аморфной фазе.
3
1. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ИНФРАКРАСНОЙ СПЕКТРОСКОПИИ
Молекула может поглощать излучение в результате трех основных процессов; в любом случае она при этом переходит в состояние с более высокой внутренней энергией, причем приращение энергии равно энергии фотона поглощенного излучения (hν). Три типа внутренней энергии квантуются, т. е. энергия может принимать только определенные значения, образуя систему дискретных уровней. Во-первых, молекула вращается вокруг своих различныхосей;находясьнаопределенномуровневращательнойэнергии,молекула может за счет поглощения излучения перейти на более высокий уровень вращательной энергии (вращательные переходы). Во-вторых, атомы или группы атомов в молекуле колеблются друг относительно друга, и энергия этих колебаний также квантуется. Молекула может поглотить дискретное количество энергии и перейти на уровень с более высокой колебательной энергией (колебательные переходы).В-третьих, электроны молекулы могут переходить на болеевысокиеуровниэлектроннойэнергии(электронныепереходы).
ИК спектроскопия — метод исследования, основанный на поглощении веществом инфракрасного излучения, в результате чего происходит усиление колебательных (и отчасти вращательных) движений молекул. Атомы в молекулах никогда не находятся в состоянии покоя, а колеблются относительно каких-то средних положений, поэтому их взаимное расположение периодически меняется. ИК излучение усиливает эти колебания, при этом часть энергии поглощается молекулами, которые переходят из одного колебательного состояния в другое, с более высокой энергией. Именно поэтому ИК спектры называют колебательными.
К инфракрасному относят электромагнитное излучение с длиной волны от 0.8 до 1000 мкм. Энергия, необходимая для возбуждения колебаний атомов в молекуле, соответствует энергии фотона с длиной волны 2.5—25 мкм или волновым числом 400—4000 см-1, т. е. электромагнитному излучению средней инфракрасной области. Области, примыкающие к ней, называются ближней инфракрасной (12500—4000 см-1) и дальней инфракрасной (400—10 см-1). Слова ближний и дальний характеризуют близость к области видимого света.
Процессы, приводящие к появлению аналитического сигнала
ИК спектроскопия дает информацию о частотах колебания связей, так как молекула поглощает инфракрасное излучение с такими частотами, с какими колеблются отдельные связи. Трехатомную молекулу (или трехатомную группировку в составе молекулы) можно представить в виде трех шариков, связанных между собой пружиной (упругой связью),
4
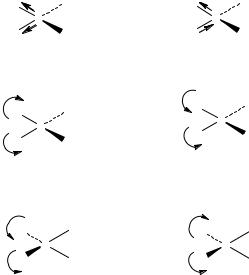
не имеющей массы. В такой системе могут происходить два вида колебаний: валентные и деформационные.
Валентные колебания (ν) — это ритмичные колебания вдоль оси связи, при которых расстояние между колеблющимися атомами увеличивается или уменьшается, но сами атомы остаются на оси валентной связи.
По форме валентные колебания бывают (рис. 1):
•симметричными(vs),еслиобесвязиодновременноудлиняютсяилиукорачиваются, а пары атомов одновременно приближаются или отдаляются;
•асимметричными (vas), если одна из связей укорачивается, а другая — удлиняется, в этом случае приближение и отдаление разных пар атомов происходит не одновременно.
Частота асимметричного колебания всегда выше, чем симметричного.
Деформационные колебания (δ) связаны с изменением валентного угла,
образованного связями у общего атома. Деформационные колебания подраз-
деляются на ножничные, веерные, крутильные, маятниковые (рис. 1). Для возбуждения деформационных колебаний требуется меньшая энергия, чем в случаевалентныхколебанийи,следовательно,ониимеютменьшуючастоту.
|
Валентныеколебания |
H |
H |
C |
C |
H |
H |
симметричные aсимметричные
Деформационные колебания в плоскости
H |
|
H |
|
C |
|
|
C |
|
|
H |
|
H |
|
|
|
|
ножничные маятниковые
Деформационныеколебания внеплоскости
H |
H |
C |
C |
H |
H |
крутильные |
веерные |
Рис. 1. Валентные и деформационные колебания метиленовой группы
5
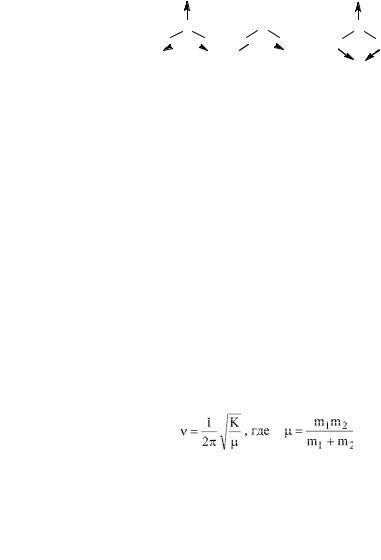
С увеличением числа атомов в молекуле число возможных колебаний быстро растет. В реальной молекуле колебания атомов тесно связаны друг с другом и взаимодействуют между собой. Спектры молекул представляют собой сложный набор различных колебаний, каждое из которых проявляется в узком интервале частот. Общее число линий (полос поглощения) в спектре, связанных с колебаниями атомов, определяется для нелинейной молекулы формулой 3n—6 основных колебаний и 3n—5 для линейной молекулы, где n — число атомов в молекуле. Например, трехатомная молекула воды имеет три вида колебаний — два валентных (симметричное и асимметричное) и одно деформационное (рис. 2).
O  O O
O O
H
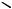 H H
H H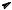
 H H H
H H H
Валентные Деформационное
Рис. 2. Типы основных колебаний молекулы воды
Фактически число полос в спектре не всегда равно расчетному числу. Оно может уменьшаться вследствие того, что часть полос не проявляется в ИКспектре,чтосвязаносостепеньюсимметриимолекулы.Уменьшениечисла полос происходит из-за того, что для достаточно симметричных молекул различные колебания могут иметь одинаковые частоты, и в результате этого вспектрепроявляетсявместодвух-трехлишьоднаполоса.ИКспектрможет также усложняться, поскольку большинство молекул являются в большей или в меньшей степени ангармоническими осцилляторами, частота колебаний которых зависит и от амплитуды. В них возможны переходы на более высокие энергетические уровни, вследствие чего в ИК спектре появляются дополнительные полосы поглощения, называемые обертонами.
Частота колебаний связи зависит от
•вида колебания;
•массы атомов, участвующих в образовании связи;
•прочности связи.
Валентные колебания имеют бóльшую частоту, чем деформационные колебания тех же связей. В идеальном случае частота валентного колебания описывается уравнением:
,
К — постоянная, характеризующая прочность связи, μ — приведенная масса атомов, участвующих в образовании связи.
6
Таким образом, частота колебания возрастает при повышении прочности связи и уменьшении приведённой массы атомов. ИК излучение способно влиять только на такие колебания, которые приводят к изменению дипольного момента молекулы. Если частота колебаний образующегося диполя и ИК излучения, попадающего на него, близки, то взаимодействие между ними может усиливать амплитуду колебаний. Энергия, необходимая для увеличения амплитуды колебаний диполя, поглощается в виде фотона из проходящего потока ИК излучения. Колебания, приводящие к изменению дипольного момента молекулы и способные приводить к появлению полосы поглощения в ИК спектре, называются активными в ИК спектре. Если дипольный момент молекулы в процессе колебания не изменяется, то поглощения ИК излучения не происходит. По этой причине такие вещества, как O2 или N2 не поглощают ИК излучения.
Частоты колебания связей бывают характеристические и нехарактери-
стические. Характеристические (в основном валентные) частоты —
это такие частоты, которые соответствуют группе атомов, поглощающих ИК излучение в узком интервале частот почти независимо от строения остальной части молекулы.
Нехарактеристические частоты — область частот (400–1000 см–1),
где проявляются многочисленные, не поддающиеся отнесению валентные колебания связей С–С, С–N, С–О и деформационные колебания. Нехарактеристическиеколебаниясоставляютосновнуючастьспектраидлякаждого вещества имеют свой, неповторимый набор полос.
ИК спектр представляет собой график зависимости относительной интенсивности прошедшего через вещество излучения в процентах (процент пропускания) от длины волны (λ) в микрометрах (мкм) или волнового числа (1/λ) в обратных сантиметрах (см–1). Волновое число обычно называют частотой. Хотя поглощение энергии квантовано, однако ИК спектр состоит не из узких линий, а из полос. Это происходит потому, что каждое изменение колебательной энергии сопровождается изменением вращательной энергии, и к колебательному переходу прибавляются вращательные переходы, значительно уширяющие сигнал. Пропускание ИК излучения фиксируется как ослабленная интенсивность I, прошедшего через образец излучения, по отношению к исходной интенсивности Io:
Т% = I/Io · 100 %
ИК спектроскопия используется для определения функциональных групп в молекуле изучаемого соединения. Совпадение частоты сравни-
7
ваемой полосы с табличным интервалом частот говорит о возможном, но не обязательном нахождении в молекуле определенного структурного фрагмента. Для идентификации органического соединения сравнивают его спектр со спектрами известных соединений.
2. АППАРАТУРА И ТЕХНИКА ЗАПИСИ ИК СПЕКТРОВ
2.1. Устройство и принцип действия ИК спектрометров
В основе получения ИК спектра лежит облучение исследуемого образца ИК излучением с постепенно изменяющейся частотой с помощью прибора — ИК спектрометра.
К диспергирующим приборам относятся сканирующие ИК спектрометры, а к недиспергирующим — ИК спектрометры с Фурье преобразованием.
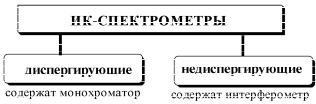
Принципиальная схема двулучевого ИК спектрометра (рис. 3) сходна со схемой УФ спектрофотометра, однако конструкция прибора сложнее. ИК излучение является тепловым; его источником обычно служит термостойкий стержень, раскаляемый проходящим электрическим током. С помощью системы зеркал световой поток от источника излучения разделяется на два одинаковых луча, один из которых пропускается через кювету с веществом, другой — через кювету сравнения. Прошедшее через кюветы излучение поступает в монохроматор, состоящий из вращающейся призмы (или дифракционной решетки), зеркала и щели, позволяющий выделять излучение со строго определенной частотой и плавно изменять эту частоту. Интенсивности двух световых потоков (основного и луча сравнения), прошедших через монохроматор, автоматически вычитаются одна из другой. Электрический импульс, образующийся при попадании результирующего светового потока на детектор типа термопары, усиливается и регистрируется компьютером. Полученная зависимость представляет собой ИК спектр в виде зависимости поглощения или пропускания (в %) от волнового числа (в см-1) или длины волны (в мкм).
8
Рис. 3. Блок-схема двулучевого сканирующего ИК спектрометра
Современная ИК спектроскопия уже представляется нераздельно связанной с принципом преобразования Фурье. Благодаря лучшим (на порядок!) пределам обнаружения и быстроте регистрации спектров в сочетании с возможностями компьютерной обработки, были открыты области применения, абсолютно недоступные для дисперсионного оборудования. ИК-Фурье спектрометры с помощью интерферометра Майкельсона без разложения света на составляющие частоты генерируют интерференционный сигнал — интерферограмму, которая в результате частотногоанализа(преобразованияФурье)преобразуетсявспектр.Хотя интерферометр Майкельсона известен еще с начала XX века, однако выполнение сложного математического преобразования интерферограммы в спектр стало возможным только с появлением современной вычислительной техники.
На рис. 4 представлена принципиальная схема ИК-Фурье спектрометра. Важными элементами конструкции интерферометра являются неподвижное и подвижное зеркала и светоделитель. Светоделитель расщепляет поступающее от источника излучение на две равные части, которые направляются в разные стороны. Одна часть света попадает на неподвижное зеркало, другая — на подвижное (сканер). После отражения зеркалами обе части излучения вновь объединяются тем же самым светоделителем. На оптическом пути между светоделителем, образцом и детектором оказывается излучение из обоих плеч интерферометра. Результатом измерения является функция зависимости интенсивности излучения от изменения длины пути Δs подвижного зеркала. Эта функция называется интерферограммой.
9

Рис. 4. Компоненты ИК-Фурье спектрометра
Запись интерферограммы осуществляется в результате перемещения подвижного зеркала в прямом и обратном направлениях. Соответствующее положение этого зеркала точно определяется с помощью лазера. Интерферограмма, пример которой представлен на рис. 5, пересчитывается в собственно ИК спектр с помощью преобразования Фурье.
Рис. 5. Интерферограмма
2.2. Источники инфракрасного излучения и принципы детектирования
ИК излучение для облучения вещества получают с помощью тепловых источников, таких как глобар или штифт Нернста.
10
