
- •Переваривание белков.
- •Общие пути обмена ак
- •I этап непосредственное трансдезаминирование ак
- •II этап трансдезаминирование глутаминовой к-ты
- •Клиническое значение аминотрансфераз.
- •Общая схема декарбоксилирования ак
- •Образование гистамина.
- •Образование серотонина
- •Образование гамма-аминомаслянной кислоты (гамк)
- •Образование катехоламинов
- •Обезвреживание биогенных аминов
- •Гниение белков в кишечнике
- •Обмен и обезвреживание аммиака
- •Механизмы обезвреживания аммиака
- •Суммарное уравнение реакции
- •4 Способ – образование аммониевых солей
- •Превращение углеродных скелетов
- •Обмен глицина
- •Обмен серина
- •Обмен серосодержащих аминокислот
- •Обмен цистеина
- •Обмен ароматических аминокислот
- •Обмен триптофана
- •Обмен дикарбоновых кислот
Обмен серосодержащих аминокислот
Из серосодержащих аминокислот образуются такие биологически активные вещества, как глутатион, инсулин, липоевая к-та, витамин В1 и многие ферменты.
Метионин донатор метильной группы при образовании адреналина, креатина и холина, а также участвует в синтезе цистеина. Активной формой метионина является его производное с адениловой кислотой – аденозил – S – метионин.
|
Метионин NН2 – СН – СООН │ (СН2) │ S – СН3 |
|
|
|
|
|
|
а
|
|||
–
Креатин Адреналин Холин |
|
Гомоцистеин + серин Ц
Цистеин |
|
Креатин и холин играют для организма важную роль. Креатин участвует в энергетике мышц, холин способствует быстрому удалению из печени ЖК, поэтому метионин применяют как липотропное лекарственное средство. Сера метионина также играет важную роль в образовании других серосодержащих АК.
СН2 – S – CH3 |
|
СН2 – SH |
│ |
|
│ |
CH2 |
- CH3 |
CH2 |
│ |
|
│ |
CH – NH2 |
|
CH – NH2 |
│ |
|
│ |
COOH Метионин |
|
COOH Гомоцистеин |
2-3)

4)

Т.о. цистин и цистеин могут заменять метионин, т.е. она не является полностью незаменимой АК. Цистин и цистеин снижают потребность в метионине ≈ на 90% .
Обмен цистеина
SH – группа цистеина легко окисляется и восстанавливается, что обеспечивает ее участие в процессах биологического окисления. Цистеин участвует в образовании гормонов – инсулина, АКТГ, а также КоА, глутатиона и др.
-
Глутатион
Ц
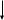 истин
истинH S – КоА

+гли
глу
Ц
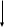 истеин
истеинNH2 – CH – COOH
│
CH2 – SH
+ Пантотеновая
к-та
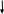
П ВК
Ц
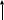 истеиновая
к-та
истеиновая
к-таТаурин
Обмен ароматических аминокислот
Фенилаланин – это незаминимая аминокислота, при ее достаточном поступлении с пищей тирозин полностью заменим.
Из тирозина в организме человека и животных образуется несколько гормонов – тироксин (гормон щитовидной железы), норадреналин, адреналин, а так же глюкоза, жирные кислоты, пигмент меланин и другие соединенияю в организме. Т ирозин образуется путем окисления фенилаланина. В тканях тирозин окисляется до СО2 и Н2О. если в белках пищи будет отсутсвовать фенилаланин, то образование гормонов тироксина и адреналина будет снижено, что в свою очередь повлияет на обмен жиров, белков и углеводов.
Ф
|
Т |
|
|||
|
|
||||
Г |
3,4-дигидроксифенилаланин (ДОФА) |
||||
|
|
Гомогентизиновая к-та |
|
||
|
|
|
Меланин |
||
Ф |
|
|
|||
|
|
Ф умарилацетоуксусная кислота |
|
||
Фениллакта |
Фенилацетат |
|
|
||
|
|
СО2 + Н2О |
|
||


 денозил
– S
– метионин
денозил
– S
– метионин СН3
СН3
 истатионин
истатионин енилаланин
енилаланин
 ирозин
ирозин
 идроксифенилпируват
идроксифенилпируват енилпируват
енилпируват
 СО2
СО2