

2 ФІЗИКО - ХІМІКА МЕТОДІВ ВИРОБНИЦТВА
2.1 Гідроочищення сировини. Сутність процесу
Метою гідроочищення сировини є перетворення і видалення речовин, дезактивуючи платиновий каталізатор риформінгу. До цих речовин відносяться: сірчисті, азотисті і кисневмісні з'єднання, утримуючі метали і галогени, ненасичені вуглеводні.
Процес гідроочищення вихідної сировини заснований на реакціях помірної гідрогенізації, у результаті яких органічні сполуки сірки, кисню й азоту перетворюються у вуглеводні з виділенням сірководню, води й аміаку.
Перетворення зазначених речовин відбувається на гідруючому каталізаторі. Леткі продукти – сірководень, аміак, вода, хлористий водень видаляють шляхом відпарки гідрогенізату. Металеві домішки відкладаються на каталізаторі гідроочищення.
Вміст і склад сірчистих з'єднань у нафтових фракціях залежить лише від природи нафти і методів її переробки; кисневі ж з'єднання можуть утворюватися при автоокисленні деяких вуглеводневих фракцій, головним чином під час збереження й експлуатації в двигуні. Причому продуктів окислювання може бути більше, ніж кисневих з'єднань, що прийшли у фракцію із сировини. Кількість їх залежить від наявності нестабільних вуглеводнів, тривалості і умов окислювання, нагромадження інгібіруючих автоокислених з'єднань і ін.
Сірчисті з'єднання в прямогонних бензинах представлені меркаптанами, сульфідами, ди- і полісульфідами, тіофенами. Зі збільшенням молекулярної ваги сірчистого з'єднання, коли відношення маси сірки до маси вуглеводневого радикала падає, специфічні властивості сірчистих з'єднань виявляється слабкіше. Високомолекулярні сірчисті з'єднання мало стабільні, піддані окислюванню в порівняно м'яких умовах, а продукти окислювання сприяють збільшенню вмісту смол в вуглеводневому середовищі.
У продуктах вторинного походження переважають циклічні з'єднання сірки ароматичного характеру – тіофени. Крім того, у бензинах можлива наявність елементарної сірки, що утвориться при термічному розпаді сірчистих з'єднань у процесі перегонки й у результаті окислювання сірководню при контакті з повітрям.
З перерахованих сполук найгірше піддаються перетворенням циклічні з'єднання сірки – тіофени.
Існують різноманітні методи очищення паливних фракцій від сірчаних, азотистих з'єднань: гідроочистка, сульфідування, екстракція, лужна обробка й ін. Більша частина цих методів заснована на руйнуванні нафта сірчаних з'єднань до сірки, азотистих до аміаку або на видаленні їх разом з смолистими відходами.
На відміну від інших гідрогенизаційних процесів, процес гідроочищення проходить у порівняно м'яких умовах, однак і йому властива сукупність ряду рівнобіжних і послідовних реакцій, у яких беруть участь усі компоненти, що утримуються у вихідній складній суміші [12].
2.2 Основні реакції гідроочистки
2.2.1 Основні реакції гідрування вуглеводнів
До основні реакції гідрування вуглеводнів належать реакції:
- насичення алкеновими зв'язками
RCH2 CH = CHCH3 + H2 → RCH2 CH2 CH2 CH3

+ Н2 → ( 2.1)
- насичення ароматичних зв'язків:

+ 3Н2 → (2.2)
- крекінг алканів
RCH2 CH2 R + H2 → 2RCH3 (2.3)
- Деалкілювання алкіл бензолів

 RCH3
R'НС3
RCH3
R'НС3
+ Н2 → + СН4 (2.4)
- крекінг циклоалканів

+ H2 → CH3 CH2 CH2 CH2 CH2 CH3 (2.5)
- гідроізоляція алканів
 CH3
CH2
CH2
CH2
CH3
+ H2
→ CH3
CH2
CH CH3
(2.6)
CH3
CH2
CH2
CH2
CH3
+ H2
→ CH3
CH2
CH CH3
(2.6)
CH3
Інтенсивність кожної з цих реакцій може змінюватися в широких межах у залежності від умов процесу і типу каталізатора.
При гідроочищенні на алюмокобальтмолібденовому каталізаторі не спостерігається помітного гідрування бензольного кільця. Біциклічні ароматичні вуглеводні в значній частині гідруються до тетралінів, поза залежністю від їхньої вихідної концентрації в сировину [9].
Реакція ізомеризації парафінових і нафтенових вуглеводнів в залежності від властивостей каталізатора спостерігається тією чи іншою мірою при будь-яких умовах обезсірчення.
2.2.2 Основні реакції сірководневмісних з'єднань
Реакції каталітичного гідрогенолізу сірководневмісних з’єднань, що лежать в основі процесу гідроочищення нафтопродуктів, вивчені досить докладно.
Схеми реакцій каталітичного розкладання основних сірчистих з'єднань у присутності водню можна представити в такий спосіб [10,12]:
Меркаптани:
R – SH + H2 → RH + H2S (2.7)
Меркаптани є аналогами спиртів або фенолів. М'якими окислювачами або киснем повітря меркаптани окисляються до дисульфідів R – S – S – R `.
При глибокому окислюванні меркаптанів утворяться сульфокислоти:
RSH → RSO3H (2.8)
Реакційна здатність і корозійна активність меркаптанів у більшій мірі залежить від будови вуглеводного радикала.
Дисульфіди:
R – S – S – R + 3H2 → 2RH + 2H2S (2.9)
Це сірчисті з'єднання з двома, рідше з більш ніж двома, зв'язаними між собою атомами сірки. Дисульфідів у нафтових фракціях утримується приблизно стільки ж, скільки меркаптанів. При нагріванні вони легко розкладаються на меркаптани, сірководень і вуглеводні; у той же час дисульфіди самі є продуктами м'якого окислювання меркаптанів.
Всі органічні сполуки двовалентної сірки відновлюються воднем до відповідних вуглеводнів і сірководню.
Склад сірчистих з'єднань не менш складний, чим вуглеводний склад нафтових дистилятів, у розчинах яких вони знаходяться.
Сульфіди:
R – S – R` + 2H2 → RH + R'Н + H2 S (2.10)
Ациклічні сульфіди
 + 2H2
→ CH3
CH2
CH2
CH3
+ H2
S (2.11)
+ 2H2
→ CH3
CH2
CH2
CH3
+ H2
S (2.11)
S
Біциклічні сульфіди

 CH3
CH3
+ 2H2 → + H2 S (2.12)
S
CH3
Вони є аналогами простих ефірів. Крім сірки до складу їхніх молекул входять звичайно парафінові або циклопарафінові радикали.
При дії сильних окислювачів (Н2О2 або НNО3) сульфіди перетворюються в сульфооксиди і сульфони:
O
O O ||
R – S – R ` → R – S – R ` → R – S – R` (2.13)
|| ||
O O
При цьому можуть протікати побічні реакції окислювання вуглеводневого ланцюга. Однак слід зазначити, що ароматичне кільце пасивує молекулу сульфіду в наслідок сполучення неграничних пар електронів атома сірки з - електронами ароматичного кільця.
Характерним для сульфідів є також утворення комплексів донорно-акцетного типу. Було встановлено, що при взаємодії природних нафтових сульфідів з йодом, бромом, галоїдними алкілатами і галоїдпохідними металів (AlBr3, SnCl4, TiCl4, HgCl2) виходять міцні комплекси.
При підвищених температурах нафтові сульфіди розпадаються з розривом зв'язків C-S і утворять складну суміш, що складається з вуглеводнів, меркаптанів, сірководню й ін.
Тіофени:
 H2
Н2
H2
Н2
+ 2H2 → → → C4 H10 + H2 S (2.14)
S S SH
тіофен
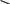

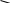 СН2
СН3
СН2
СН3
 +
3H2
→
+ H2
S (2.15)
+
3H2
→
+ H2
S (2.15)
S
бензотіофен

 +
H2
S
+
H2
S

+ ХН2 + Н2 S (2.16)
S
+ H2 S
Тіофени малореакційно здатні, як і ароматичні вуглеводні. Атом сірки в кільці інертний. У перерахованих реакціях первинної є розрив зв'язку вуглець – сірка і приєднання водню до осколків молекули, що утворяться.
Меркаптани, сульфіди і дисульфіди легко гідруються у відповідні вуглеводні вже при порівняно легких умовах. У залежності від будівлі сірчистих з'єднань глибина їх гідрогенолізу різна. Стійкість сірчистих збільшується в наступному ряді.
меркаптан < дисульфід < сульфід < тіофен
Всередині групи сірчистих з'єднань швидкість обезсірчення зменшується із збільшенням молекулярної маси. Так, етілмеркаптан менш стійкий, чим децілмеркаптан.
Міцність S – S - зв'язків у дисульфідах з аліфатичними радикалами, починаючи з диетілсульфіда і кінчаючи діоктандецилсульфідом, не залежить від довжини алкільних ланцюгів. Міцність зв'язків S – S у дисульфідах з ароматичними [9]. В циклічних сульфідах, наприклад тіофенах, кільця піддаються розривові з наступним відщіпленням сірководню й утворенням відповідного вуглеводню.
Тіофен, бензотіофен і дібензотіофен спочатку гідруються до похідних тіофену, що при наступному гідруванні перетворюються в парафінові й алкілароматичні вуглеводні. Насичення ароматичних кілець в умовах гідроочищення не відбувається. Воно можливе при більш жорстких умовах гідрування. Найбільше важко вступають у реакції гідрування тіофен і його гомологи.
Для більш повного перетворення тіофенів і його гомологів необхідні більш низькі об'ємні швидкості при високому парціальному тиску водню. Обезсірчення тіофену може бути глибоким при гідрогенолізі, вуглеводні піддаються гідрокрекінгу з утворенням метану [12].
Склад сірчистих з'єднань не менш складний, чим вуглеводній склад нафтових дистилятів, у розчинах яких вони знаходяться. Як ілюстрації в табл.2.1 надана характеристика сірчистих з'єднань дистилятних фракцій сірчистих нафт. [5].
Сірчисті з'єднання взаємодіють також з металевими й оксідметалевими каталізаторами, завдяки переходу їх у сульфідну форму. У залежності від складу каталізатора це приводить до його активування або викликає отруєння чи дезактивацію.
