
- •4 Валеологічні індекси та показники.
- •Ізометричне - розвивається напруга але не міняється довжина м’язу, таке скорочення називають статичним.
- •Концентричне (міометричне) – максимальний опір, який м’яз здатен подолати на шляху відповідного руху.
- •Ексцентричне (іліометричне) – виникає при опорі зовнішній силі під впливом якої м’язи розтягуються, тобто їх довжина збільшується.
- •Причини активної гіперемії
- •Причини венозної гіперемії
- •13 Де рекомендується вимірювати жирову складку для визначення складу маси тіла чоловіків
- •24 Історія вживання алкоголю.
- •Симптоми емболії
- •29 Кількісні та якісні методи визначення алкоголю в організмі.
- •30. Класифікація алкогольних напоїв та тютюнових виробів.
- •37. Методи дослідження гостроти зору та кольоросприйняття.
- •47 Непрямі методи визначення анаеробної продуктивності
- •48 Новітні методи лікування наркозалежності.
- •53 Оцінка функцій дихальної системи
- •54 Оцінка функціонального стану нервової системи
- •62 Поняття про фізичний розвиток.
- •63 Проби і тести для визначення рівня функціонування серцево-судинної системи.
1 Алергія та алергени. Їх види Алергі́я (грец. αλλος — інший і εργον — дія) — змінена чутливість організму тварин і людини до чужорідних речовин (здебільшого білкової природи), що вводяться повторно. Речовини, які викликають алергію (т. з. алергени), здебільшого мають білкову природу (тваринні та рослинні білки, білкові речовини мікроорганізмів). Алергени можуть потрапляти в організм через шкіру і слизові оболонки або надходити в кров з вогнищ запалення. Прояви алергії виникають лише тоді, коли перше і повторне надходження алергену розділені певним проміжком часу (не менше 5–7 днів). До проявів алергії належать протилежні за своїми ознаками, але спільні за первинним механізмом явища зміненої реактивності організму — анафілаксія (підвищення чутливості до шкідливої дії алергену) та імунітет (зниження чутливості внаслідок посилення опірності організму). Механізм виникнення алергії: коли алерген потрапляє до організму на його знешкодження виділяються певна кількість антитіл, проте якщо в організмі є якісь порушення, то їх виділиться в надлишку, що призведе до виділення надлишку високомолекулярних сполук, які і спричиняють розвиток алергії. Різновиди алергенів за походженням:
побутові: домашній пил, книковий пил, дафнії
епідермальні: хутро, пух, перо, лупа, екскременти, слина домашніх тварин, епідерміс людини
інсектні: синантропні мікрокліщі, таргани, жалячі і кровосисні комахи, павукоподібні
пилкові: пилок рослин
харчові: потенційно — будь-який продукт харчування, але особливо — червоні фрукти (полуниця, малина,, абрикос, цитрусові), молоко, риба і морепродукти, шоколад, горіхи
лікарські: потенційно — будь-які лікарські препарати, в тому числі і протиалергічні
грибкові: частіше плісняві і дріжджові гриби, як компонент домашнього пилу
гельмінтні: антигени аскарид, гостриків, волосоголовців та інших гельмінтів
Особливості алергенів, що проникають через дихальні шляхи
всі вони є білками, що відносяться до категорії Т-залежних антигенів
висока розчинність в умовах вологого середовища дихальних шляхів обумовлює швидку дифузію алергенів із вдихуваних частинок
низька молекулярна маса забезпечує алергенам відносно вільне проникнення у слизову оболонку
низька провокуюча доза сприяє залученню до відповіді хелперних CD4 Т-клітин; продукція цими клітинами інтерлейкіна-4 забезпечує переключення синтезу імуноглобулінів у В-клітинах на IgE-ефекторну молекулу алергічних реакцій
2 Атрофія, дистрофія, гіпертрофія та їх види Гипертрофия (от греч. hyper – чрезмерно, trophe – питание) – увеличение органа или ткани за счет ее паренхиматозных элементов. Реализуется как за счет гиперплазии клеток, так и увеличения размеров отдельных клеток. Это происходит в тех случаях, когда функциональная нагрузка велика и длительна, гиперплазия ультраструктур клетки достигает высоких степеней, масса последней увеличивается, и, наблюдая это в светооптическом микроскопе, мы говорим о гипертрофии клетки. В органах, клетки которых не размножаются (миокард, ЦНС), этот процесс выражается исключительно в гиперплазии ультраструктур и соответственно в гипертрофии клеток. Там же, где клетки способны размножаться, орган увеличивается как за счет гипертрофии клеток, так и их гиперплазии. Таким образом, гипертрофия, в принципе, есть «внешнее» выражение высокой степени гиперплазии. Клинико морфологически различают следующие виды гипертрофии: 1. Рабочая или компенсаторная, которая возникает под воздействием усиленной нагрузки, предъявляемой к органу или ткани. В физиологических условиях примером рабочей гипертрофии является увеличение массы поперечно-полосатой мускулатуры у спортсменов и лиц тяжелого физического труда. В условиях болезни или патологического процесса органу или его части приходится усиленно функционировать. Такой вид гипертрофии обычно встречается в полых органах: желудочно-кишечный тракт, мочевой пузырь. В клинической практике большое значение имеет рабочая гипертрофия сердца. Морфологически различают два вида гипертрофии этого органа: концентрическая – когда происходит утолщение миокарда без расширения полостей сердца и эксцентрическая – сопровождающаяся значительным расширением полостей сердца. Концентрическая гипертрофия развивается, как правило, при артериальной гипертензии и симптоматических артериальных гипертониях и обычно касается стенки левого желудочка. Толщина его стенки может достигать 3-х и более сантиметров (при норме – 1,2см). Эксцентрическая гипертрофия возникает при пороках сердца, когда в его полостях накапливается остаточная кровь. При этом размеры сердца могут достигать больших размеров, как это бывает при аортальных пороках. Микроскопически кардиомиоциты увеличиваются в объеме, неравномерно утолщаются. Их ядра становятся крупными, гиперхромными. Одновременно в строме миокарда увеличивается количество капилляров и аргирофильных волокон, увеличивается количество и размеры ультраструктур каждой клетки. Если устранена причина исход рабочей гипертрофии благоприятный. В противном случае происходит декомпенсация гипертрофированного органа с развитием в нем дистрофических, некротических и склеротических процессов. 2. Викарная или заместительная гипертрофия, которая развивается в парных органах при удалении одного из них, или при удалении части органа, например, в печени и легких. 3. Гормональная (нейрогуморальная) или коррелятивная гипертрофия. Примером такой гипертрофии в физиологических условиях может явиться увеличение матки при беременности. В условиях патологии такая гипертрофия возникает при нарушении функции эндокринных желез. Примером является акромегалия, возникающая при опухолях передней доли гипофиза, железистая гиперплазия эндометрия при дисфункции яичников. 4. Гипертрофические разрастания, которые чаще возникают при воспалении в виде гиперпластических полипов, кондилом, или же при нарушении лимфообращения и застое лимфы в нижних конечностях, что приводит к развитию слоновости вследствие разрастания соединительной ткани. 5. Кроме того, выделяют патологическую гипертрофию, когда увеличение органа происходит при отсутствии соответствующего стимула. Примерами такой гипертрофии являются гипертрофические варианты циррозов печени, дилятационные и констриктивные формы кардиомиопатии. В патологии существует понятие ложной гипертрофии, когда орган уве-личен в размерах за счет не паренхиматозных элементов. Примером такой ложной гипертрофии является простое ожирение сердца, когда размеры этого органа увеличиваются за счет разрастания жировой клетчатки. Противоположным гипертрофии процессом является атрофия.
АТРОФІЯ (atrophia; грец. a — не, заперечення + trophе — живлення) — процес, який характеризується зменшенням об’єму і розмірів, а також вираженими тією чи іншою мірою якісними змінами клітин, тканин і органів. Однак явища А. не завжди належать до патологічних. Деякі органи в певному віці піддаються атрофічним змінам у зв’язку з віковим ослабленням їх функцій. 1 Така фізіологічна А. (вікова інволюція) спостерігається, напр. у щитовидній залозі, яєчниках і молочних залозах. При старечій А., як фізіологічному явищі, виявляють стоншення і втрату еластичності шкіри, розрідження губчатої і стоншення компактної речовини кісток (остеопороз), зменшення розмірів внутрішніх органів і головного мозку, що супроводжується зменшенням товщини мозкових звивин. 2 Патологічна А. відрізняється від фізіологічної як причинами виникнення, так і деякими якісними особливостями. Основою А. є перевага процесів дисиміляції над процесами асиміляції у зв’язку зі зниженням активності цитоплазматичних ферментів. Залежно від причини, що викликає А., розрізняють: нейротичну А.; функціональну А.; гормональну А.; А. внаслідок недостатнього харчування; А. в результаті впливу фізичних, хімічних і механічних чинників. 3 Нейротична А. розвивається при травматичному або запальному руйнуванні нервових провідників між органом і нервовою системою, а також при руйнуванні нервових клітин. 4 Функціональна А. розвивається внаслідок зниження діяльності органа і позначається як А. від бездіяльності. Гормональна А. розвивається внаслідок порушення діяльності залоз внутрішньої секреції. До цієї групи А. належать: гіпофізарна кахексія (розвивається у зв’язку з недостатністю функцій гіпофіза) і тиреопривна кахексія (виникає при зниженні функції щитовидної залози). А. внаслідок недостатнього харчування може бути загальною і місцевою. 5 Загальна А., або кахексія, розвивається при недостатньому чи неповноцінному харчуванні, а також внаслідок глибокого порушення обміну речовин. Кахексія спостерігається при тяжких, виснажувальних хворобах (туберкульоз, злоякісні новоутворення, хвороби органів травлення, голодування, хронічні інтоксикації, хвороби ендокринної системи) і виражається наростаючим загальним схудненням і А. внутрішніх органів та м’язів. 6 Місцева А. внаслідок недостатнього харчування виникає через звуження просвіту артерій. Так, атеросклероз мозкових судин призводить до А. тканини головного мозку, атеросклероз судин нирок — до їх А. та зморщування. А. в результаті дії фізичних чинників виникає при впливі на організм променевої енергії, що викликає особливо сильні атрофічні зміни в шкірі, лімфатичних вузлах, яєчках і яєчниках. До А. внаслідок дії хімічних чинників належать атрофічні зміни в щитовидній залозі, викликані застосуванням йоду. До А. внаслідок впливу механічних чинників слід віднести А. від тиску. Вона спостерігається у випадках, коли будь-яка тканина виявляється під впливом стискальної сили, напр. у кістці при здавленні її пухлинним вузлом або аневризматичним мішком. У зв’язку з тим, що А. розвивається поступово, деякі її види можна розпізнати і попередити на ранній фазі розвитку. У разі своєчасного усунення причини, яка зумовила А., відбувається вилікування з відновленням структури та функції атрофованого органа.
Дистрофія (Від грец. Dys - порушення і trophe - маю) - складний патологічний процес, в основі якого лежить порушення тканинного (клітинного) метаболізму, що веде доструктурним змінам. Тому дистрофії розглядаються як один з видів ушкодження. Під трофікою розуміють сукупність механізмів, що визначають метаболізм і структурну організацію тканини (клітини), які необхідні для відправленняспеціалізованої функції. Серед цих механізмів виділяють клітинні і позаклітинні. Клітинні механізми забезпечуються структурною організацією клітини і її ауторегуляцією. Це означає, що трофіка клітини в значній мірі є властивістю самої клітини як складноїсаморегульованої системи. Життєдіяльність клітини забезпечується «навколишнім середовищем» і регулюється за допомогою ряду систем організму. Тому позаклітинні механізми трофіки розташовують транспортними (кров, лімфа, мікроциркуляторне русло) і інтегративними(Нейро-ендокринні, неірогуморальние) системами її регулювання. Зі сказаного випливає, що безпосередньою причиною розвитку дистрофій можуть служити порушення як клітинних, так і позаклітинних механізмів, що забезпечують трофіку. асстройстваауторегуляції клітини можуть бути викликані різними факторами (гіперфункція, токсичні речовини, радіація, спадкова недостатність або відсутність ферменту і т. д.). Велику роль надають рецепторам, які здійснюють «координоване гальмування» функційрізних ультраструктур. Порушення ауторегуляции клітини веде до енергетичного її дефіциту і до порушення ферментативних процесів в клітині. Ферментопатія, або ензимопатія (придбана або спадкова), стає основним патогенетичним ланкою і виразомдистрофії при порушеннях клітинних механізмів трофіки. Порушення функції транспортних систем, що забезпечують метаболізм і структурну цілість тканин (клітин), викликають гіпоксію, яка є провідною в патогенезі дисциркуляторних дистрофій. Прирозладах ендокринної регуляції трофіки (тиреотоксикоз, діабет, гіперпаратиреоз і т. д.) можна говорити про ендокринних, а при порушенні нервової регуляції трофіки (порушена іннервація, пухлина головного мозку і т. д.) - про нервові або церебральних дистрофіях. Особливості патогенезу внутрішньоутробних дистрофій визначаються безпосереднім зв'язком їх з хворобами матері. В результаті при загибелі частини зачатка органу або тканини може розвинутися незворотний порок розвитку. При дистрофіях в клітці і. (Або) міжклітинномуречовині накопичуються різні продукти обміну (білки, жири, вуглеводи, мінерали, вода), які характеризуються кількісними або якісними змінами в результаті порушення ферментативних процесів. Морфогенез. Серед механізмів,які призводять до розвитку характерних для дистрофій змін, розрізняють інфільтрацію, декомпозицію (фанероз), збочений синтез і трансформацію. Інфільтрація - надлишкове проникнення продуктів обміну з крові і лімфи в клітини або міжклітинну речовину зподальшим їх накопиченням у зв'язку з недостатністю ферментних систем, метаболізуючих ці продукти. Такі, наприклад, інфільтрація Грубодисперсні білком епітелію проксимальних канальців нирок при нефротичному синдромі, інфільтрація холестерином іліпопротеїдами інтими аорти та великих артерій при атеросклерозі. Декомпозиція (фанероз) - розпад ультраструктур клітин і міжклітинної речовини, що веде до порушення тканинного (клітинного) метаболізму і накопичення продуктів порушеного обміну в тканині(Клітині). Такі жирова дистрофія кардіоміоцитів при дифтерійної інтоксикації, фібриноїдне набухання сполучної тканини при ревматичних хворобах. Збочений синтез - це синтез в клітинах або в тканинах речовин, які не зустрічаються в них в нормі. До нихвідносяться: синтез аномального білка амілоїду в клітині і аномальних білково-полісахаридних комплексів амілоїду в міжклітинній речовині; синтез білка алкогольного гіаліну гепатоцитами; синтез глікогену в епітелії вузького сегмента нефрона при цукровому діабеті. Трансформація - освіта продуктів одного виду обміну із загальних вихідних продуктів, які йдуть на побудову білків, жирів і вуглеводів. Така, наприклад, трансформація компонентів жирів і вуглеводів в білки, посилена полімеризація глюкози в глікоген та ін Інфільтрація і декомпозиція - провідні морфогенетичні механізми дистрофій - часто є послідовними стадіями в їхньому розвитку. Проте в деяких органах і тканинах у зв'язку зі структурно-функціональними особливостями їх переважає якийсь один з морфогенетичних механізмів (інфільтрація - в епітелії ниркових канальців, декомпозиція - в клітинах міокарда), що дозволяє говорити про ортолога (від грец. Orthos - прямий, типовий) дистрофій. Морфологічна специфіка. При вивченні дистрофій на різних рівнях - ультраструктурному, клітинному, тканинному, органному - морфологічна специфіка проявляється неоднозначно. Ультраструктурна морфологія дистрофій зазвичай не має будь-якої специфіки. Вона відображає не тільки пошкодження органел, а й їх репарацію (внутрішньоклітинна регенерація). Разом з тим можливість виявлення в органелах ряду продуктів обміну (ліпіди, глікоген, феритин) дозволяє говорити про ультраструктурних змін, характерних для того чи іншого виду дистрофій. Характерна морфологія дистрофій виявляється, як правило, на тканинному і клітинному рівнях, причому для доказу зв'язку дистрофії з порушеннями того чи іншого виду обміну потрібне застосування гістохімічних методів. Без встановлення якості продукту порушеного обміну не можна верифікувати тканинну дистрофію, тобто віднести її до білкових, жирових, вуглеводних або інших дистрофій. Зміни органа при дистрофії (розмір, колір, консистенція, структура на розрізі) в одних випадках представлені винятково яскраво, в інших - відсутні, і лише мікроскопічне дослідження дозволяє виявити їх специфічність. У ряді випадків можна говорити про системний характер змін при дистрофії (системний гемосидероз, системний мезенхімальних амілоїдоз, системний ліпоїдоз). У класифікації дистрофій дотримуються кількох принципів. Виділяють дистрофії: В залежності від переважання морфологічних змін у спеціалізованих елементах паренхіми або стромі і судинах: паренхіматозні; стромально-судинні; змішані. За домінуванням порушень того чи іншого виду обміну: білкові; жирові; вуглеводні; мінеральні. В залежності від впливу генетичних факторів: придбані; спадкові. За поширеністю процесу: загальні; місцеві.
3. В якому продукті, що отримують з коноплі найбільший вміст тетрагідроканабінолу? Гашишне масло
4 Валеологічні індекси та показники.
5 Види м’язових скорочень Механізм скорочення м'язових тканин У молекулярному механізмі скорочення м'язових тканин виділяють 2 процеси. Один з них кальций-залежний, інший - АТФ-залежний. У поперечносмугастих і гладеньких м'язах кальций-залежний процес здійснюється по-різному, а АТФ-залежний - однаково. Кальций-залежний ПрОЦесс скорочення в посмугованому м'язі. Скорочення м'язового волокна (або кардіоміоциту) відбувається тільки у тому випадку, коли на актині відкриваються ділянки для скріплення міозину, внаслідок чого міозин з'єднується з актином. При цьому етапність ініціації скорочення відбувається в наступній послідовності: скоротливий стимул (нервовий імпульс) проходить по сарколемі і поступає на мембрани Т-трубочок, що стимулює утворення з ліпідів мембран Т-трубочок инозитол-фосфатів, які взаємодіють з рецепторами на мембранах АЕС, що ініціює відкриття кальцієвих каналів в її мембранах. Вихід кальцію з АЕС в цитозоль (у спокої концентрація кальцію в цитозолі 10-7-10-8 ммоль/л, при скороченні - 10-5) і його дифузія до міофібріл завершується утворенням комплексного з'єднання кальцію з тропоніном С, внаслідок чого на актині відкриваються місця для скріплення міозину, який з'єднується з актином і відбувається скорочення. Кальций-залежний процес скорочення в гладкому м'язі. Скорочення міоциту відбувається унаслідок фосфорилування легкого ланцюга міозину, тільки в цьому випадку головка міозину може зв'язувати і розщеплювати АТФ і взаємодіяти з актином. Надходження скоротливого стимулу (нервовий імпульс, гормон) ініціює відкриття кальцієвих каналів в цитомембрані міоциту, АЕС і мітохондріях. Поступаючий через ці канали кальцій з'єднується з кальмодуліном. Комплекс кальций-кальмодулін, що утворюється, активує кіназу легких ланцюгів міозину, яка фосфорилює легкі ланцюги його головок, внаслідок чого вони придбавають здатність зв'язувати і розщеплювати АТФ і з'єднуватися з актином. АТФ-залежний процес скорочення Головка міозину приєднує молекулу АТФ і розщеплює її до АДФ і фосфату, унаслідок чого головка міозину приєднується до актина. Одночасно з цим від головки міозину від'єднуються АДФ і фосфат. Саме у цей момент головка міозину робить гребковий рух і молекула міозину просувається уздовж молекули актина (іншими словами - молекула міозину тягне на себе актин) (див. мал. 13). Вслід за цим головка міозину приєднує нову молекулу АТФ і лише після цього від'єднується від актина і придбаває первинне положення. Таким чином, без АТФ м'язи не можуть ні скоротитися, ні розслабитися. В процесі скорочення м'язових тканин важливу роль виконує гладенька ендоплазматична сітка (АЕС). У структурних одиницях м'язових тканин (особливо в поперечносмугастій) дуже добре розвинена АЕС, що є сховищем іонів кальцію. У її мембрані є кальцієві канали, по яких кальцій виходить з порожнини АЕС і входить назад. Вихід іонів кальцію з плості АЕС в цитозоль здійснюється пасивно, оскільки їх концентрація в цитозолі набагато нижча, ніж в порожнині АЕС, а надходження назад в порожнину є активним транспортом з витратою енергії АТФ. Скорочення поперечносмугастих м'язів В процесі скорочення поперечносмугастих м'язів довжина актинових і міозинових філаментів не змінюється, а відбувається їх зсув щодо один одного: міозинові філаменти всовуються в простори між актиновими, а актинові - між міозиновими; в результаті цього: ширина I-диска і H-смужки А-диска зменшується, в той же час ширина диска А не змінюється, а довжина саркомера коротшає (див. мал. 12). У структурних одиницях поперечносмугастих м'язових тканин АЕС обплітає кожну міофібрілу і близько підходить до Т-трубочок. Сигналом для виходу кальцію з канальців АЕС є спеціальні регуляторні речовини - ліпідні медіатори - інозітол-3-фосфат і інозітол-4-фосфат, які синтезуються в мембранах Т-трубочок тільки у момент проходження по них скоротливого імпульсу. Оскільки канальці АЕС близько підходять до Т-трубочок, инозитол-фосфати швидко досягають АЕС і взаємодіють із специфічними рецепторами для инозитол-фосфатів, що знаходяться на її мембранах. Це приводить до відкриття кальцієвих каналів в мембранах АЕС і швидкий вихід іонів кальцію з порожнини канальців в цитозоль, що і ініціюють скорочення. Скорочення гладеньких м'язів На відміну від поперечносмугастих м'язів, в яких міофібріли існують постійно, в гладеньких м'язах вони утворюються тільки у момент скорочення, яке відбувається унаслідок надходження сигналу від нервових клітин. Під впливом медіатора в плазмолемі міоцитів утворюються кавеоли, в які шляхом ендоцитоза поступають іони кальцію, що викликають полімеризацію міозину і його взаємодію з актиновими філаментами. Актинові філаменти одним своїм кінцем за допомогою зшиваючих білків прикріпляються до спеціальних областей внутрішньої поверхні плазмолеми, а іншим - до міозину. Міозинові філаменти прикріпляються до спеціальних місць в цитозолі клітини (нексуси). Зсув актинових філаментів щодо міозинових приводить до укорочення клітини. Після припинення надходження сигналу кальцій покидає кавеоли, міозин деполімерізується, міофібріли розпадаються і клітина розслабляється (мал. 14).
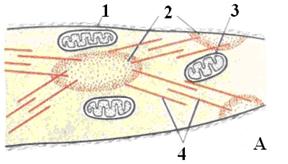
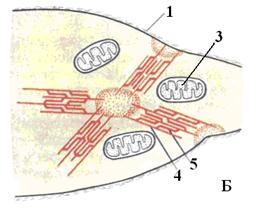
Мал. 14. Схема будови міоциту гладенької м'язової тканини в розслабленому стані (А) і при скороченні (Б). 1 - цитолема: 2 - щільні тільця; 3 - мітохондрії; 4 - актинові філаменти; 5 - міозинові філаменти. Типи скелетних м'язових волокон °- фазні - у відповідь на нервовий імпульс швидко скорочуються; локалізація - майже вся скелетна мускулатура; °- тонічні - скорочення викликається лише множинними (повторними) нервовими імпульсами; локалізація - зовнішні вушні і зовнішні очні м'язи; °- червоні - містять багато міоглобіну, багато мітохондрій, висока активність окислювальних ферментів; поволі стомлюються, а по швидкості скорочення можуть бути як швидкими, так і повільними. Такий тип м'язів переважаючим є у пернатих і ссавців дикої фауни; °- білі - мають мало міоглобіну, мало мітохондрій, низька активність окислювальних ферментів, висока активність гліколітичних ферментів; мають високу швидкість скорочення, але швидко стомлюються; °- швидкі - мають високу швидкість скорочення, у них висока швидкість розщеплювання АТФ; °- повільні - скорочуються поволі, низька швидкість розщеплювання АТФ. Швидкість скорочення залежить від типу міозину в м'язі. Розрізняють швидкий і повільний міозин. У одному м'язі присутні волокна як з швидким, так і з повільним міозином, і від їх співвідношення залежить швидкість скорочення м'яза в цілому.
