
- •4. Биологические функции белков. Роль пространственной организации полипептидной цепи в образовании активных центров. Взаимодействие белков с лигандами. Денатурация белков.
- •5. Строение и биологическая роль нуклеотидов.
- •6. Первичная и вторичная структуры днк. Правила Чаргаффа. Принцип комплементарности. Типы связей в молекуле днк. Биологическая роль днк. Молекулярные болезни - следствие генных мутаций.
- •7. Первичная и вторичная структуры рнк. Типы рнк: особенности строения. Основные компоненты белоксинтезирующей системы. Функция рибосом. Адапторная функция тРнк и роль мРнк в синтезе белка.
- •8. Биосинтез днк (репликация) и мРнк (транскрипция). Процессы "созревания" первичного транскрипта при образовании мРнк.
- •11. Роль ферментов в метаболизме. Наследственные энзимопатии в раннем детском возрасте.Многообразие ферментов. Специфичность действия ферментов. Классификация ферментов. Изоферменты, мультиферменты.
- •12. Свойства ферментов. Зависимость скорости ферментативной реакции от концентрации фермента и субстрата, температуры и рН среды.
- •14. Основные механизмы регуляции действия ферментов и их роль в регуляции метаболизма. Проферменты.
- •23. Молоко как продукт питания. Основные компоненты женского и коровьего молока. Преимущества грудного вскармливания детей.
- •24. Неорганические метаболиты: натрий, калий, медь, цинк, магний, фтор, йод, селен, сульфат, роль в организме.
- •26. Жирорастворимые витамины а, е и к – биологическая роль, пищевые источники, причины и проявления гипо- и гипервитаминоза.
- •27. Витамин d. Образование активной формы витамина из провитамина. Биологическая роль. Нарушения обмена при недостаточности витамина d3 у детей.
- •28. Витамин b1 — коферментные функции, биологическая роль, суточная потребность, пищевые источники, строение, нарушения обмена при недостаточности тиамина.
- •29. Витамин b2 — коферментные функции, биологическая роль, суточная потребность, пищевые источники, строение.
- •30. Витамин рр — коферментные функции, биологическая роль, суточная потребность, пищевые источники, строение.
- •31. Витамин b6 —коферментные функции, биологическая роль, пищевые источники, строение. Потребность в витамине b6 в зависимости от качественного состава пищевого рациона.
- •33. Витамин b12 – биологическая роль, суточная потребность, источники. Причины недостаточности витаминаB12 в организме и ее проявления. Роль "внутреннего фактора Касла" в усвоении витамина b12.
- •34. Витамин с – биологическая роль, суточная потребность, пищевые источники, строение, нарушения обмена при недостаточности аскорбиновой кислоты.
- •35. Безопасность пищи. Химические и биологические загрязнители, их влияние на обмен веществ. Метаболизм этанола.
- •38. Ацетил-КоА: источники и основные пути использования в тканях. Компартментализация обмена ацетил-КоА.
- •39. Цикл трикарбоновых кислот: последовательность реакций, характеристика ферментов. Амфиболическая функция цитратного цикла. Связь с обменом углеводов, жиров и белков.
- •42. Образование и пути использования глюкозо-6-фосфата в организме. Особенности обмена глюкозо-6-фосфата в различных тканях, обусловленные функциональными различиями этих тканей.
- •44. Дихотомический аэробный распад глюкозы: схема последовательности реакций, значение. Энергетический баланс аэробного окисления глюкозы.
- •45. Пентозофосфатный путь превращений глюкозы. Реакции окислительного этапа. Роль пентозофосфатного пути в различных тканях.
- •48. Принципы построения биологических мембран. Роль основных компонентов (липидов, белков, углеводов) в структурной организации и функционировании мембран.
- •49. Липиды-амфипаты: представители, способность к агрегации, образованию мицелл, бислоев. Полярные липиды как компоненты биомембран и липопротеинов.
- •9.5.3. Перенос через мембраны частиц и высокомолекулярных соединений
- •51. Окисление высших жирных кислот. Последовательность реакций b-окисления. Связь окисления жирных кислот с цитратным циклом и дыхательной цепью. Биологическая роль.
- •52. Биосинтез жирных кислот в тканях: последовательность реакций, биологическая роль. Компартментализация и регуляция обмена жирных кислот.
- •53. Биосинтез ацилглицеролов и фосфолипидов: последовательность реакций, значение. Липотропный эффект фосфолипидов, роль в предупреждении жирового перерождения печени.
- •54. Биосинтез и использование кетоновых тел. Гиперкетонемия: причины механизм развития и последствия.
- •55. Обмен и функции холестерола. Нарушения обмена холестерола.
- •1) Инициация: образование свободного радикала (l•)
- •2) Развитие цепи:
- •3) Разрушение структуры липидов
- •58. Непрямое дезаминирование аминокислот. Роль глутаматдегидрогеназы и глутаминовой кислоты. Реакции трансаминирования, ферменты, биологическое значение.
- •59. Декарбоксилирование аминокислот. Образование биогенных аминов — гистамина, серотонина, гамк. Роль биогенных аминов в регуляции метаболизма и функций. Распад биогенных аминов.
- •60. Источники образования аммиака и пути его обезвреживания в организме. Связывание аммиака в местах образования и транспорт в печень. Особенности детоксикации аммиака у детей первого года жизни.
- •61. Биосинтез мочевины. Связь орнитинового цикла с превращениями фумаровой и аспарагиновой кислот. Причины гипераммониемии. Уремия как следствие нарушения выведения мочевины из организма.
- •62. Обмен глутамата и аспартата, роль в азотистом обмене, распад до конечных продуктов.
- •63. Роль серина и глицина в образовании одноуглеродных групп и их использование в биологических синтезах. Участие тгфк в этих процессах.
- •64. Метионин и s-аденозилметионин: строение, участие в процессах трансметилирования. Регенерация s-аденозилметионина из гомоцистеина..
- •67. Обмен железа. Суточная потребность, источники, всасывание, транспорт, депонирование, использование в организме, реутилизация железа.
- •69. Регуляция метаболизма. Иерархия регуляторных систем. Значение эндокринной системы. Роль гормонов гипоталамуса и гипофиза.
- •70. Механизм действия дистантных гормонов. Роль мембраносвязанных ферментов в передаче внешнего сигнала внутрь клетки.
- •71. Циклический аденозинмонофосфат – строение, синтез, распад, роль в клетке. Факторы, влияющие на синтез и распад циклического аденозинмонофосфата.
- •72. Гормоны передней доли гипофиза - строение, механизм действия, биологическая роль. Последствия нарушений функции гипофиза в разные возрастные периоды.
- •73. Гормоны задней доли гипофиза: вазопрессин и окситоцин. Строение, механизм действия, биологическая роль. Последствия нарушения продукции вазопрессина.
- •74. Инсулин - строение, образование из проинсулина, регуляция секреции инсулина, взаимодействие инсулина с рецептором.
- •75. Изменения активности внутриклеточных ферментов под действием инсулина, влияние инсулина на обмен веществ.
- •76. Глюкагон - строение, факторы, влияющие на секрецию, механизм действия и биологическая роль
- •77. Биохимические изменения при сахарном диабете. Метаболические механизмы развития осложнений при сахарном диабете. Последствия длительной гипергликемии. Особенности сахарного диабета у детей.
- •1. Инсулинзависимый сахарный диабет
- •2. Инсулинонезависимый сахарный диабет
- •1. Симптомы сахарного диабета
- •2. Острые осложнения сахарного диабета. Механизмы развития диабетической комы
- •3. Поздние осложнения сахарного диабета
- •78. Адреналин - механизм действия и биологическая роль, строение, реакции образования адреналина из тирозина.
- •79. Глюкокортикоиды – образование, механизм действия, биологическая роль, строение. Метаболические изменения при избытке глюкокортикоидов.
- •80. Минералокортикоиды – механизм действия, биологическая роль, строение. Метаболические изменения при избытке и недостатке минералокортикоидов.
- •81. Иодтиронины - строение, синтез, механизм действия, биологическая роль. Гипо- и гипертиреозы.
- •82. Паратгормон и кальцитонин, строение, механизм действия, биологическая роль. Гипер- и гипопаратиреозы.
- •29.4.3. Нарушения гормональной функции паращитовидных желёз.
- •83. Ренин-ангиотензиновая система, роль в регуляции водно-электролитного обмена.
- •84. Половые гормоны - механизм действия, биологическая роль, образование, строение,
- •85. Нарушения функций эндокринных желез: гипер- и гипопродукция гормонов. Примеры заболеваний, связанных с дисфункцией эндокринных желез.
- •87. Низкомолекулярные азотсодержащие вещества крови ("остаточный азот'') и диагностическое значение их определения. Гиперазотемия (ретенционная и продукционная).
- •88. Буферные системы крови и кислотно-основное состояние (кос). Роль дыхательной и выделительной систем в поддержании кос. Нарушения кислотно-основного баланса. Особенности регуляции кос у детей.
- •90. Характеристика основных факторов гемокоагуляции. Свертывание крови как каскад реакций активации проферментов путем протеолиза. Биологическая роль витамина к. Гемофилии.
- •91. Роль печени в углеводном обмене. Источники глюкозы крови и пути метаболизма глюкозы в печени. Уровень глюкозы в крови в раннем детском возрасте.
- •92. Роль печени в обмене липидов.
- •93. Роль печени в азотистом обмене. Пути использования фонда аминокислот в печени. Особенности в детском возрасте.
- •94. Компартментализация метаболических процессов в печени. Регуляция направления потока метаболитов через мембраны внутриклеточных (субклеточных) структур. Значение в интеграции обмена веществ.
- •5. Фазы метаболизма ксенобиотиков.
- •97. Роль почек в поддержании гомеостаза организма. Механизмы ультрафильтрации, канальцевой реабсорбции и секреции. Гормоны, влияющие на диурез. Физиологическая протеинурия и креатинурия у детей.
- •34.2. Механизмы процессов ультрафильтрации, канальцевой реабсорбции и секреции в почках.
- •34.3. Гормональные механизмы регуляции почечной функции
- •98. Важнейшие биополимеры соединительной ткани и межклеточного матрикса (коллаген, эластин, протеогликаны), состав, пространственная структура, биосинтез, функции.
- •99. Особенности обмена в скелетных мышцах и миокарде: характеристика основных белков, молекулярные механизмы мышечного сокращения, энергетическое обеспечение мышечного сокращения.
- •100. Особенности обмена в нервной ткани. Биологически активные молекулы нервной ткани.
- •102. Диагностическое значение определения метаболитов в крови и моче.
1. Первичная структура белка. Зависимость свойств и конформации белков от первичной структуры. Примеры полиморфизма белков, гемоглобин А и F, структурные и функциональные отличия. Роль фетального гемоглобина в период внутриутробного развития плода. Наследственные изменения первичной структуры — молекулярные болезни (серповидно-клеточная анемия).
Первичной структурой белка называют последовательность чередования аминокислот в полипептидной цепи. Эту структуру формируют пептидные связи между α-амино- и α-карбоксильными группами аминокислот (см. 1.4.2). Имейте в виду, что даже небольшие изменения первичной структуры белка могут значительно изменять его свойства. Примером заболеваний, развивающихся в результате изменения первичной структуры белка, являются гемоглобинопатии (гемоглобинозы) .
В эритроцитах здоровых взрослых людей присутствует гемоглобин А (Hb А) . В крови некоторых людей содержится аномальный (изменённый) гемоглобин - гемоглобин (Hb S). Единственное отличие первичной структуры Hb S от Hb A - замена гидрофильного остатка глутаминовой кислоты на гидрофобный остаток валина в концевом участке их β-цепей.
Как известно, основная функция гемоглобина -транспорт кислорода к тканям. В условиях пониженного парциального давления О2 снижается растворимость гемоглобина S в воде и его способность связывать и переносить кислород. Эритроциты принимают при этом серповидную форму, быстро разрушаются, вследствие чего развивается малокровие (серповидно-клеточная анемия] .
Установлено, что последовательность аминокислотных остатков полипептидной цепи белка несёт в себе информацию, необходимую для формирования пространственной структуры белка. Установлено, что каждой полипептидной последовательности соответствует только один стабильный вариант пространственной структуры. Процесс сворачивания полипептидной цепи в правильную трёхмерную структуру получил название фолдинг.
До последнего времени считалось, что формирование пространственной структуры белка происходит самопроизвольно, без участия каких-либо компонентов. Однако сравнительно недавно обнаружилось, что это справедливо только для сравнительно небольших белков (порядка 100 аминокислотных остатков). В процессе фолдинга более крупных белков принимают участие специальные протеины - шапероны, которые создают возможность быстрого формирования правильной пространственной структуры белка.
Примером полиморфизма белков является гемоглобин, имеющий множество форм. Гемоглоби́н A— нормальный гемоглобин взрослого человека. Этот белок представляет собой тетрамер, состоящий из двух пар полипептидных цепей — мономеров: двух мономеров α-цепей и двух мономеров β-цепей, или двух мономеров α и двух мономеров δ. Гемоглоби́н F— фетальный, плодный тип гемоглобина человека. Гемоглобин F — это белок-гетеротетрамер из двух α-цепей и двух γ-цепей глобина. Гемоглобин F обладает повышенным сродством к кислороду(в нём серин вместо лизина) и позволяет сравнительно малому объёму крови плода выполнять кислородоснабжающие функции более эффективно. Однако гемоглобин F обладает меньшей стойкостью к разрушению и меньшей стабильностью. В течение последнего триместра беременности и после рождения гемоглобин F постепенно — замещается «взрослым» гемоглобином А (HbA), менее активным транспортёром кислорода, но более стойким к разрушению и более стабильным. Молекулярные болезни – наследственные нарушения в первичной структуре булка. Например, замена в β-субъединице гемоглобина шестой глутаминовой аминокислоты на валин приводит к образованию гемоглобина S и тому, что молекула гемоглобина в целом не может выполнять свою основную функцию — транспорт кислорода; в таких случаях у человека развивается заболевание — серповидноклеточная анемия.
2. Конформация белковой молекулы (вторичная и третичная структуры). Типы внутримолекулярных связей в белках. Фибриллярные и глобулярные белки (примеры). Четвертичная структура белка. Примеры строения и функционирования олигомерных белков.
Вторичная структура белка представляет собой способ свёртывания полипептидной цепи в спиральную или иную конформацию. При этом образуются водородные связи между СО-и NH-группами пептидного остова одной цепи или смежных полипептидных цепей. Известно несколько типов вторичной структуры пептидных цепей, среди которых главными являются α-спираль и β-складчатый слой.
α-Спираль - жёсткая структура, имеет вид стержня. Внутреннюю часть этого стержня создаёт туго закрученный пептидный остов, радикалы аминокислот направлены наружу. При этом СО-группа каждого аминокислотного остатка взаимодействует с NH-группой четвёртого от него остатка. На один виток спирали приходится 3,6 аминокислотных остатка, а шаг спирали составляет 0,54 нм (рисунок 2.1).

Рисунок 2.1. α-Спираль.
Некоторые аминокислоты препятствуют свёртыванию цепи в α-спираль, и в месте их расположения непрерывность спирали нарушается. К этим аминокислотам относятся пролин (в нём атом азота входит в состав жёсткой кольцевой структуры и вращение вокруг связи N - Сα становится невозможным) , а также аминокислоты с заряженными радикалами, которые электростатически или механически препятствуют формированию α-спирали. Если в пределах одного витка (примерно 4 аминокислотных остатка) находятся два таких радикала (или более), они взаимодействуют и деформируют спираль.
β-Складчатый слой отличается от α-спирали тем, что имеет плоскую, а не стержневидную форму. Образуется при помощи водородных связей в пределах одной или нескольких полипептидных цепей. Пептидные цепи могут быть расположены в одном направлении (параллельно) или в противоположных направлениях (антипараллельно) , напоминая меха аккордеона. Боковые радикалы находятся выше и ниже плоскости слоя.

Рисунок 2.2. β-Складчатый слой.
Обратите внимание на то, что тип вторичной структуры белка определяется его первичной структурой. Например, в месте расположения остатка пролина (атомы пирролидинового кольца в пролине лежат в одной плоскости) пептидная цепь делает изгиб, и водородные связи между аминокислотами не образуются. Поэтому белки с высоким содержанием пролина (например, коллаген) не способны образовывать а-спираль. Радикалы аминокислот, несущие электрический заряд, также препятствуют спирализации.
2.1.3. Третичная структура белка - это распределение в пространстве всех атомов белковой молекулы, или иначе говоря, пространственная упаковка спирализованной полипептидной цепи. Основную роль в образовании третичной структуры белка играют водородные, ионные, гидрофобные и дисульфидные связи, которые образуются в результате взаимодействия между радикалами аминокислот.
Водородные связи образуются между двумя полярными незаряженными радикалами или между незаряженным и заряженным радикалами, например, радикалами серина и глутамина:

Ионные связи могут возникать между противоположно заряженными радикаламинапример, радикалами глутамата и аргинина:
Гидрофобные взаимодействия характерны для неполярных радикалов, например, валина и лейцина:
Дисульфидные связи образуются между SH-группами двух радикалов цистеина, находящихся в разных участках полипептидной цепи: .
По форме молекулы и особенностям формирования третичной структуры белки делят на глобулярные и фибриллярные.
Глобулярные белки - имеют сферическую или эллипсовидную форму молекулы (глобула). В процессе образования глобулы гидрофобные радикалы аминокислот погружаются во внутренние области, гидрофильные радикалы располагаются на поверхности молекулы. При взаимодействии с водной фазой полярные радикалы образуют многочисленные водородные связи. Белки удерживаются в растворённом состояния за счёт заряда и гидратной оболочки. В организме глобулярные белки выполняют динамические функции (транспортную, ферментативную, регуляторную, защитную). К глобулярным белкам относятся:
Альбумин - белок плазмы крови; содержит много остатков глутамата и аспартата; осаждается при 100%-ном насыщении раствора сульфатом аммония.
Глобулины - белки плазмы крови; по сравнению с альбумином оббладают большей молекулярной массой и содержат меньше остатков глутамата и аспартата, осаждаются при 50%-ном насыщении раствора сульфатом аммония.
Гистоны - входят в состав ядер клеток, где образуют комплекс с ДНК. Содержат много остатков аргинина и лизина.
Фибриллярные белки - имеют нитевидную форму (фибриллы) , образуют волокна и пучки волокон. Между соседними полипептидными цепями имеется много поперечных ковалентных сшивок. Нерастворимы в воде. Переходу в раствор препятствуют неполярные радикалы аминокислот и сшивки между пептидными цепями. В организме выполняют главным образом структурную функцию, обеспечивают механическую прочность тканей. К фибриллярным белкам относятся:
Коллаген - белок соединительной ткани. В его составе преобладают аминокислоты глицин, пролин, гидроксипролин.
Эластин - более эластичен, чем коллаген, входит в состав стенок артерий, лёгочной ткани, в его составе преобладают аминокислоты глицин, аланин, валин.
Кератин - белок эпидермиса и производных кожи, в его структуре преобладает аминокислота цистеин.
3. Гемоглобин - аллостерический белок. Конформационные изменения молекулы гемоглобина. Кооперативный эффект. Регуляторы сродства гемоглобина к кислороду. Структурные и функциональные различия миоглобина и гемоглобина.
К гемопротеинам относятся: гемоглобин, миоглобин, цитохромы, пероксидаза, каталаза. Эти белки содержат в качестве простетической группой гем.
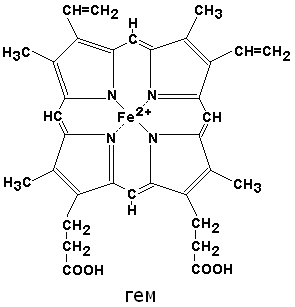
По своему химическому строению гем представляет собой протопорфирин IX, связанный с двухвалентным железом. Протопорфирин IX - органическое соединение, относящееся к классу порфиринов. Протопорфирин IX содержит четыре замещённых пиррольных кольца, соединённых метиновыми мостиками =СН—. Заместителями в пиррольных кольцах являются: четыре метильные группы СН3—, две винильные группы СН2=СН— и два остатка пропионовой кислоты — СН2—СН2—СООН. Гем соединяется с белковой частью следующим образом. Неполярные группы . протопорфирина IX взаимодействуют с гидрофобными участками аминокислот при помощи гидрофобных связей. Кроме того, имеется координационная связь между атомом железа и имидазольным радикалом гистидина в белковой цепи. Ещё одна координационная связь атома железа может использоваться для связывания кислорода и других лигандов.
Присутствие в биологическом материале гемсодержащих белков обнаруживается при помощи бензидиновой пробы (при добавлении бензидина и пероксида водорода исследуемый раствор окрашивается в сине-зелёный цвет).
равните структуру и функцию миоглобина и гемоглобина, запомните характерные особенности каждого из этих белков.
Миоглобин - хромопротеин, присутствующий в мышечной ткани и обладающий большим сродством к кислороду. Молекулярная масса этого белка около 16000 Да, Молекула миоглобина имеет третичную структуру и представляет собой одну полипептидную цепь, соединённую с гемом. Миоглобин не обладает аллостерическими свойствами (см. 2.4.), кривая насыщения его кислородом имеет вид гиперболы (рисунок 4). Функция миоглобина заключается в создании в мышцах кислородного резерва, который расходуется по мере необходимости, восполняя временную нехватку кислорода.
Гемоглобин (Hb) - хромопротеин, присутствующий в эритроцитах и участвующий в транспорте кислорода к тканям. Гемоглобин взрослых людей называется гемоглобином А (Hb A). Молекулярная масса его составляет около 65000 Да. Молекула Hb А имеет четвертичную структуру и включает четыре субъединицы - полипептидные цепи (обозначаемые α1, α2, β1 и β2, каждая из которых связана с гемом.
Запомните, что гемоглобин относится к аллостерическим белкам, его молекулы могут обратимо переходить из одной конформации в другую. При этом изменяется сродство белка к лигандам. Конформация, обладающая наименьшим сродством к лиганду, называется напряжённой, или Т-конформацией. Конформация, обладающая наибольшим сродством к лиганду, называется релаксированной, или R-конформацией.
Различные факторы среды могут сдвигать это равновесие в ту или иную сторону. Аллостерическими регуляторами, влияющими на сродство Hb к O2, являются: 1) кислород; 2) концентрация Н+ (рН среды); 3) углекислота (СO2) ; 4) 2,3-дифосфоглицерат (ДФГ) . Присоединение молекулы кислорода к одной из субъединиц гемоглобина способствует переходу напряжённой конформации в релаксированную и повышает сродство к кислороду других субъединиц той же молекулы гемоглобина. Это явление получило название кооперативного эффекта. Сложный характер связывания гемоглобина с кислородом отражает кривая насыщения гемоглобина O2, имеющая S-образную форму (рисунок 3.1).
Повышение содержания СO2, Н+, ДФГ на фоне низкого парциального давления O2 в тканях способствует взаимодействию этих факторов с гемоглобином и переходу R-конформации в Т-конформацию. Это приводит к смещению равновесия в уравнении (1) вправо. Выделившийся O2 поступает в ткани.
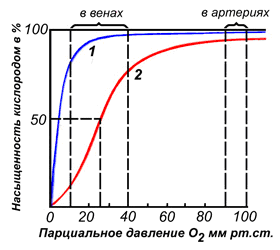
Рисунок 3.1. Кривые насыщения миоглобина (1) и гемоглобина (2) кислородом.
4. Биологические функции белков. Роль пространственной организации полипептидной цепи в образовании активных центров. Взаимодействие белков с лигандами. Денатурация белков.
Белки играют важнейшую роль в организме, выполняя многообразные биологические функции.Запомните наиболее важные из них и примеры соответствующих белков, изучив таблицу 2.2.
Таблица 2.2 Функциональная классификация белков |
||||||||||||||||||||||||
2.2.2. Обратите внимание на то, что в основе функционирования любого белка лежит его способность к избирательному взаимодействию со строго определёнными молекулами или ионами (лигандами) . Например, для ферментов, катализирующих химические реакции, лигандами будут вещества, участвующие в этих реакциях (субстраты), для транспортных белков - транспортируемые вещества и т.д. 2.2.3. Лиганд способен взаимодействовать не со всей поверхностью белковой молекулы, а только с определённым её участком, который представляет собой центр связывания или активный центр. Этот центр формируется пространственно сближенными радикалами аминокислот на уровне вторичной или третичной структуры белка. Способность лиганда взаимодействовать с центром связывания обусловлена их комплементарностью, то есть взаимным соответствием их пространственной структуры (подобно взаимодействию «ключ - замок»). Между функциональными группами лиганда и центра связывания образуются нековалентные (водородные, ионные, гидрофобные), а также ковалентные связи. Комплементарностью лиганда и центра связывания можно объяснить высокую специфичность (избирательность) взаимодействия белок - лиганд. Важно отметить, что изменение пространственной структуры белка в процессе денатурации (см. 2.4) приводит к разрушению центров связывания и утрате биологической функции белка. |
Денатурацией белков называется это изменение нативных (природных) физико-химических и, главное, биологических свойств белка вследствие нарушения его четвертичной, третичной и даже вторичной структуры. Денатурацию белка могут вызвать:
температура выше 60° С;
ионизирующая радиация;
концентрированные кислоты и щёлочи;
соли тяжёлых металлов (ртути, свинца, кадмия);
органические соединения (спирты, фенолы, кетоны) .
Для денатурированных белков характерно:
изменение конформации молекулы;
уменьшение растворимости в воде;
изменение заряда молекулы;
меньшая устойчивость к действию протеолитических ферментов;
потеря биологической активности.
Обратите внимание, что при определённых условиях возможно восстановление исходной (нативной) конформации белка после удаления фактора, вызвавшего денатурацию. Этот процесс получил название ренаживации.
Запомните некоторые примеры использования процесса денатурации белков в медицине:
для осаждения белков плазмы крови при определении содержания небелковых веществ в крови;
при проведении дезинфекции и санитарной обработки;
при лечении и профилактике отравлений солями тяжёлых металлов (в качестве противоядия применяют молоко или яичный белок);
для получения лекарственных веществ белковой природы (используется денатурация в мягких условиях с последующей ренативацией).
