
- •§ 1. Уравнение непрерывности
- •§ Pvrff,
- •§ 2. Уравнение Эйлера
- •§ 3. Гидростатика
- •§ 4. Условие отсутствия конвекции
- •§ 5. Уравнение Бернулли
- •§ 6. Поток энергии
- •§ 7. Поток импульса
- •§ 8. Сохранение циркуляции скорости
- •§ 9. Потенциальное движение
- •§ 10. Несжимаемая жидкость
- •§ 12. Гравитационные волны
- •§ 13. Внутренние волны в несжимаемой жидкости
- •§ 14. Волны во вращающейся жидкости
- •Глава II
- •§ 15. Уравнения движения вязкой жидкости
- •§ 16. Диссипация энергии в несжимаемой жидкости
- •§17. Течение по трубе
- •§ 18. Движение жидкости между вращающимися цилиндрами
- •§ 19. Закон подобия
- •§ 20. Течение при малых числах Рейнольдса
- •§ 21. Ламинарный след
- •§ 22. Вязкость суспензий
- •§ 23. Точные решения уравнений движения вязкой жидкости
- •§ 24. Колебательное движение в вязкой жидкости
- •§ 25. Затухание гравитационных волн
- •Глава III
- •§ 26. Устойчивость стационарного движения жидкости
- •§ 27. Устойчивость вращательного движения жидкости
- •§ 29. Неустойчивость тангенциальных разрывов
- •§ 30. Квазипериодическое движение и синхронизация частот3)
- •§ 31. Странный аттрактор
- •§ 32. Переход к турбулентности путем удвоения периодов
- •§ 33. Развитая турбулентность
- •§ 34. Корреляционные функции скоростей
- •§ 35. Турбулентная область и явление отрыва
- •§ 36. Турбулентная струя
- •§ 37. Турбулентный след
- •§ 38. Теорема Жуковского
- •Глава IV
- •§ 39. Ламинарный пограничный слой
- •1. Определить толщину пограничного слоя вблизи критической точки (см. § 10) на обтекаемом жидкостью теле.
- •2. Определить движение в пограничном слое при конфузорном (см. § 23) течении между двумя пересекающимися плоскостями (к.. Pohlhausen, 1921).
- •§ 41. Устойчивость движения в ламинарном пограничном слое
- •2) Эта аналогия указана а в. Тимофеевым (1979) и а а Андроновым и а л. Фабрикантом (1979); ниже мы следуем изложению а. В. Тимофеева.
- •8) При V"(y) шг 0 уравнение (41,2) вообще не имеет решений, удовлетворяющих необходимым граничным условиям.
- •§ 42. Логарифмический профиль скоростей
- •§ 43. Турбулентное течение в трубах
- •§ 44. Турбулентный пограничный слой
- •§ 45. Кризис сопротивления
- •§ 46. Хорошо обтекаемые тела
- •§ 47. Индуктивное сопротивление
- •§ 48. Подъёмная сила тонкого крыла
- •S2(£)-Citt) 6-«
- •Глава V
- •§ 49. Общее уравнение переноса тепла
- •§ 50. Теплопроводность в несжимаемой жидкости
- •§ 51. Теплопроводность в неограниченной среде
- •§ 52. Теплопроводность в ограниченной среде
- •§ 53. Закон подобия для теплопередачи
- •§ 54. Теплопередача в пограничном слое
- •ВгТт « - у«р-
- •§ 55. Нагревание тела в движущейся жидкости
- •§ 56. Свободная конвекция
- •§ 57. Конвективная неустойчивость неподвижной жидкости
- •§ 58. Уравнения гидродинамики для жидкой смеси
- •§ 59. Коэффициенты диффузии и термодиффузии
- •§ 60. Диффузия взвешенных в жидкости частиц
- •Глава VII
- •§ 61. Формула Лапласа
- •§ 62. Капиллярные волны
- •§ 63. Влияние адсорбированных пленок на движение жидкости
- •Глава VIII
- •§ 64. Звуковые волны
- •§ 66. Энергия и импульс звуковых волн
- •§ 66. Отражение и преломление звуковых волн
- •§ 67. Геометрическая акустика
- •§ 68. Распространение звука в движущейся среде
- •§ 69. Собственные колебания
- •§ 70. Сферические волны
- •§71. Цилиндрические волны
- •§ 72. Общее решение волнового уравнения
- •Ctjc42-(X-q2- (*/-г,)2'
- •§ 73. Боковая волна
- •§ 74. Излучение звука
- •§ 75. Возбуждение звука турбулентностью
- •V 1г' 4я j дхидх1к
- •§ 76. Принцип взаимности
- •§ 77. Распространение звука по трубке
- •§ 78. Рассеяние звука
- •§ 79. Поглощение звука
- •4. Определить дополнительное поглощение звука, распространяющегося в смеси двух веществ, связанное с диффузией (и. Г. Шапошников и 3. А Гольдберг, 1952).
- •§ 80. Акустическое течение
- •§ 81. Вторая вязкость
- •Глава IX
- •§ 82. Распространение возмущений в потоке сжимаемого газа
- •2) Во избежание недоразумений оговорим, что если перед обтекаемым телом возникает ударная волна, то эта область несколько увеличивается (см. § 122).
- •§ 83. Стационарный поток сжимаемого газа
- •§ 84. Поверхности разрыва
- •§ 85. Ударная адиабата
- •2) Такой выбор системы координат будет подразумеваться везде в этой главе, за исключением § 92.
- •§ 86. Ударные волны слабой интенсивности
- •§ 87] Направление изменения величин в ударной волне 463
- •§ 87. Направление изменения величин в ударной волне
- •§ 88. Эволюционность ударных волн
- •§ 89. Ударные волны в политропном газе
- •1. Получить формулу
- •§ 90. Гофрировочная неустойчивость ударных волн
- •2) Сравните с аналогичной ситуацией для тангенциальных разрывов — задача 2 § 84.
- •1) Эта неустойчивость тоже была указана с. П. Дьяковым (1954); правильное значение нижней границы в (90,17) найдено в. М. Конторовичем (1957).
- •§ 91. Распространение ударной волны по трубе
- •§ 92. Косая ударная волна
- •§ 93. Ширина ударных волн
- •§ 94. Ударные волны в релаксирующей среде
- •§ 96. Слабые разрывы
- •Глава X
- •§ 97. Истечение газа через сопло
- •§ 98. Вязкое движение сжимаемого газа по трубе
- •§ 99. Одномерное автомодельное движение
- •5. Определить движение в изотермической автомодельной волне разрежения.
- •§ 100. Разрывы в начальных условиях
- •§ 101. Одномерные бегущие волны
- •§ 102. Образование разрывов в звуковой волне
- •§ 103. Характеристики
- •§ 104. Инварианты Римана
- •§ 105. Произвольное одномерное движение сжимаемого газа
- •§ 106. Задача о сильном взрыве
- •§ 107. Сходящаяся сферическая ударная волна
- •2) Эта задача была рассмотрена независимо Гудерлеем (о. Guderleu, 1942) и л. Д. Ландау и к. П. Станюковичем (1944, опубликовано в 1955).
- •§ 108. Теория «мелкой воды»
- •Глава XI
- •§ 109. Волна разрежения
- •§ 111. Пересечение ударных волн с твердой поверхностью
- •§ 112. Сверхзвуковое обтекание угла
- •§ 113. Обтекание конического острия
- •Глава XII
- •§ 114. Потенциальное движение сжимаемого газа
- •§ 115. Стационарные простые волны
- •§ 116. Уравнение Чаплыгина (общая задача
- •§ 117. Характеристики плоского стационарного течения
- •§ 118. Уравнение Эйлера — Трикоми. Переход через звуковую скорость
- •§1191 Решение уравнения эйлера —трикоми 619
- •§ 119. Решения уравнения Эйлера — Трикоми вблизи неособых точек звуковой поверхности
- •§ 120. Обтекание со звуковой скоростью
- •§ 121. Отражение слабого разрыва от звуковой линии
- •Глава XIII
- •§ 122. Образование ударных воли при сверхзвуковом обтекании тел
- •§ 123. Сверхзвуковое обтекание заостренного тела
- •§ 124. Дозвуковое обтекание тонкого крыла
- •§ 125. Сверхзвуковое обтекание крыла
- •§ 126. Околозвуковой закон подобия
- •§ 127. Гиперзвуковой закон подобия
- •Глава XIV
- •§ 128. Медленное горение
- •§ 129. Детонация
- •§ 130. Распространение детонационной волны
- •§ 131. Соотношение между различными режимами горения
- •§ 132. Конденсационные скачки
- •Глава XV
- •§ 133. Тензор энергии-импульса жидкости
- •§ 134. Релятивистские гидродинамические уравнения
- •§ 135. Ударные волны в релятивистской гидродинамике
- •§ 136. Релятивистские уравнения движения вязкой и теплопроводной среды
- •§ 137. Основные свойства сверхтекучей жидкости
- •§ 138. Термомеханический эффект
- •§ 139. Уравнения гидродинамики сверхтекучей жидкости
- •§ 140. Диссипативные процессы в сверхтекучей жидкости
- •§ 141. Распространение звука в сверхтекучей жидкости
§ 59. Коэффициенты диффузии и термодиффузии
Диффузионный поток вещества i и тепловой поток q возникают в результате наличия в жидкости градиентов концентрации и температуры. Не следует при этом думать, что i зависит только от градиента концентрации, a q — только от градиента температуры. Напротив, каждый из этих потоков зависит, вообще говоря, от обоих указанных градиентов.
Если градиенты температуры и концентрации невелики, то можно считать, что i и q являются линейными функциями от Vp. и vr (от градиента давления — при заданных Vp и V7" — потоки q и i не зависят по той же причине, которая была уже указана для q в § 49). Соответственно этому напишем i и q в виде линейных функций от градиентов и. и Т:
i = - aV|x - Bvr,
q=_6Vp.-YVr-f pi.
Между коэффициентами В и 6 существует простое соотношение, являющееся следствием принципа симметрии кинетических коэффициентов. Содержание этого общего принципа заключается в следующем (см. V § 120). Рассмотрим какую-нибудь замкнутую систему и пусть хи х2 ... — некоторые величины, характеризующие состояние системы. Их равновесные значения определяются тем, что в статистическом равновесии энтропия 5 всей системы должна иметь максимум, т. е. должно быть Ха = 0, где Ха обозначают производные:
Предположим, что система находится в состоянии, близком к равновесному. Это значит, что все ха лишь мало отличаются от своих равновесных значений, а величины Ха малы. В системе будут происходить процессы, стремящиеся привести ее в состояние равновесия. Величины ха являются при этом функциями времени, а скорость их изменения определяется производными по времени ха; представим последние в виде функций от Ха и разложим эти функции в ряд. С точностью до членов первого порядка имеем:
ха = — Z ЧаьХъ- (59,2)
Принцип симметрии кинетических коэффициентов Онсагера утверждает, что величины уаь (называемые кинетическими коэффициентами) симметричны по индексам а, Ь:
УаЬ = УЬа. (59,3)
Скорость изменения энтропии 5 равна
S = ^ Хаха-
а
Пусть теперь сами величины ха различны в разных точках тела, т. е. каждый элемент объема тела должен характеризоваться своими значениями величин ха. Другими словами, будем рассматривать ха как функции от координат. Тогда в выражении для 5, кроме суммирования по а, надо произвести также и интегрирование по всему объему системы, т. е.
а
Что касается зависимости между Ха и ха, то обычно можно утверждать, что значения ха в каждой данной точке системы зависят только от значений величин Ха в этой же точке. Если это условие выполняется, то можно писать связь между ха и Ха для каждой точки в системе, и мы возвращаемся к прежним соотношениям.
В данном случае выберем в качестве величин ха компоненты векторов i и q — pi. Тогда из сравнения (58,7) с (59,4) видно, что роль величин Ха будут играть соответственно компоненты векторов T-'Vp и T~2VT Кинетическими же коэффициентами уаь будут являться коэффициенты при этих векторах в равенствах
, = -аГ(^)-РЯ(^-). ч-ц| = _6Г(^)-уГ2(^).
В силу симметрии кинетических коэффициентов должно быть BP = 67\ т. е.
6 = рТ.
Это и есть искомое соотношение. Мы можем поэтому написать потоки i и q в виде
i = - aVp - р* V7\ q = — pTVp, — уЧТ + pi (59,5)
всего с тремя независимыми коэффициентами: а, 8, у. В выражении для теплового потока удобно исключить градиент J7p, выразив его через i и $Т. Сделав это, получим:
i = - aVfi - Svr, (59,6)
q = (n + -^)i-*V7\
где введено обозначение
X = Y_ZL. (59)7)
Если поток вещества i отсутствует, то говорят о чистой теплопроводности. Для того чтобы было i =0, Т и и. должны удовлетворять уравнению aVp.+ BVT = 0, или
ady, + $dT = 0.
Интегрирование этого уравнения приводит к соотношению вида f(c,T) = 0, не содержащему в явном виде координат (химический потенциал является функцией не только от с, Т, но и от давления; в равновесии, однако, давление постоянно вдоль тела, и потому мы полагаем р = const). Это соотношение определяет связь между концентрацией и температурой, которая должна иметь место для отсутствия потока вещества. Далее, при i = 0 имеем из (59,7) q = —xVT"; таким образом, х является не чем иным, как теплопроводностью.
Перейдем теперь к обычным переменным р, Т и с. Имеем:
Последний член можно преобразовать, используя термодинамическое соотношение
dro = — sdT + Vdp + tide, (59,8)
где ф — термодинамический потенциал единицы массы, V — удельный объем. Имеем:
( д\х\ _ д\ _( дУ\ \др)с,Т дрдс V дс)р,г'
Подставив Vp. в (59,6) и введя обозначения
D=f (£),,• Ф -(*)„+ *• w
получим следующие выражения:
I = -pD(vc + -^vr + ^Vp), (59,11)
Коэффициент D называют коэффициентом диффузии; он определяет диффузионный поток при наличии одного только гра-
диента концентрации. Диффузионный же поток, вызываемый градиентом температуры, определяется коэффициентом термо-диффузии krD (безразмерную же величину кт называют термодиффузионным отношением). В учете последнего члена в (59,11) может возникнуть необходимость лишь при наличии в жидкости существенного градиента давления, вызванного, например, внешним полем. Величину kpD можно назвать коэффициентом баро-диффузии; мы вернемся еще к этой величине в конце параграфа.
В чистой жидкости диффузионный поток, разумеется, отсутствует. Поэтому ясно, что коэффициенты kr и kp должны обращаться в нуль на обоих пределах: с == 0 и с = 1.
Условие возрастания энтропии накладывает определенные ограничения на коэффициенты в формулах (59,6). Подставив эти формулы в выражение (58,7) для скорости изменения энтропии, получим:
±^PsdV = \^P^dV + \-£FdV+ ... (59,13)
Отсюда видно, что наряду с известным уже нам условием % > О должно выполняться также условие а > 0. Имея в виду, что согласно одному из термодинамических неравенств всегда
(*).,>»'
(см. V, § 96), мы находим, что должен быть положителен коэффициент диффузии: D > 0. Величины же ft г и kp могут быть как положительными, так и отрицательными.
Мы не станем выписывать громоздких общих уравнений, получающихся при подстановке полученных здесь выражений для i и q в уравнения (58,3), (58,6). Ограничимся лишь случаем, когда нет- никакого существенного градиента давления, а концентрация и температура настолько мало меняются в жидкости, что коэффициенты в выражениях (59,11) и (59,12), являющиеся в общем случае функциями от с и 7", можно считать постоянными. Будем, кроме того, считать, что в жидкости нет никакого макроскопического движения, помимо того, которое может быть вызвано самим наличием градиентов температуры и концентрации. Скорость такого движения будет пропорциональна этим градиентам, и потому в уравнениях (58,3) и (58,6) члены, содержащие скорость, оказываются величинами второго порядка малости и могут быть опущены. Величиной второго порядка является также и член iVp в (58,6). Таким образом, остается
Р-Ц- +divi = 0, рГ-g-+ div (q — pi) = 0.
Подставим сюда для i и q выражения (59,11) и (59,12) (без
ds
члена с Vp), а производную -^т преобразуем следующим
образом:
ds ( ds \ dT fds\ дс ср дт С^Л дс "дТ^КдТ)с,р~ЪТ"^"\дс)т, pW^TlTt \дт)р, С~Ы
Здесь учтено, что согласно (59,8):
(59,14)
![]()
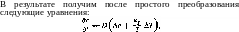
![]()
Эта система линейных уравнений определяет распределение температуры и концентрации в жидкости.
В особенности важен случай, когда концентрация смеси мала. При стремлении концентрации к нулю коэффициент диффузии стремится к некоторой конечной постоянной, а коэффициент термодиффузии— к нулю. Поэтому при малых концентрациях кт мало, и в уравнении (59,14) можно пренебречь членом krST, Оно переходит тогда в уравнение диффузии:
![]()
(59,16)
Граничные условия для уравнения (59,16) в разных случаях различны. На границе с поверхностью тела, не растворимого в жидкости, должна обращаться в нуль нормальная к поверхности компонента диффузионного потока i = —pDVc; другими словами, должно быть дс/дп — Q. Если же речь идет о диффузии от тела, растворяющегося в жидкости, то вблизи его поверхности быстро устанавливается равновесие, при котором концентрация в примыкающей к поверхности тела жидкости равна концентрации насыщенного раствора с0; диффузия вещества из этого слоя происходит медленнее, чем процесс растворения. Поэтому граничное условие на такой поверхности гласит: с — Cq. Наконец, если твердая поверхность «поглощает» попадающее на нее диффундирующее вещество, то граничным условием является равенство с = 0 (с таким случаем приходится, например, иметь дело при изучении химических реакций, происходящих на поверхности твердого тела).
Поскольку уравнения чистой диффузии (59, 16) и теплопроводности имеют одинаковый вид, то все выведенные в §§ 51, 52 формулы могут быть непосредственно перенесены на случай диффузии простой заменой Т на с и % на D. Граничному условию теплоизолированной поверхности соответствует при дйффузии условие на нерастворимой твердой поверхности; поверхности же, поддерживаемой при постоянной температуре, соответствует диффузия от поверхности растворяющегося в жидкости тела.
В частности, по аналогии с формулой (51,5) можно написать следующее решение уравнения диффузии:
c{\,t)= ^-^e-W. (59,17)
Оно определяет распределение растворенного вещества в произвольный момент времени, если в начальный момент / = 0 все вещество было сконцентрировано в бесконечно малом элементе объема жидкости в начале координат (М — полное количество растворенного вещества).
К сказанному в этом параграфе надо сделать важное замечание. Выражения (59,5) или (59,11—12) представляют собой первые неисчезающие члены разложения потоков по производным от термодинамических величин. Как известно из кинетической теории (см. X, §§ 5, 6, 14), такое разложение является, с микроскопической точки зрения, разложением (для газов) по степеням 1/L отношения длины свободного пробега молекул газа / к характерной пространственной длине задачи L. Учет членов с производными высших порядков означал бы учет величин более высокого порядка по указанному отношению. Следующими после написанных в (59,5) членов, которые можно образовать из производных от скалярных величин р и Т, были бы члены с производными третьего порядка: grad Ар, и gradAT1; эти члены заведомо малы по сравнению с уже учтенными в отношении (//Z,)2.
Но выражения для потоков могут содержать в себе также и члены с производными скорости. С помощью производных первого порядка, dvi/dxk, можно образовать лишь тензорные величины; это — вязкий тензор напряжений, входящий в состав тензора плотности потока импульса. Величины же векторного характера можно составить из производных второго порядка. Так, в векторе плотности диффузионного потока появятся члены
Г = рЛ,Ду + рл.,^гуу. (59,18)
Требование, чтобы эти члены были малы по сравнению с уже фигурирующими в формулах (59,11 — 12), приводит к дополнительным условиям применимости последних. Так, для того чтобы имело смысл оставлять в (59,11) член с Vp и в то же время опускать члены (59, 18), должно выполняться условие
--7 »^7t.
где р2 — pi — характерный перепад давлений на длине L, a U — характерный перепад скорости (в этой оценке положено kP ~ 1 — см. задачу). Согласно кинетической теории, D и % выражаются через характеристики теплового движения молекул газа. Уже из соображений размерности очевидно, что X/D ~ 1/vt, где vr — средняя тепловая скорость молекул. Учтя также, что давление газа р ~ pv2-, приходим к условию
Р2-Р1>Р^4"- <59'19>
Это условие отнюдь не выполняется автоматически. Напротив, в важном случае стационарных течений с малыми числами Рейнольдса в диффузионном потоке члены с Vp и с Ду оказываются одинакового порядка величины (Ю. М. Каган, 1962). Действительно, для такого движения градиент давления связан с производными скорости уравнением (20,1)
jVp = v\v (59,20)
(принимаем, что при движении газа его можно считать несжимаемым). Кинематическая вязкость оценивается как v ~ vrl и потому из этого уравнения находим:
р2 — Pi ~ ~ pvTU ~т
•—вместо неравенства в (59,19). Поскольку Ду прямо выражается через Vp согласно (20,1), то необходимость одновременного учета членов с Vp и Ду означает, что бародиффузионный коэффициент kP заменяется «эффективным» коэффициентом
(ApW = fcp—$5"- (59,21)
Обратим внимание на то, что этот коэффициент оказывается в результате кинетической величиной, а не чисто термодинамической, каковой является согласно (59,10) коэффициент kp.
Задача
Определить коэффициент бародиффузии для смеси двух идеальных газов. Решение. Для удельного объема имеем:
Г—у (Я1 + П.)
(обозначения — см. примечание на стр.321), а химические потенциалы имеют вид (см. V §93)
|ii-MP. Г) + Лп —qi—, И2 = ЫР. Г) + Пп —З2—.
Числа Л[, п% выражаются через концентрацию газа / согласно «imt = с, щгпг = 1 — с. Вычисление по формуле (59,10) дает
kp = (m2 - m,) с (1 - с) [±ZLi + ^-].
