
- •Часть 1
- •Глава I
- •§ 1. Статистическое распределение
- •§ 2. Статистическая независимость
- •§ 3. Теорема Лиувилля
- •§ 4. Роль энергии
- •§ 5. Статистическая матрица
- •§ 6. Статистическое распределение в квантовой статистике
- •§ 7. Энтропия
- •§ 8. Закон возрастания энтропии
- •Глава II
- •§ 9. Температура
- •§10. Макроскопическое движение
- •1) Производную по вектору надо понимать как вектор, составляющие которого равны производным по составляющим вектора, по которому произ- водится дифференцирование.
- •§11. Адиабатический процесс
- •§ 12. Давление
- •§ 13. Работа и количество тепла
- •§ 14. Тепловая функция
- •§ 15. Свободная энергия н термодинамический потенциал
- •§16. Соотношения между производными термодинамических
- •§ 16] Производные термодинамических величин
- •§ 17. Термодинамическая шкала температуры
- •§ 18. Процесс Джоуля — Томсона
- •§ 19. Максимальная работа
- •§ 20. Максимальная работа, производимая телом, находящимся во внешней среде
- •§ 20] Тело, находящееся во внешней среде 77
- •§ 21. Термодинамические неравенства
- •§ 22. Принцип Ле-Шателье
- •§ 23. Теорема Нернста
- •§ 24. Зависимость термодинамических величин от числа частиц
- •§ 25. Равновесие тела во внешнем поле
- •§ 26. Вращающиеся тела
- •§ 27. Термодинамические соотношения в релятивистской области
- •Глава III
- •§ 28. Распределение Гиббса
- •§ 29. Распределение Максвелла
- •§ 30. Распределение вероятностей для осциллятора
- •§ 31. Свободная энергия в распределении Гиббса
- •§ 32. Термодинамическая теория возмущений
- •§ 33. Разложение по степеням %
- •§ 34. Распределение Гиббса для вращающихся тел
- •§ 35. Распределение Гиббса с переменным числом частиц
- •§ 36. Вывод термодинамических соотношений из распределения Гиббса
- •Глава IV
- •§ 37. Распределение Больцмана
- •§ 38. Распределение Больцмана в классической статистике
- •§ 39. Столкновения молекул
- •§ 40. Неравновесный идеальный газ
- •§ 41. Свободная энергия больцмановского идеального газа
- •§ 42. Уравнение состояния идеального газа
- •§ 43. Идеальный газ с постоянной теплоемкостью
- •15. Определить максимальную работу, которую можно получить с по- мощью идеального газа при охлаждении от температуры т до температуры среды т0 при постоянном объеме.
- •§ 44. Закон равнораспределения
- •§ 43. Одноатомный идеальный газ
- •§ 46. Одноатомный газ. Влияние электронного момента
- •§ 47. Двухатомный газ с молекулами из различных атомов. Вращение молекул
- •§ 48. Двухатомный газ с молекулами из одинаковых атомов. Вращение молекул
- •§ 49. Двухатомный газ. Колебания атомов
- •§ 50. Двухатомный газ. Влияние электронного момента
- •§51] Многоатомный газ 169
- •§ 51. Многоатомный газ
- •§ 52. Магнетизм газов
- •Глава V
- •§ 53. Распределение Ферми
- •§ 54. Распределение Бозе
- •§ 55. Неравновесные ферми- и бозе-газы
- •§ 56. Ферми- и бозе-газы элементарных частиц
- •§ 56] Ферми- и бозе-газы элементарных частиц 185
- •§ 57. Вырожденный электронный газ
- •§ 58. Теплоемкость вырожденного электронного газа
- •§ 59. Магнетизм электронного газа. Слабые поля
- •§ 60. Магнетизм электронного газа. Сильные поля
- •§ 61. Релятивистский вырожденный электронный газ
- •§ 62. Вырожденный бозе-газ
- •§ 63. Черное излучение
- •Глава VI
- •§ 64. Твердые тела при низких температурах
- •§ 65. Твердые тела при высоких температурах
- •§ 66. Интерполяционная формула Дебая
- •§ 67. Тепловое расширение твердых тел
- •§ 68. Сильно анизотропные кристаллы
- •§ 69. Колебания кристаллической решетки
- •§ 70. Плотность числа колебаний
- •§ 71. Фононы.
- •§ 72. Операторы рождения и уничтожения фононов
- •§ 73. Отрицательные температуры
- •Глава VII
- •§ 74. Отклонение газов от идеальности
- •§ 75. Разложение по степеням плотности
- •§ 76. Формула ван-дер Ваальса
- •§ 77. Связь вириального коэффициента с амплитудой рассеяния
- •§ 78. Термодинамические величины классической плазмы
- •§ 79. Метод корреляционных функций
- •§ 80. Термодинамические величины вырожденной плазмы
- •1) В этом случае
- •Глава VIII
- •§ 81. Условия равновесия фаз
- •§ 82. Формула Клапейрона — Клаузиуса
- •§ 83. Критическая точка
- •§ 84. Закон соответственных состояний
- •Глава IX
- •§ 85. Системы с различными частицами
- •§ 86. Правило фаз
- •§ 87. Слабые растворы
- •§ 88. Осмотическое давление
- •§ 89. Соприкосновение фаз растворителя
- •§ 90. Равновесие по отношению к растворенному веществу
- •§ 91. Выделение тепла и изменение объема при растворении
- •§ 92. Растворы сильных электролитов
- •§ 93. Смесь идеальных газов
- •§ 94. Смесь изотопов
- •§ 95. Давление пара над концентрированным раствором
- •§ 96. Термодинамические неравенства в растворах
- •§ 97. Кривые равновесия
- •§ 98. Примеры диаграмм состояния
- •§ 99. Пересечение особых кривых поверхности равновесия
- •§ 100. Газ и жидкость
- •Глава X
- •§ 101. Условие химического равновесия
- •§ 102. Закон действующих масс
- •§ 103. Теплота реакции
- •§ 104. Ионизационное равновесие
- •§ 105. Равновесие по отношению к образованию пар
- •Глава XI
- •§ 106. Уравнение состояния вещества при больших плотностях
- •§ 107. Равновесие тел с большой массой
- •§ 108. Энергия гравитирующего тела
- •§ 109. Равновесие нейтронной сферы
- •Глава XII
- •§110. Распределение Гаусса
- •§ 110] Распределение гаусса 365
- •§ 111. Распределение Гаусса для нескольких величин
- •§ 113. Флуктуации в идеальном газе
- •§114. Формула Пуассона
- •§ 115. Флуктуации в растворах
- •§ 116. Пространственная корреляция флуктуации плотности
- •§ 117. Корреляция флуктуации плотности в вырожденном газе
- •§ 118. Корреляция флуктуации во времени
- •§ 119. Временная корреляция флуктуации нескольких величин
- •§ 120. Симметрия кинетических коэффициентов
- •§ 121. Диссипативная функция
- •§ 122. Спектральное разложение флуктуации
- •§ 123. Обобщенная восприимчивость
- •§ 123] Обобщенная восприимчивость 411
- •§ 124. Флуктуационно-диссипационная теорема
- •§ 125. Флуктуационно-диссипационная теорема для нескольких величин
- •§ 126. Операторное выражение обобщенной восприимчивости
- •§ 127. Флуктуации изгиба длинных молекул
- •Глава XIII
- •§ 128. Элементы симметрии кристаллической решетки
- •§ 129. Решетка Бравэ
- •§ 130. Кристаллические системы
- •§ 131. Кристаллические классы
- •§ 132. Пространственные группы
- •§ 133. Обратная решетка
- •§ 134. Неприводимые представления пространственных групп
- •§ 135. Симметрия относительно обращения времени
- •§ 136. Свойства симметрии нормальных колебаний кристаллической решетки
- •§ 137. Структуры с одно- и двумерной периодичностью
- •§ 138. Корреляционная функция в двумерных системах
- •§ 139. Симметрия по ориентации молекул
- •§ 140. Нематические и холестерические жидкие кристаллы
- •§ 141. Флуктуации в жидких кристаллах
- •Глава XIV
- •§ 142. Фазовые переходы второго рода
- •§ 143. Скачок теплоемкости
- •§ 144. Влияние внешнего поля на фазовый переход
- •§ 145. Изменение симметрии при фазовом переходе второго рода
- •§ 146. Флуктуации параметра порядка
- •§ 147. Эффективный гамильтониан
- •§ 148. Критические индексы
- •§ 149. Масштабная инвариантность
- •§ 150. Изолированные и критические точки непрерывного перехода
- •§ 151. Фазовый переход второго рода в двумерной решетке
- •§ 153. Флуктуационная теория критической точки
- •Глава XV
- •§ 154. Поверхностное натяжение
- •§ 155. Поверхностное натяжение кристаллов
- •§ 156. Поверхностное давление
- •§ 157. Поверхностное натяжение растворов
- •§ 158. Поверхностное натяжение растворов сильных электролитов
- •§ 159. Адсорбция
- •§ 160. Смачивание
- •§ 161. Краевой угол
- •§ 162. Образование зародышей при фазовых переходах
- •§ 1Б2] образование зародышей при фазовых переходах 581
- •§ 163. Невозможность существования фаз в одномерных системах
§ 62. Вырожденный бозе-газ
При низких температурах свойства бозе-газа не имеют ничего общего со свойствами ферми-газа. Это заранее очевидно из того, что у бозе-газа состоянием наименьшей энергии, в котором газ находится при 7 = 0, должно быть состояние с £ = 0 (все частицы в квантовом состоянии с е = 0), между тем как ферми-газ при абсолютном нуле обладает отличной от нуля энергией.
Если при заданной плотности N/V газа понижать его температуру, то химический потенциал р, определяемый уравнением (56,5) (с нижним знаком), будет увеличиваться, т. е., будучи отрицательным, уменьшаться по абсолютной величине. Он достигнет значения р. = 0 при температуре, определяемой равенством
N _g(mT)^} Yzdz ^
V 21/гяФ.) ez— 1 *
о
Входящий сюда интеграл выражается через ^-функцию (см. примечание на стр. 191); обозначая искомую температуру посредством Т0, получим
При Т <Т0 уравнение (56,5) не имеет отрицательных решений, между тем как в статистике Бозе химический потенциал должен быть отрицательным при всех температурах.
Это кажущееся противоречие связано с тем, что в данных условиях не законен переход от суммирования (в формуле (54,3)) к интегрированию (в формуле (56,5)). Действительно, при_этом переходе первый член суммы (с eft = 0) умножается на ]/е = 0, т. е. выпадает из суммы. Между тем при понижении температуры частицы должны скапливаться именно в этом состоянии с наименьшей энергией, пока при Т = 0 туда не попадут все они. Математически это обстоятельство проявляется в том, что в сумме (54,3) при переходе к пределу р—+0 сумма всех членов ряда, за исключением первого, стремится к конечному пределу (определяемому интегралом (56,5)), а первый член (с еА = 0) стремится к бесконечности. Устремляя р не к нулю, а к некоторому малому конечному значению, можно, следовательно, придать указанному первому члену суммы требуемое конечное значение.
Поэтому в действительности при Т < Т0 дело будет обстоять следующим образом. Частицы с энергией е > 0 распределены по формуле (56,4) с р = 0:
dN _ m8/2V V^de
Полное число частиц с энергиями е > 0 будет, следовательно,
о
Остальные
ЛГЕ=о = Лг[1-(-^-)3/2] (62,4)
р_ёУ(тТГ*Т
С
о
gV(mT)3/2T } z3/2dz
21/2яФ J ег—1 о
Этот интеграл приводится к £ (5/2) (см. примечание на стр. 191) и получается
/Т \ 3/2 тЗ/2т.5/2
£ = 0,770Л/Г(-) =0,128g^-^—V. (62,5)
С„
=
Ш> (62,6)
(
"° 2Т
т. е. теплоемкость пропорциональна Т3/2. Интегрируя теплоем- кость, находим энтропию:
S=~, (62,7)
и свободную энергию F — E— TS:
F^-~E. (62,8)
Последний результат вполне естествен, так как при р, = 0 F = (b~PV = Nn+Q = Q. Для давления Р =—(dF/dV)r имеем
тЗ/2Г5/2
P = 0,0851g^-_Z_. (62,9)
Мы видим, что при Т < Г0 давление пропорционально Тъ!г и не зависит вовсе от объема. Это обстоятельство—естественное следствие того, что частицы, находящиеся в состоянии с е = 0, не обладая импульсом, не дают никакого вклада в давление.
В самой точке Т = Т0 все перечисленные термодинамические величины непрерывны. Можно, однако, показать, что производная
Явление накапливания частиц в состоянии с е=0 называют конденсацией Бозе—Эйнштейна. Подчеркнем, что речь может при этом идти разве что о «конденсации в импульсном пространстве», никакой реальной конденсации в газе, конечно, не происходит.
от теплоемкости по температуре испытывает в этой точке скачок (см. задачу к этому параграфу). Кривая самой теплоемкости как функции от температуры имеет в точке Т = Т0 излом,
причем в этой точке теплоемкость максимальна (я равна
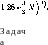 Определить
скачок производной (dCv/dT)v
в
точке Т
=
Т0.
Решение.
Для решения задачи надо определить
энергию газа при малых положительных
Т—Т„.
Переписываем
равенство (56,5) тождественно в виде
Определить
скачок производной (dCv/dT)v
в
точке Т
=
Т0.
Решение.
Для решения задачи надо определить
энергию газа при малых положительных
Т—Т„.
Переписываем
равенство (56,5) тождественно в виде
N = N0(T)
3/2
21/2п2Р
1
I
g(e-n)/r_ j
1
1
где функция N0 (Т) определяется равенством (62,1). Разлагаем подынтегральное выражение, имея в виду, что ц мало вблизи точки Т = Т0, а поэтому в интеграле существенна область малых е, и находим, что стоящий здесь интеграл равен
de
KM«+ll*D
-лТ У~Щ.
(1)
Подставляя это значение и выражая затем ц через N—N0, получим
2л2Р fN0 — N\2
g2ms
TV
С той же точностью пишем теперь:
ajj. 2 дц~ 2 N ~ 2 °'
откуда
■N
g2ms 0 у
TV
fdCv
\
дТ
(2)
6я*« Г ( 1 dN0
g2msV2
=—3,66^- . г=г0 Т0
*)
Подчеркнем, однако, что такое поведение
теплоемкости—результат именно полного
пренебрежения взаимодействием частиц
газа; ситуация меняется при введении
уже хотя бы слабого взаимодействия.
