
- •Часть 1
- •Глава I
- •§ 1. Статистическое распределение
- •§ 2. Статистическая независимость
- •§ 3. Теорема Лиувилля
- •§ 4. Роль энергии
- •§ 5. Статистическая матрица
- •§ 6. Статистическое распределение в квантовой статистике
- •§ 7. Энтропия
- •§ 8. Закон возрастания энтропии
- •Глава II
- •§ 9. Температура
- •§10. Макроскопическое движение
- •1) Производную по вектору надо понимать как вектор, составляющие которого равны производным по составляющим вектора, по которому произ- водится дифференцирование.
- •§11. Адиабатический процесс
- •§ 12. Давление
- •§ 13. Работа и количество тепла
- •§ 14. Тепловая функция
- •§ 15. Свободная энергия н термодинамический потенциал
- •§16. Соотношения между производными термодинамических
- •§ 16] Производные термодинамических величин
- •§ 17. Термодинамическая шкала температуры
- •§ 18. Процесс Джоуля — Томсона
- •§ 19. Максимальная работа
- •§ 20. Максимальная работа, производимая телом, находящимся во внешней среде
- •§ 20] Тело, находящееся во внешней среде 77
- •§ 21. Термодинамические неравенства
- •§ 22. Принцип Ле-Шателье
- •§ 23. Теорема Нернста
- •§ 24. Зависимость термодинамических величин от числа частиц
- •§ 25. Равновесие тела во внешнем поле
- •§ 26. Вращающиеся тела
- •§ 27. Термодинамические соотношения в релятивистской области
- •Глава III
- •§ 28. Распределение Гиббса
- •§ 29. Распределение Максвелла
- •§ 30. Распределение вероятностей для осциллятора
- •§ 31. Свободная энергия в распределении Гиббса
- •§ 32. Термодинамическая теория возмущений
- •§ 33. Разложение по степеням %
- •§ 34. Распределение Гиббса для вращающихся тел
- •§ 35. Распределение Гиббса с переменным числом частиц
- •§ 36. Вывод термодинамических соотношений из распределения Гиббса
- •Глава IV
- •§ 37. Распределение Больцмана
- •§ 38. Распределение Больцмана в классической статистике
- •§ 39. Столкновения молекул
- •§ 40. Неравновесный идеальный газ
- •§ 41. Свободная энергия больцмановского идеального газа
- •§ 42. Уравнение состояния идеального газа
- •§ 43. Идеальный газ с постоянной теплоемкостью
- •15. Определить максимальную работу, которую можно получить с по- мощью идеального газа при охлаждении от температуры т до температуры среды т0 при постоянном объеме.
- •§ 44. Закон равнораспределения
- •§ 43. Одноатомный идеальный газ
- •§ 46. Одноатомный газ. Влияние электронного момента
- •§ 47. Двухатомный газ с молекулами из различных атомов. Вращение молекул
- •§ 48. Двухатомный газ с молекулами из одинаковых атомов. Вращение молекул
- •§ 49. Двухатомный газ. Колебания атомов
- •§ 50. Двухатомный газ. Влияние электронного момента
- •§51] Многоатомный газ 169
- •§ 51. Многоатомный газ
- •§ 52. Магнетизм газов
- •Глава V
- •§ 53. Распределение Ферми
- •§ 54. Распределение Бозе
- •§ 55. Неравновесные ферми- и бозе-газы
- •§ 56. Ферми- и бозе-газы элементарных частиц
- •§ 56] Ферми- и бозе-газы элементарных частиц 185
- •§ 57. Вырожденный электронный газ
- •§ 58. Теплоемкость вырожденного электронного газа
- •§ 59. Магнетизм электронного газа. Слабые поля
- •§ 60. Магнетизм электронного газа. Сильные поля
- •§ 61. Релятивистский вырожденный электронный газ
- •§ 62. Вырожденный бозе-газ
- •§ 63. Черное излучение
- •Глава VI
- •§ 64. Твердые тела при низких температурах
- •§ 65. Твердые тела при высоких температурах
- •§ 66. Интерполяционная формула Дебая
- •§ 67. Тепловое расширение твердых тел
- •§ 68. Сильно анизотропные кристаллы
- •§ 69. Колебания кристаллической решетки
- •§ 70. Плотность числа колебаний
- •§ 71. Фононы.
- •§ 72. Операторы рождения и уничтожения фононов
- •§ 73. Отрицательные температуры
- •Глава VII
- •§ 74. Отклонение газов от идеальности
- •§ 75. Разложение по степеням плотности
- •§ 76. Формула ван-дер Ваальса
- •§ 77. Связь вириального коэффициента с амплитудой рассеяния
- •§ 78. Термодинамические величины классической плазмы
- •§ 79. Метод корреляционных функций
- •§ 80. Термодинамические величины вырожденной плазмы
- •1) В этом случае
- •Глава VIII
- •§ 81. Условия равновесия фаз
- •§ 82. Формула Клапейрона — Клаузиуса
- •§ 83. Критическая точка
- •§ 84. Закон соответственных состояний
- •Глава IX
- •§ 85. Системы с различными частицами
- •§ 86. Правило фаз
- •§ 87. Слабые растворы
- •§ 88. Осмотическое давление
- •§ 89. Соприкосновение фаз растворителя
- •§ 90. Равновесие по отношению к растворенному веществу
- •§ 91. Выделение тепла и изменение объема при растворении
- •§ 92. Растворы сильных электролитов
- •§ 93. Смесь идеальных газов
- •§ 94. Смесь изотопов
- •§ 95. Давление пара над концентрированным раствором
- •§ 96. Термодинамические неравенства в растворах
- •§ 97. Кривые равновесия
- •§ 98. Примеры диаграмм состояния
- •§ 99. Пересечение особых кривых поверхности равновесия
- •§ 100. Газ и жидкость
- •Глава X
- •§ 101. Условие химического равновесия
- •§ 102. Закон действующих масс
- •§ 103. Теплота реакции
- •§ 104. Ионизационное равновесие
- •§ 105. Равновесие по отношению к образованию пар
- •Глава XI
- •§ 106. Уравнение состояния вещества при больших плотностях
- •§ 107. Равновесие тел с большой массой
- •§ 108. Энергия гравитирующего тела
- •§ 109. Равновесие нейтронной сферы
- •Глава XII
- •§110. Распределение Гаусса
- •§ 110] Распределение гаусса 365
- •§ 111. Распределение Гаусса для нескольких величин
- •§ 113. Флуктуации в идеальном газе
- •§114. Формула Пуассона
- •§ 115. Флуктуации в растворах
- •§ 116. Пространственная корреляция флуктуации плотности
- •§ 117. Корреляция флуктуации плотности в вырожденном газе
- •§ 118. Корреляция флуктуации во времени
- •§ 119. Временная корреляция флуктуации нескольких величин
- •§ 120. Симметрия кинетических коэффициентов
- •§ 121. Диссипативная функция
- •§ 122. Спектральное разложение флуктуации
- •§ 123. Обобщенная восприимчивость
- •§ 123] Обобщенная восприимчивость 411
- •§ 124. Флуктуационно-диссипационная теорема
- •§ 125. Флуктуационно-диссипационная теорема для нескольких величин
- •§ 126. Операторное выражение обобщенной восприимчивости
- •§ 127. Флуктуации изгиба длинных молекул
- •Глава XIII
- •§ 128. Элементы симметрии кристаллической решетки
- •§ 129. Решетка Бравэ
- •§ 130. Кристаллические системы
- •§ 131. Кристаллические классы
- •§ 132. Пространственные группы
- •§ 133. Обратная решетка
- •§ 134. Неприводимые представления пространственных групп
- •§ 135. Симметрия относительно обращения времени
- •§ 136. Свойства симметрии нормальных колебаний кристаллической решетки
- •§ 137. Структуры с одно- и двумерной периодичностью
- •§ 138. Корреляционная функция в двумерных системах
- •§ 139. Симметрия по ориентации молекул
- •§ 140. Нематические и холестерические жидкие кристаллы
- •§ 141. Флуктуации в жидких кристаллах
- •Глава XIV
- •§ 142. Фазовые переходы второго рода
- •§ 143. Скачок теплоемкости
- •§ 144. Влияние внешнего поля на фазовый переход
- •§ 145. Изменение симметрии при фазовом переходе второго рода
- •§ 146. Флуктуации параметра порядка
- •§ 147. Эффективный гамильтониан
- •§ 148. Критические индексы
- •§ 149. Масштабная инвариантность
- •§ 150. Изолированные и критические точки непрерывного перехода
- •§ 151. Фазовый переход второго рода в двумерной решетке
- •§ 153. Флуктуационная теория критической точки
- •Глава XV
- •§ 154. Поверхностное натяжение
- •§ 155. Поверхностное натяжение кристаллов
- •§ 156. Поверхностное давление
- •§ 157. Поверхностное натяжение растворов
- •§ 158. Поверхностное натяжение растворов сильных электролитов
- •§ 159. Адсорбция
- •§ 160. Смачивание
- •§ 161. Краевой угол
- •§ 162. Образование зародышей при фазовых переходах
- •§ 1Б2] образование зародышей при фазовых переходах 581
- •§ 163. Невозможность существования фаз в одномерных системах
§ 39. Столкновения молекул
Молекулы газа, заключенного в сосуде, сталкиваются при своем движении с его стенками. Вычислим среднее число ударов молекул газа об единицу поверхности стенки за единицу времени.
Выберем какой-нибудь элемент поверхности стенки сосуда и введем систему координат с осью г, направленной перпендикулярно к этому элементу поверхности (который можно теперь написать в виде dxdy). Из молекул газа в единицу времени долетят до стенки сосуда, т. е. столкнутся с ней, только те, координаты z которых не больше, чем компонента vz их скорости по этой оси (которая, конечно, должна к тому же быть направлена к стенке, а не в противоположную сторону).
Число dvv столкновений молекул в единицу времени (отнесенное к единице площади поверхности стенки), при которых компоненты скорости лежат в заданных интервалах dvx, dvy, dvz, получится, следовательно, умножением распределения (38,4) на объем цилиндра с основанием 1 см2 и высотой, равной vz. Мы получим тогда
dvv = T(,2nrJ е z'vzdvxdvydvz. (39,1)
Отсюда легко найти полное число v ударов молекул газа об единицу поверхности стенки сосуда в единицу времени. Для этого проинтегрируем (39,1) по всем скоростям vz от 0 до оо и по vx и vv от —оо до +°° (по vz не надо интегрировать от —оо до О, так как при vz < 0 молекула летит в сторону, противоположную стенке, и, следовательно, не столкнется с ней). Это дает
*=тУш = уЬ? (39'2)
(плотность газа выражена через его давление согласно уравнению Клапейрона).
Формулу (39,1) можно написать в сферических координатах в пространстве скоростей, вводя вместо vx, vy, vz абсолютную величину скорости v и полярные углы 0 и ср, определяющие ее направление. Если выбрать полярную ось по оси г, то vz = v cos б и
dvv = -^- 3/2 ехр ^— Tffrj v3 sin 9 cos 6 dQ dy dv. (39,3)
Рассмотрим теперь столкновения молекул газа друг с другом. Для этого необходимо найти предварительно распределение молекул по их скоростям (скорость есть везде скорость центра инерции) относительно друг друга. При этом мы выбираем какую-нибудь из молекул газа и рассматриваем движение всех остальных молекул относительно этой, т. е. для каждой молекулы ■ мы
рассматриваем
не ее абсолютную скорость v
(относительно
стенок сосуда), а скорость v'
относительно
некоторой другой молекулы. Другими
словами, вместо того чтобы иметь дело
с отдельными молекулами, мы каждый раз
рассматриваем относительное движение
пары молекул, причем не интересуемся
движением их общего центра инерции.
Из
механики известно, что энергия
относительного движения двух частиц
(с массами тх
и
тъ)
равна
1/2mV2,
где
т'
=
=
m1m2l(m1Jrm!i)
—
их «приведенная масса», a
v'
—
относительная скорость. Поэтому
распределение молекул идеального газа
по относительным скоростям имеет такой
же вид, как и распределение по
абсолютным скоростям, но только вместо
т
стоит
приведенная масса т'.
Поскольку
все молекулы одинаковы, m'
= m/2, и
мы получаем для числа молекул в единице
объема, обладающих скоростью относительно
данной молекулы, лежащей между у' и
v'-j-dv',
выражение
(39,4)
Столкновения
молекул друг с другом могут сопровождаться
различными процессами: отклонением их
(рассеянием) на определенный угол,
распадом на атомы и т. д. Процессы,
происходящие при столкновениях, принято
характеризовать их эффективными
сечениями. Именно, эффективным
сечением
или
просто сечением для некоторого процесса,
происходящего нри столкновении данной
частицы с другими, называется отношение
вероятности такого столкновения в
единицу времени к плотности потока
частиц (плотностью потока называется
количество соответствующих частиц в
единице объема, помноженное на их
скорость). Поэтому число столкновений
(в единицу времени) данной частицы с
другими, сопровождающихся некоторым
процессом с сечением а,
равно![]()
![]()
(39,5)
Полное число таких столкновений, происходящих в единицу времени во всем объеме газа, равно, очевидно, v'N/2.
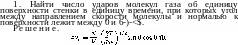
Задачи
