
- •Лабораторна робота № 1
- •3. Матеріали і обладнання :
- •4. Порядок проведення роботи.
- •4.1 Виявлення Карбону та Гідрогену
- •4.2 Виявлення Нітрогену
- •4.2.3 Хімізм процесу:
- •4.3 Виявлення Сульфуру.
- •Хімізм реакцій:
- •4.4 Виявлення Хлору. Реакція ф.Ф. Бейльштейна.
- •Хімізм реакцій:
- •4.5 Одержання метану і вивчення його властивостей.
- •4.7 Відношення рідких алканів до окисників.
- •Контрольні запитання:
- •Лабораторна робота № 2
- •1. Тема: Алкени. Алкіни.
- •3. Матеріали і обладнання:
- •4. Порядок проведення роботи:
- •4.1. Одержання етилену та його горіння.
- •4.1.3 Хімізм реакцій:
- •4.2 Приєднання до етилену брому.
- •4.3 Відношення етилену до окисників.
- •Одержання ацетилену і його горіння.
- •Приєднання до ацетилену брому.
- •Відношення ацетилену до окисників.
- •Утворення арґентуму ацетиленіду.
- •Контрольні запитання:
- •Лабораторна робота № 3.
- •Матеріали і обладнання :
- •Порядок проведення роботи:
- •Горіння бензену.
- •Дія перманганату калію.
- •4.4.Окислення гомологів бензену.
- •4.5 Нітрування бензену.
- •4.6 Бромування ароматичних вуглеводнів.
- •4.7 Вплив каталізатора на бромування ароматичних вуглеводнів.
- •4.8 Нітрування нафталену.
- •4.9 Возгонка нафталену (сублімація).
- •Хімізм реакцій: -
- •Контрольні запитання:
- •Література:
- •Лабораторна робота №4
- •Матеріали і обладнання:
- •4. Порядок проведення роботи:
- •4.1 Відношення спиртів до індикатора.
- •Хімізм реакцій:
- •Утворення і гідроліз алкоголятів.
- •Окислення етилового спирту купрум (іі) оксидом.
- •Окислення етилового спирту хромовою сумішшю.
- •Взаємодія гліцерину з купрум (іі) гідроксидом.
- •Хімізм реакцій:
- •Контрольні запитання:
- •Література:
- •Лабораторна робота № 5.
- •Тема: Гідроксильні сполуки і їх похідні. Феноли.
- •3. Матеріали і обладнання:
- •4. Порядок проведення роботи:
- •4.1 Розчинення фенолу у воді.
- •4.1.3 Хімізм реакцій:
- •4.2 Одержання натрію феноляту.
- •Розклад натрію феноляту хлоридною кислотою.
- •Реакція фенолу з ферум (ііі) хлоридом.
- •Нітрування фенолу.
- •Кольорові реакції багатоатомних фенолів з ферум (ііі) хлоридом.
- •Хімізм реакцій:
- •Окислення пірогалолу киснем повітря.
- •4.8.3 Хімізм реакцій:
- •Контрольні запитання:
- •Література:
- •Лабораторна робота № 6
- •Матеріали і обладнання:
- •Порядок проведення роботи:
- •4.1 Кислотні властивості карбонових кислот.
- •4.1.1. Хід роботи:
- •Спостереження:
- •Хімізм реакцій:
- •4.1.4 Висновок:
- •4.2. Окислення мурашиної кислоти калію перманганатом.
- •4.3. Розклад мурашиної кислоти при нагріванні з концентрованою сульфатною кислотою.
- •4.4.Одержання натрієвої солі щавлевої кислоти.
- •4.5. Розкладання щавлевої кислоти при нагріванні.
- •4.5.3. Хімізм реакцій:
- •4.6. Розклад щавлевої кислоти при нагріванні з концентрованою сульфатною кислотою.
- •4.6.3.Хімізм реакцій:
- •4.7. Окислення щавлевої кислоти калію перманганатом.
- •4.8. Приєднання брому до олеїнової кислоти.
- •Контрольні запитання:
- •Література:
- •Лабораторна робота № 7
- •Матеріали і обладнання:
- •4. Порядок проведення роботи:
- •4.1 Одержання ацететилового естеру.
- •4.1.3. Хімізм реакцій:
- •4.2. Взаємодія оцтового ангідриду з водою .
- •4.3. Взаємодія оцтового ангідриду з лугом.
- •4.3.3. Хімізм реакцій:
- •4.4.3. Хімізм реакцій:
- •4.5. Розчинність мила у воді.
- •4.5.3. Хімізм реакцій:
- •4.6. Виділення вільних жирних кислот із мила.
- •4.6.3. Хімізм реакцій:
- •4.7. Гідроліз спиртового розчину мила.
- •4.7.3. Хімізм реакцій:
- •4.8. Утворення нерозчинних кальцієвих солей жирних кислот.
- •4.8.3. Хімізм реакцій:
- •Література:
- •Лабораторна робота № 8.
- •1. Тема: Нітросполуки. Аміни. Реакції діазотування і азосполучення.
- •3. Матеріали і обладнання:
- •4.Порядок проведення роботи.
- •4.1.Одержання нітробензену.
- •4.2.Одержання динітробензену.
- •4.3. Нітрування фенолу.
- •4.4. Одержання метиламіну з ацетаміду.
- •4.4.3. Хімізм реакцій:
- •4.5. Властивості амінів жирного ряду.
- •4 .5.3. Хімізм реакцій:
- •4.6. Реакція з розчином купрум (іі) сульфату.
- •4.6.3. Хімізм реакцій:
- •4.7.3.Хімізм реакцій:
- •4.9.3. Хімізм реакцій:
- •4.11. Кольорова реакція аніліну з хлоридним вапном.
- •4.11.3. Хімізм реакцій:
- •4.12. Бромування аніліну.
- •4.12.3. Хімізм реакцій:
- •4.13. Діазотування сульфанілової кислоти.
- •4 .13.3. Хімізм реакцій:
- •4.14.Одержання геліантину.
- •4.14.3. Хімізм реакцій:
- •4.15. Властивості геліантину.
- •4.15.3. Хімізм реакцій:
- •Контрольні запитання:
- •Література:
- •Лабораторна робота № 9.
- •3. Матеріали і обладнання :
- •4.Порядок проведення роботи.
- •4.1.3. Хімізм реакцій:
- •4.2. Окислення глюкози амоніачним розчином арґентум оксиду ( реакція срібного дзеркала).
- •4.2.3. Хімізм реакцій:
- •4.3.Окислення глюкози лугом.
- •4.3.3. Хімізм реакцій:
- •4.4.3. Хімізм реакцій:
- •4.5.Кислотний гідроліз сахарози.
- •4.5.3. Хімізм реакцій:
- •4.6.Наявність відновлюючої здатності у лактози.
- •4.6.3. Хімізм реакцій:
- •Література :
- •Лабораторна робота № 10.
- •3. Матеріали і обладнання :
- •4.Порядок проведення роботи.
- •4.1.Реакція крохмалю з йодом.
- •4.1.3. Хімізм реакцій:
- •4.3.3. Хімізм реакцій:
- •4.4.Взаємодія клітковини з лугом.
- •4.4.3. Хімізм реакцій:
- •4.6.Одержання азотокислих ефірів (естерів) клітковини.
- •4.6.3. Хімізм реакцій:
4.8 Нітрування нафталену.
Хід роботи: в суху пробірку поміщають кристалик нафталену, 3 краплі нітратної кислоти, 2 краплі сульфатної кислоти. На водяній бані суміш нагрівають 2-3 хв. Гарячий розчин виливають у пробірку з холодною водою.
Спостереження: нафтален опускається на дно у вигляді оранжевої маслянистої рідини, яка твердне при збовтуванні.
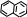
4.8.3 Хімізм реакцій: + НО – NO2 → + H2O
4.8.4 Висновок: ми добули нітронафтален. Нітрування нафталену проходить легше, ніж нітрування бензену.
4.9 Возгонка нафталену (сублімація).
4.9.1 Хід роботи: в суху пробірку поміщають кристалик нафталену і закріплюють її у штативі. Верхню половину пробірки обгортають вологим фільтрувальним папером і починають обережно нагрівати дно пробірки.
Спостереження: у охолоджуваній частині пробірки утворяться кристали нафталену.
Хімізм реакцій: -
Висновок: сублімація нафталену є одним із способів його очистки.
Контрольні запитання:
1. Методи одержання гомологів бензену.
2. Написати рівняння реакцій хімічних властивостей бензену, толуену, нафталену.
3. Здійснити синтези
З метану 2,4,6-тринітротолуен.
З етилену бромбензен.
З ацетилену нітробензен.
4. Скільки літрів Гідрогену необхідно для перетворення 100 г нафталену в декалін?
5. Із 78 г толуену при реакції нітрування було одержано 69 г о-нітротолуену. Скільки відсотків це становить від теоретичного виходу?
Література:
А.В.Аверина, А.Я.Снегирева. Лабораторный практикум по органической химии. М.: “ВШ”. 1980. Глава 3. Досл. 26,27,31,33. Глава 8. Досл. 136.
Лабораторна робота №4
Тема: Гідроксильні сполуки і їх похідні.
Мета: Вивчити властивості етилового спирту і гліцерину.
Матеріали і обладнання:
Етиловий спирт, гліцерин.
СuSO4 2 н розчин
Фенолфталеїн 1 %-ий розчин, лакмус 1 %-ий розчин.
Натрій металічний.
Хромова суміш, Н2SO4 концентрована.
4. Порядок проведення роботи:
4.1 Відношення спиртів до індикатора.
4.1.1 Хід роботи: в пробірку дають 3 краплі води і додають 2 краплі етанолу. Перевіряємо на фенолфталеїн і лакмус.
Спостереження: забарвлення індикаторів не змінюється
Хімізм реакцій:
Висновок: спирти – практично нейтральні речовини.
Утворення і гідроліз алкоголятів.
Хід роботи: в суху пробірку поміщають металічний натрій, додають 3 краплі етилового спирту і закривають пробірку пальцем. По закінченню реакції підносять пробірку до полум’я пальника і забирають палець. В отворі пробірки загоряється водень, який виділяється. Залишок натрію етилату розчиняють в 2-3 краплях дистильованої води і додають 1 краплю фенолфталеїну.
Спостереження: з’являється малинове забарвлення
Хімізм реакцій: С2Н5ОН + Na → C2H5ONa + ½H2 C2H5ONa + H – OH → C2H5OH + NaOH
Висновок: атоми водню гідроксильних груп в спиртах проявляють певну активність. В спиртах слабо виражені кислотні властивості.
