
- •1. История, современное состояние и перспективы развития газоснабжения
- •2.Современноесостояние и перспективы развития газоснабжения Беларуси
- •3. Закон Бойля-Мариотта
- •4. Уравнение состояния идеального газа
- •5. Закон Авогадро
- •6. Закон Грейама
- •7. Закон Дальтона
- •8. Закон Рауля
- •9 .Закон Генри
- •10. Критические параметры газов
- •11. Физико-химические свойства реальных газов
- •12. Состав и свойства горючих газов
- •13. Давление
- •14. Температура
- •14*. Объем
- •15. Масса, плотность и удельный объём газа.
- •16. Вязкость
- •17. Влажность газов
- •18. Диффузия газов
- •19. Теплоемкость газов
- •20. Теплопроводность газов
- •21. Теплота сгорания газов
- •22. Взаимозаменяемость газов. Число Воббе
- •23. Горение газов
- •24. Температура горения газов
- •25. Температура воспламенения газов
- •26. Пределы воспламеняемости
- •27. Скорость распространения пламени
- •28. Зависимость нормальной скорости распространения пламени от температурных условий
- •29. Зависимость критического диаметра (диаметра гашения) от температуры подогрева газовоздушной смеси
- •30.Природные газы
- •31.Попутные нефтяные газы
- •32.Сжиженные углеводородные газы
- •33. Пиролизные газы.
- •34. Газы безостаточной газификации
- •35. Топливо будущего – водород
- •36. Сероводород
- •37. Влага
- •38. Нафталин, пыль и смола
- •39. Балластные примеси
- •40. Влияние газов и продуктов их сгорания на организм человека
- •41. Окись углерода
- •42. Сероводород и сернистый газ
- •43. Сероуглерод
- •44. Аммиак
- •45. Цианистый водород
- •46. Предельные углеводороды
- •47. Азот и водород
- •48. Углекислота (диоксид углерода)
- •49. Окислы азота (no и no2)
- •50. Очистка газа от пыли и смолы
- •51. Осушка и охлаждение газовой смеси
- •52. Методы очистки газов от аммиака
- •53. Очистка газов от сероводорода, нафталина и цианистых соединений
- •54. Одоризация газов
- •55. Компрессорные станции (кс). Назн-е и размещение кс
- •56. Составные элементы кс
- •57. Газораспределительные станции (грс)
- •59. Прокладка газопроводов
- •61. Оборудование и сооружения на газопроводе
- •62. Стальные трубы
- •63. Полиэтиленовые трубы и их детали
- •64. Соединительные части и детали стальных труб
- •65. Уплотнительные материалы
- •66. Запорная и регулирующая арматура
- •67. Задвижки
- •68. Краны
- •69. Вентили
- •70. Гидравлические затворы
- •71 Спец. Устройства и устройства для предохранения газопроводов от повреждений.
- •72 Назначение и класификация грп (гру)
- •73 Размещение грп :
- •74. Размещение шкафных грп
- •75. Размещение гру:
- •76. Оборудование грп и гру.
- •77.Компоновка отдельно стоящих грп.
- •78. Компоновка шкафных грп.
- •82.Предохранительно-запорный клапан.
- •83. Предохранительно-сбросной клапан.
- •84.Газовые фильтры.
18. Диффузия газов
Диффузией называется процесс проникновения молекул одного вещества в массу другого или процесс распространения вещества, в какой – либо среде.
Различают три вида диффузии газов: газ в газ, газ в жидкость и газ в твердое тело.
Диффузия газ в газ представляет собой свободную диффузию. Она происходит во всех случаях смешения различных газов.
Диффузия газ в жидкость происходит в процессе контакта газа с жидкостью, при котором происходит проникновение газа в жидкость и его поглощение (процесс абсорбции).
Диффузия газ в твердое вещество происходит в процессе контакта газа с твердым телом, при котором происходит проникновение молекул газа в поры твердого тела (процесс адсорбции).
Движущей силой процесса диффузии является градиент давления, который представляет собой изменение парциального давления на единицу пути диффундируемого газа, т.е. dP/dx
Количество газа, продиффундировавшего через единицу поверхности в единицу времени называется скоростью диффузии. Она определяется по следующей формуле:
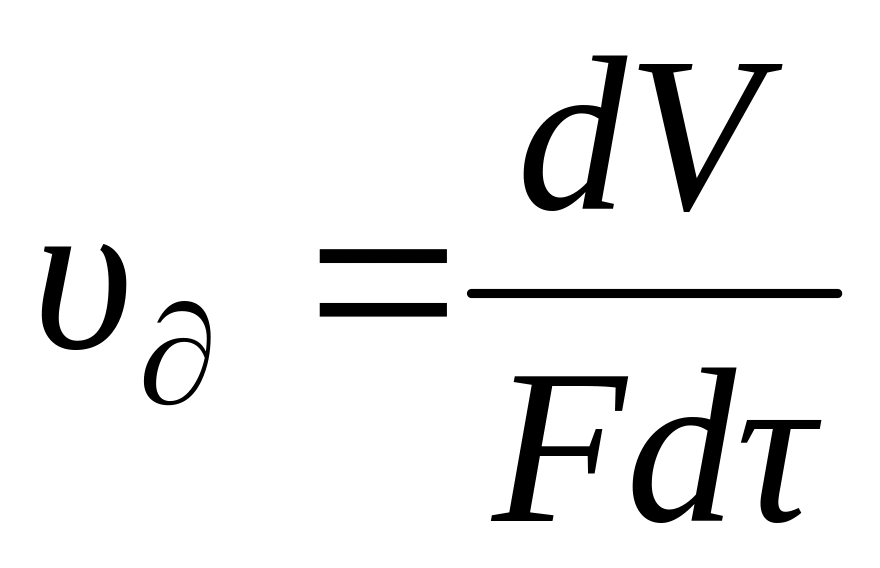 ,где
д
– скорость диффузии; V
– количество продиффундировавшего
газа (в объемных единицах); F
– поверхность диффузии;
- время диффузии. Согласно закону Фика:
,где
д
– скорость диффузии; V
– количество продиффундировавшего
газа (в объемных единицах); F
– поверхность диффузии;
- время диффузии. Согласно закону Фика:
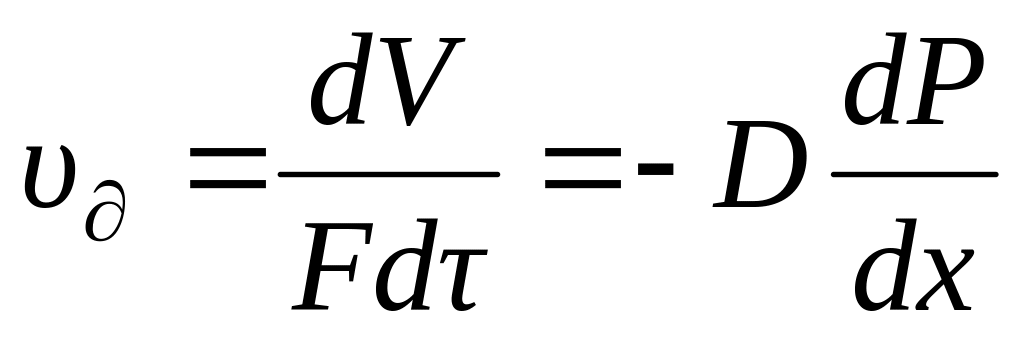 ,
где D
– коэффициент диффузии.
,
где D
– коэффициент диффузии.
Знак минус показывает, что с увеличением расстояния x происходит уменьшение давления Р. Процесс диффузии одного газа в другой в значительной степени зависит от температуры и давления. Если нам известен коэффициент диффузии D0,полученный при температуре T0 и давлении P0, а нам необходимо определить коэффициент диффузии D1, при температуре Т1 и давлении Р1, то необходимо использовать следующее уравнение:
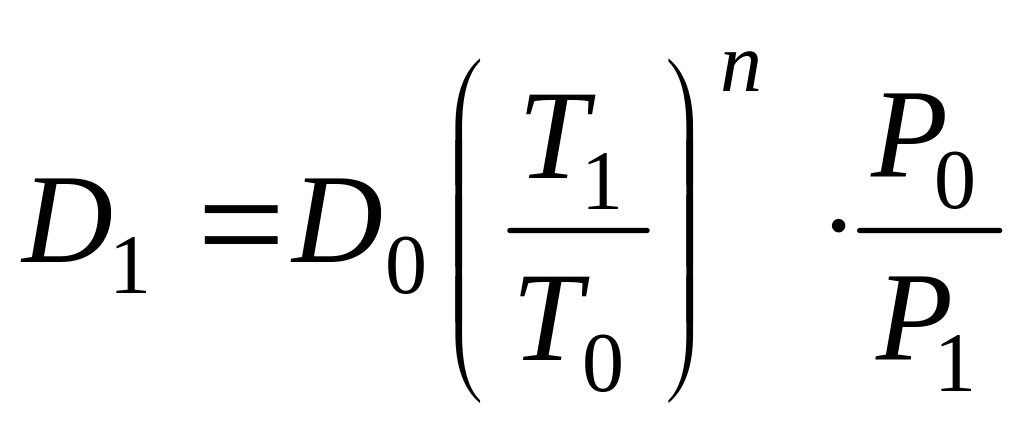 ,
где n
– показатель степени (n
= 1.5…2.0). – для неподвижных систем.
,
где n
– показатель степени (n
= 1.5…2.0). – для неподвижных систем.
Для
систем находящихся в движении:
![]()
ГД D2 – значение коэффициента диффузии с учетом перемещения газа или жидкости;
D1 – коэффициент диффузии для неподвижной системы;
- скорость потока газа или жидкости.
В соответствии с законом Грейама скорость диффузии разных газов обратно пропорциональна корню квадратному из их молекулярных весов. При Р=const и t=const для водорода:
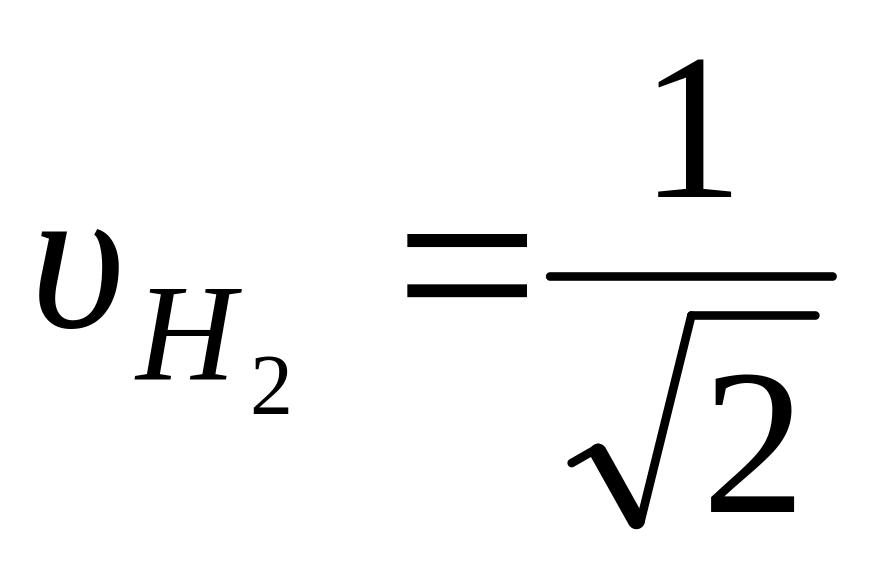 ;
для кислорода:
;
для кислорода:
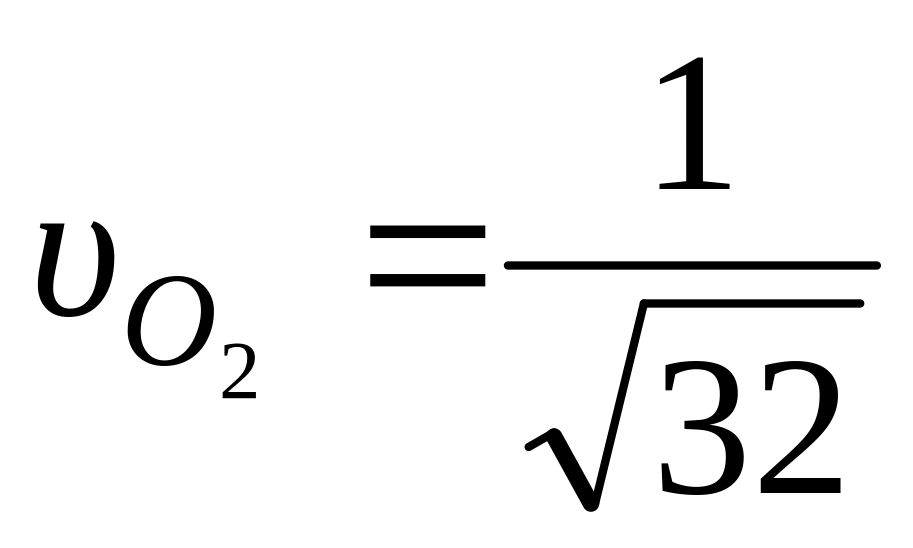 .
.
Коэффициент диффузии газа в жидкость:
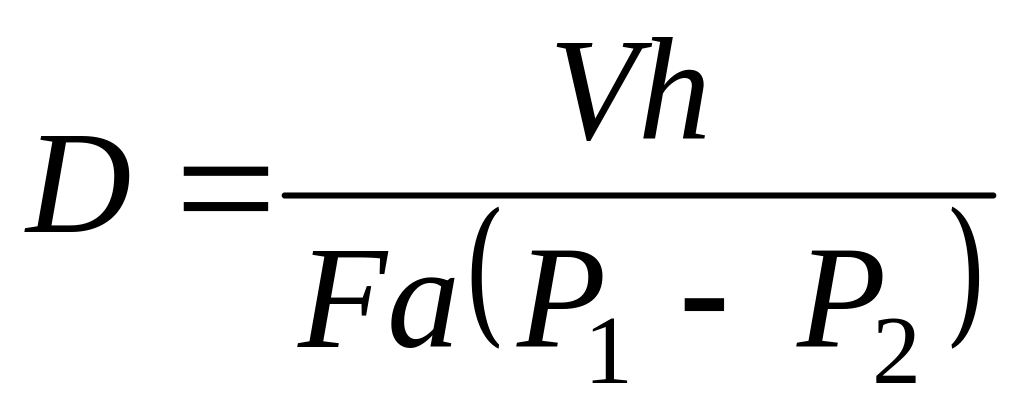
где V – количество диффундируемого газа;
F – площадь контакта газ-жидкость;
h – толщина слоя жидкости;
a – коэффициент растворимости;
(P1 – P2) – перепад давления.
19. Теплоемкость газов
Количество тепла, необходимого для нагревания единицы веса или объема газа на 1 0С называется теплоемкостью.
Если предположить, что некоторый объем газа нагревается с температуры t1 до температуры t2. В результате на этот нагрев затрачивается некоторое количество тепла Q. Тогда средняя теплоемкость вещества может быть определена как отношение количества тепла, затраченного на нагревание вещества к разности температур, т.е.:
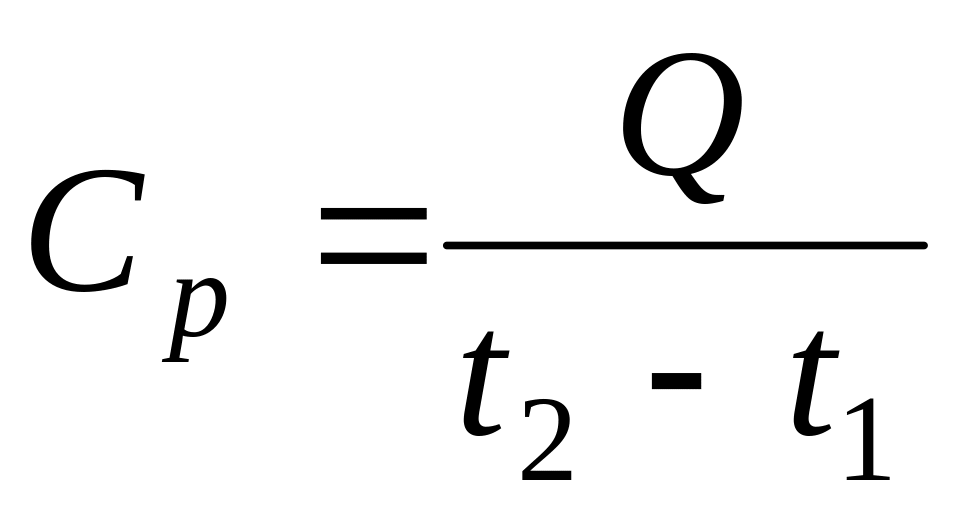 Теплоёмкость
измеряется в Дж
/(кгК)
или Дж/
(м3К).
Теплоёмкость
измеряется в Дж
/(кгК)
или Дж/
(м3К).
В случае, когда тепло подводят к газу, находящемуся в сосуде с постоянным объемом, то мы имеем дело с теплоемкостью при постоянном объеме, СV. В случае же подвода тепла к газу при постоянном давлении, мы имеем дело с теплоемкостью при постоянном давлении, СР.
Значение истинной теплоемкости, при данной температуре:
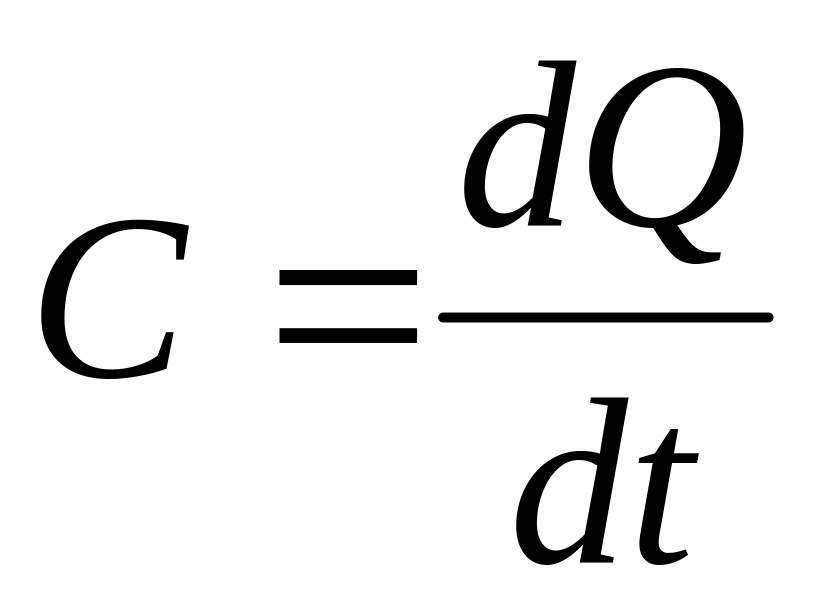 .
.
Отношение теплоемкости при постоянном давлении к теплоемкости при постоянном объеме называется показателем адиабаты и обозначается буквой k, т.е.
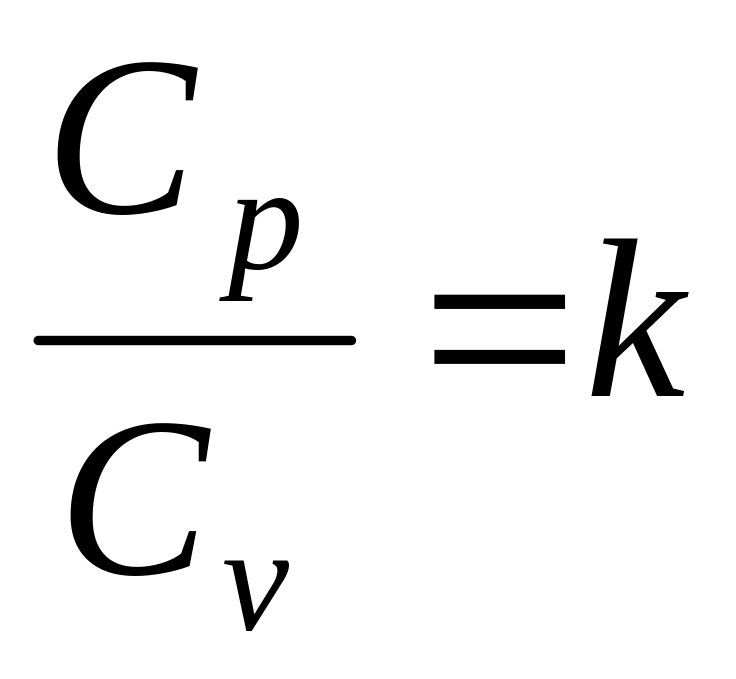 .
.
Следует отметить, что теплоемкость при постоянном давлении СР всегда больше теплоемкости при постоянном объеме СV.
Приведенные выше уравнения справедливы для идеальных газов. Для реальных газов значения теплоемкости будут отличаться от идеальных на величину дополнительного слагаемого:
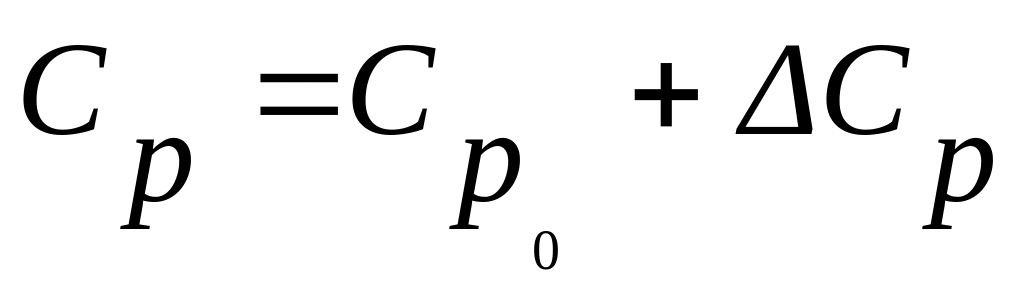 ,
,
где ![]() -
теплоемкость газа, приведенного к
идеальному состоянию;
-
теплоемкость газа, приведенного к
идеальному состоянию; ![]() -
корректирующий параметр, который
учитывает изменение теплоемкости от
давления и температуры.
-
корректирующий параметр, который
учитывает изменение теплоемкости от
давления и температуры.
