
- •Оглавление
- •Введение
- •1. Основные понятия термодинамики
- •1.1. Термодинамическая система
- •1.2. Состояние и параметры состояния термодинамической системы
- •1.3. Термодинамическое состояние
- •1.4. Уравнение состояния идеального газа
- •1.5. Термодинамический процесс
- •1.6. Внутренняя энергия
- •2. Основные законы термодинамики
- •2.1. Первое начало (первый закон) термодинамики
- •2.2. Второе начало термодинамики
- •3. Дифференциальные уравнения термодинамики
- •4. Основные термодинамические процессы
- •4.1. Политропный процесс
- •4.2. Расчет политропных процессов идеального газа
- •4.3. Частные случаи политропных процессов
- •5. Термодинамика систем с переменным числом частиц
- •5.1. Уравнение Гиббса
- •5.2. Термодинамические потенциалы и характеристические функции
- •5.3. Химический потенциал и его свойства
- •5.4. Термодинамика фазовых переходов
- •5.4.1. Фазы и компоненты
- •5.4.2. Фазовые переходы I и II рода
- •5.4.3. Правило фаз Гиббса. Условия термодинамического равновесия однофазной и многофазных систем
- •5.4.4. Уравнение Клапейрона – Клаузиса
- •6. Реальные газы (водяной пар)
- •6.1. Термодинамические свойства водяного пара
- •6.2. Процессы водяного пара
- •6.3. Диаграмма
- •7. Термодинамика потока
- •7.1. Основные законы для потока
- •7.1.1. Первое и второе начала термодинамики для потока
- •7.1.2. Массовый расход. Уравнение неразрывности
- •7.2. Сопло и диффузор
- •7.3. Скорость истечения и расход в адиабатически изолированных каналах без трения
- •7.4. Закон обращения геометрического воздействия
- •7.5. Дросселирование газов и паров
- •Список литературы
- •Дополнительная литература
- •Методические разработки
- •Часть 1 Основные законы и процессы термодинамики
2. Основные законы термодинамики
2.1. Первое начало (первый закон) термодинамики
Первое начало термодинамики это закон сохранения полной энергии, для термодинамической системы.
Если система как целое остается неподвижной при взаимодействии с окружающей средой, то изменяется ее внутренняя энергия. Обычно I начало термодинамики записывают для неподвижных систем и формулируют следующим образом: теплота, подведенная к системе, затрачивается на изменение ее внутренней энергии и на совершение ею работы:
![]() .
.
Знаки перед L и Q выбраны в соответствии с принятым в технической термодинамике условием, что положительными считаются работа, совершаемая системой над внешними телами, и теплота, подводимая к системе.
Для бесконечно малого изменения параметров системы
![]() .
.
где
![]() – бесконечно малые количества теплоты
и работы в процессе, а
– бесконечно малые количества теплоты
и работы в процессе, а
![]() – дифференциально малое изменение
внутренней энергии.
– дифференциально малое изменение
внутренней энергии.
Закон сохранения энергии может быть также сформулирован в виде утверждения о невозможности построения так называемого вечного двигателя (perpetuum mobile) I рода, т.е. такого искусственно созданного устройства, которое позволяло бы получать полезную работу без затраты энергии извне. Несмотря на то, что закон сохранения энергии еще не был сформулирован, французская академия наук в 1775 году приняла решение о прекращении рассмотрения проектов вечного двигателя любой конструкции.
Первый закон термодинамики может быть записан для удельных величин:
![]() .
.
В случае простых систем, для
которых
![]() ,
,
![]()
Если в качестве независимых параметров системы выбрать температуру T и удельный объем v, то полный дифференциал внутренней энергии будет записываться в виде
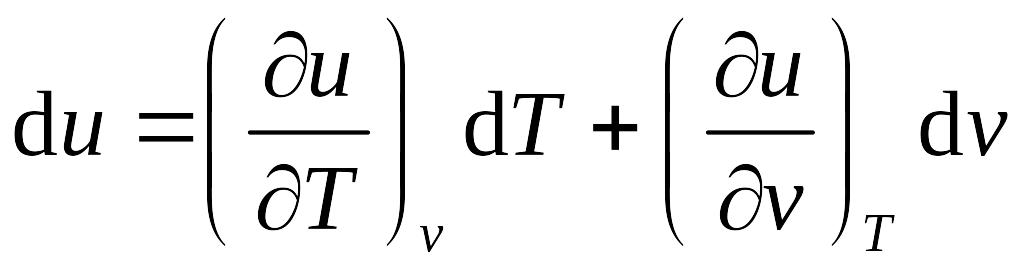 .
.
Энтальпия и полезная внешняя работа
П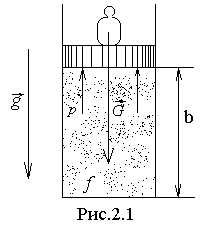 усть
в вертикально расположенном цилиндре
под поршнем находится газ (рис.2.1). На
поршень давит груз весом G = Mгрg.
Если груз вместе с поршнем неподвижны,
значит, на поршень снизу действует
давление со стороны газа, равное
усть
в вертикально расположенном цилиндре
под поршнем находится газ (рис.2.1). На
поршень давит груз весом G = Mгрg.
Если груз вместе с поршнем неподвижны,
значит, на поршень снизу действует
давление со стороны газа, равное
![]() ,
где f – площадь поршня. Это выражение
может быть записано в виде
,
где f – площадь поршня. Это выражение
может быть записано в виде
![]() .
Умножив левую и правую части этого
равенства на высоту b
положения поршня от дна цилиндра, получим
.
Умножив левую и правую части этого
равенства на высоту b
положения поршня от дна цилиндра, получим
![]() .
Произведение
есть потенциальная энергия поршня с
грузом в поле тяжести Земли, удерживающая
газ в заданном объеме V, рассчитанная
по отношению к положению дна цилиндра.
Можно показать, что и в общем случае
потенциальная энергия оболочки,
удерживающей систему, равняется
произведению pV. При
этом система не обязательно должна быть
заключена в физическую оболочку.
.
Произведение
есть потенциальная энергия поршня с
грузом в поле тяжести Земли, удерживающая
газ в заданном объеме V, рассчитанная
по отношению к положению дна цилиндра.
Можно показать, что и в общем случае
потенциальная энергия оболочки,
удерживающей систему, равняется
произведению pV. При
этом система не обязательно должна быть
заключена в физическую оболочку.
Если в качестве системы
рассматривать не только газ, но и груз
с поршнем, то энергия такой расширенной
системы будет складываться из
внутренней энергии газа и потенциальной
энергии поршня с грузом. Эта энергия и
называется энтальпией
термодинамической системы и обозначается
буквой H:
![]() .
.
Применим к I закону термодинамики преобразование Лежандра:
![]() .
.
Здесь под знаком полного дифференциала появляется новая функция состояния – энтальпия (старое название – теплосодержание). Таким образом, первое начало термодинамики может быть записано в двух эквивалентных формах:

В результате этого преобразования
появилось слагаемое
![]() ,
имеющее смысл бесконечно малого
количества некоторой работы
,
имеющее смысл бесконечно малого
количества некоторой работы
![]() :
:
![]() .
.
Интеграл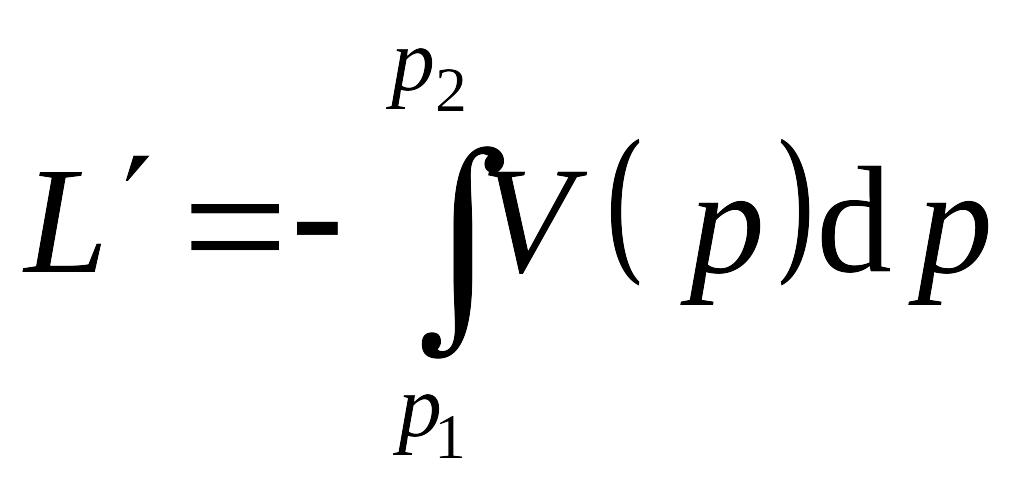
носит название
полезной внешней работы (или располагаемой
работы). Выясним смысл полезной внешней
работы. Работа
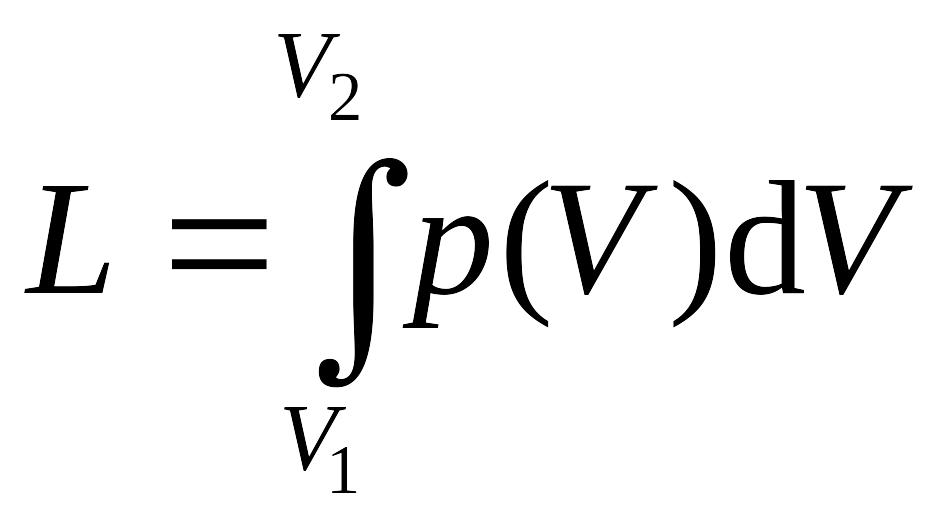 ,
которую можно назвать работой изменения
объема, представляет собой работу,
совершаемую системой против внешних
сил. Часть этой работы, называемая
работой проталкивания Lпр,
затрачивается на изменение потенциальной
энергии оболочки и может быть вычислена
как разность
,
которую можно назвать работой изменения
объема, представляет собой работу,
совершаемую системой против внешних
сил. Часть этой работы, называемая
работой проталкивания Lпр,
затрачивается на изменение потенциальной
энергии оболочки и может быть вычислена
как разность
![]() .
.
Дифференциал этой работы, очевидно, полный. Разность бесконечно малых количеств работы и работы проталкивания равна
![]()
или после
интегрирования ![]() .
.
Таким образом, полезная внешняя работа есть разность между работой термодинамической системы и работой проталкивания.
Г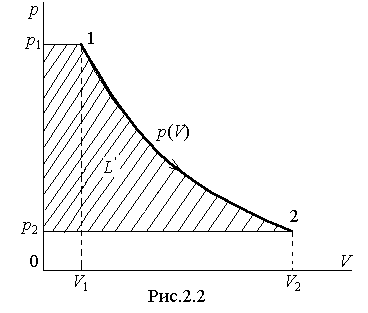 рафически
количество полезной внешней работы L',
соответствует площади слева от кривой
зависимости p(V)
в координатахp – V
(рис.2.2).
рафически
количество полезной внешней работы L',
соответствует площади слева от кривой
зависимости p(V)
в координатахp – V
(рис.2.2).
Таким образом, первое начало термодинамики для простых систем может быть записано в виде
![]() .
.
Полный дифференциал удельной энтальпии в переменных T и p имеет вид
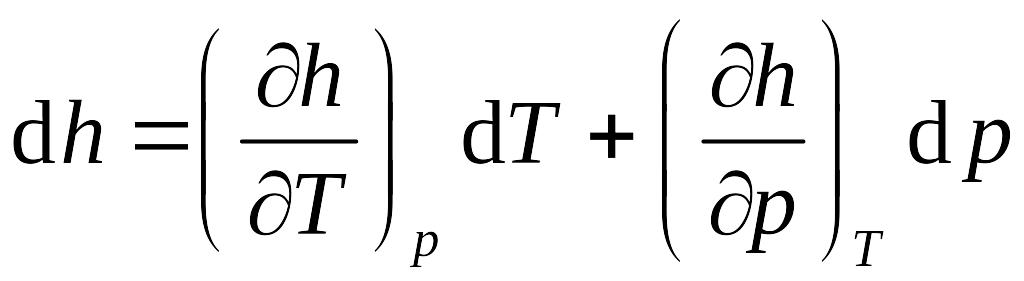 .
.
Лекция 5
