
- •1.Общая характеристика колебательных процессов
- •2. Дифференциальное уравнение гармонических колебаний
- •3. Колебания пружинного маятника
- •4. Колебания физического маятника
- •5. Вертикальные колебания центра тяжести судна
- •6. Энергия гармонического колебания
- •Сложение скалярных колебаний
- •8. Сложение гармонических колебаний с равными частотами
- •8.2 Сложение гармонических колебаний с близкими частотами. Биения
- •21.9. Сложение взаимно перпендикулярных (векторных) колебаний
- •Затухающие колебания
- •1. Вынужденные колебания
- •2. Вынужденные вертикальные колебания судна
- •3. Параметрический резонанс
- •4. Автоколебания
- •5. Спектр колебаний
- •. Ангармонические колебания
- •7. Фазовая траектория
- •Общая характеристика волновых процессов
- •22.2. Упругие волны
- •3. Энергетические характеристики волновых процессов
- •Акустика
- •1. Объективные и субъективные характеристики звука
- •2. Распространение звуковых волн
- •3. Ультразвук
- •4. Эффект Доплера в акустике
- •Статистическая теория газов
- •1. Средние характеристики движения молекул идеального газа
- •2. Распределение молекул по скоростям (распределение Максвелла)
- •3. Барометрическая формула
- •4. Распределение Больцмана
- •5. Средняя длина свободного пробега молекул
- •1. Общая характеристика явлений переноса
- •2. Молекулярно-кинетическая теория явлений переноса
- •8.6.3. Анализ коэффициентов переноса
- •1. Основные понятия термодинамики
- •Первое начало термодинамики и его применение к изопроцессам
- •9.3. Число степеней свободы. Внутренняя энергия идеального газа
- •1. Классическая теория теплопроводности газов
- •2. Адиабатный процесс
- •3. Обратимые и необратимые процессы. Круговые процессы (циклы). Принцип действия тепловой машины
- •4. Идеальная тепловая машина Карно
- •1. Второе начало термодинамики
- •9.9. Энтропия
- •2. Статистический смысл второго начала термодинамики
- •4. Теорема Нернста (третье начало термодинамики)
- •5. Термодинамика необратимых процессов
- •10.1. Реальные газы
- •10.1.2. Модель реального газа по Ван-дер-Ваальсу
- •10.1.3. Опытные изотермы реальных газов
- •10.1.4. Теоретические изотермы реальных газов (изотермы Ван-дер-Ваальса)
- •10.1.5. Расчет критических параметров вещества из уравнения Ван-дер-Ваальса
- •10.2. Жидкое состояние
- •10.2.1. Общие представления. Характер теплового движения молекул жидкости
- •10.2.2. Поверхностные явления
- •10.3. Твердое тело
- •10.3.1. Общие представления о твердых телах
- •10.3.2. Теплоемкость твердых тел. Закон Дюлонга и Пти
- •10.4. Фазовые равновесия и фазовые переходы
- •10.4.1. Общие понятия
- •10.4.2. Фазовый переход первого рода. Уравнение Клапейрона-Клаузиуса
10.2.2. Поверхностные явления
В отличие от газов жидкости имеют поверхность, отделяющую их от другой (например, газовой) фазы. Рассмотрим явления, происходящие на этой поверхности раздела.
Рис. 10.8
Если сфера взаимодействия лежит внутри жидкости, то в силу изотропности свойств жидкости результирующая сила, действующая на молекулу, равна нулю (рис. 10.8, а). Если же сфера взаимодействия частично выходит за пределы жидкости, то полной компенсации не будет – возникнет результирующая сила, направленная в глубь жидкости (рис. 10.8, б, в). Таким образом, результирующие силы всех молекул поверхностного слоя оказывают на жидкость давление, которое называется внутренним (или межмолекулярным).
Рис. 10.9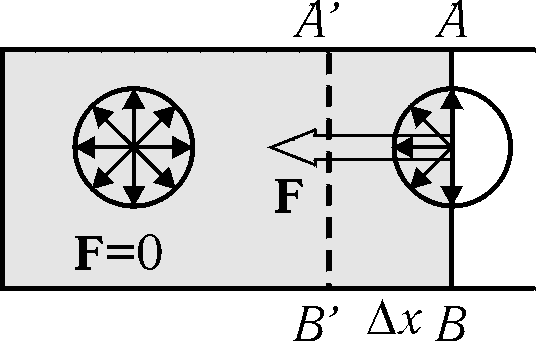
Суммарная сила F, действующая на все молекулы, находящаяся на границе раздела "пленка-воздух", пропорциональна числу молекул N, которое, в свою очередь, пропорционально длине l линии раздела. Таким образом,
-
 ,
,(10.6)
где – коэффициент поверхностного натяжения.
Из (10.6) видно, что коэффициент поверхностного натяжения численно равен силе поверхностного натяжения, действующей на единицу длины линии раздела и направленной в глубь пленки перпендикулярно к линии раздела.
Если граница раздела АВ (рис. 10.9) не закреплена, то под действием силы поверхностного натяжения эта граница будет перемещаться и спустя некоторое время займет положение A'B'. Работа этой силы
-
 ,
,
Рис. 10.10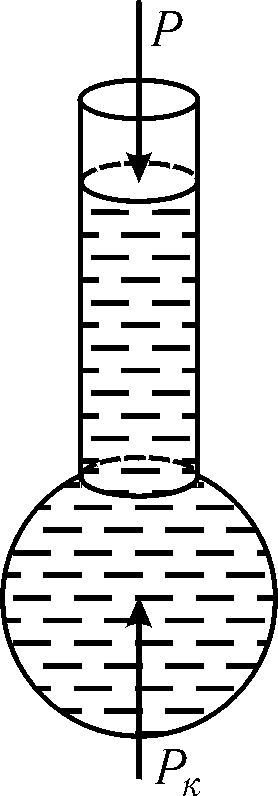
-
 ,
,(10.7)
где
![]() –
изменение площади пленки жидкости. Из
(10.7) можно дать другое определение
коэффициента поверхностного натяжения
как работы, которую совершают поверхностные
силы по изменению площади свободной
поверхности жидкости на единицу.
–
изменение площади пленки жидкости. Из
(10.7) можно дать другое определение
коэффициента поверхностного натяжения
как работы, которую совершают поверхностные
силы по изменению площади свободной
поверхности жидкости на единицу.
Если поверхность раздела искривлена, то силы поверхностного натяжения приводят к возникновению дополнительного капиллярного давления. Чтобы получить выражение для капиллярного давления, рассмотрим вертикальную трубку, заполненную жидкостью (рис. 10.10). На конце трубки образуется капля, имеющая в первом приближении сферическую форму. Жидкость в трубке находится в состоянии равновесия, поскольку гидростатическое давление компенсируется капиллярным давлением PK, возникающим под искривленной поверхность жидкости.
Чтобы увеличить объем висящей капли, необходимо совершить работу против капиллярных сил:
-
 .
.(10.8)
Эта работа будет затрачена на увеличение свободной поверхности капли
-
 .
.(10.9)
Приравнивая
(10.8) к (10.9) и учитывая, что для капли
![]() ,
а
,
а
![]() ,
получаем
,
получаем
-
 .
.(10.10)
Отметим, что капиллярное давление направлено всегда по радиусу кривизны поверхности к ее центру и может быть весьма значительным, если радиус кривизны поверхности мал.
Капиллярное давление играет значительную роль в процессах смачивания, растекания и капиллярного подъема.
Лекція 18.
Загальна характеристика фазових переходiв. Фазовий перехiд першого роду. Рiвняння Клапейрона-Клаузiуса. Фазовi переходи другого роду.
