16. Уравнение Никольского и отклонения от него.
В растворах наряду
с ионом Н+
могут находиться другие катионы. В
этом случае возможно следующее протекание
ионообменной реакции:

В результате такой
реакции активность ионов в мембране
уменьшится на некоторую величину х, а
равновесная концентрация Н+ в фазе
раствора соответственно увеличивается
на величину х, что приведет к возрастанию
потенциала электрода, согласно уравнению:
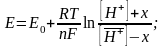
Количество вытесненных ионов зависит
от глубины протекания ионообменной
реакции, которая описывается по закону
действия масс уравнением:

Если это уравнение решить относительно
х и подставить в уравнение и сделать
допущение, что водная фаза не изменит
своего состава, а изменится концентрация
ионов водорода в фазе мембраны , т.е.
только раствор может влиять на электрод,
а не наоборот:
 - уравнение
Никольского
- уравнение
Никольского



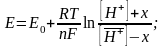

 - уравнение
Никольского
- уравнение
Никольского