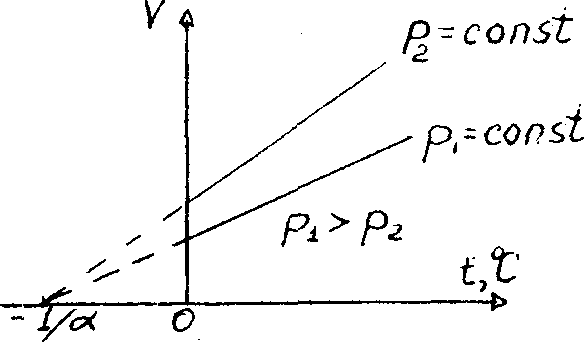- •Вопросы к экзамену для бакалавров
- •Раздел 1. Механика и молекулярная физика
- •1.2. Скорость
- •1.3. Ускорение и его составляющие
- •1.4 Угловая скорость и угловое ускорение
- •2.2. Второй закон Ньютона
- •2.3. Третий закон Ньютона
- •2.4. Силы трения
- •Сила тяжести и вес. Невесомость
- •Сила всемирного тяготения
- •2.5. Закон сохранения импульса. Центр масс
- •3.1. Энергия, работа, мощность
- •3.2. Кинетическая и потенциальная энергии
- •3.3. Закон сохранения энергии
- •4.1. Момент инерции
- •4.4. Момент импульса и закон его сохранения
- •7. Момент силы. Основной закон динамики вращательного движения. Кинетическая энергия вращательного движения.
- •4.3. Момент силы. Уравнение динамики вращательного движения твердого тела
- •4.2. Кинетическая энергия вращения
- •5.1. Гармонические колебания и их характеристики
- •5.2. Механические гармонические колебания
- •5.4. Сложение гармонических колебаний одного направления и одинаковой частоты. Биения
- •5.5. Сложение взаимно перпендикулярных колебаний
- •Основы молекулярной физики и термодинамики
- •1. Молекулярно-кинетическая теория идеального газа
- •1.1. Опытные законы идеального газа
- •1.2. Уравнение Клапейрона-Менделеев
- •1.3. Основное уравнение молекулярно-кинетической теории идеальных газов
- •Тогда давление газа, оказываемое им на стенку сосуда
- •Уравнение (1.11) с учетом (1.12) примет
- •1.4. Закон Максвелла для распределениямолекул идеального газа по скоростям
- •2.1. Число степеней свободы молекулы. Закон равномерного распределения энергиипо степеням свободы молекул
- •2.2. Первое начало термодинамики
- •2.3. Работа газа при изменении его объема
- •2.4. Теплоемкость
- •2.5. Применение первого начала термодинамики к изопроцессам
- •Тогда для произвольной массы газа получим
- •Раздел 2. Электричество. Постоянный ток. Магнетизм
- •1.2. Закон Кулона
- •1.3. Электростатическое ноле. Напряженность электростатического поля
- •1.4. Теорема Гаусса для электростатического поля
- •1.5. Применение теоремы Гаусса к расчету некоторых электростатических полей в вакууме
- •1.6. Циркуляция вектора напряженности электростатического поля
- •1.7. Потенциал электростатического поля
- •1.9. Вычисление разности потенциалов по напряженности поля
- •2.1. Электрический ток. Сила и плотность тока
- •2.3. Закон Ома. Сопротивление проводников
- •Действие магнитного поля на движущийся заряд
- •3.7. Движение заряженных частиц в магнитном поле
- •Работа по перемещению проводника и контура с током в магнитном поле
- •3.14. Закон Фарадой и его вывод из закона сохранения энергии
- •Раздел 3. Оптика и атомная физика
- •Если оптическая разность хода равна целому числу волн в вакууме
- •Если оптическая разность хода равна целому числу волн в вакууме
- •Расчет интерференционной картины от двух источников
- •Если оптическая разность хода равна целому числу волн в вакууме
- •Интерференция света в тонких пленках
- •Применение интерференции света
- •4.1. Принцип Гюйгенса-Френеля
- •4.2. Метод зон Френеля. Прямолинейное распространение света
- •Дифракция Фраунгофера на одной щели
- •Дифракция Фраунгофера на дифракционной решетке
- •Поляризация света при отражении и преломлениина границе двух диэлектриков
- •Закон Стефана-Больцмана и смещение Вина
- •Планк вывел для универсальной функции Кирхгофа формулу
- •Модели атома Томсона и Резерфорда
- •Постулаты Бора
- •7.4. Спектр атома водорода по Бору
- •Линейчатый спектр атома водорода
- •Корпускулярно-волновой дуализм свойств вещества
- •Спин электрона. Спиновое число
- •Согласно общим выводам квантовой механики, спин квантуется по закону
- •11.2. Дефект массы и энергия связи ядра
1. Молекулярно-кинетическая теория идеального газа
1.1. Опытные законы идеального газа
В молекулярно-кинетической теории пользуются идеализированной моделью идеального газа, согласно которой:
собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда;
между молекулами газа отсутствуют силы взаимодействия;
столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
Модель идеального газа можно использовать при изучении реальных газов, т.к. они в условиях, близких к нормальным (например, кислород и гелий), а также при низких давлениях и высоких температурах близки по своим свойствам к идеальному газу. Кроме того, внеся поправки, учитывающие собственный объем молекул газа и действующие молекулярные силы, можно перейти к теории реальных газов.
Опытным путем, еще до появления молекулярно-кинетической теории, был установлен целый ряд законов, описывающих поведение идеальных газов, которые мы и рассмотрим.
12. Изопроцессы. Газовые законы: закон Бойля – Мариотта, Гей – Люссака, Авогадро, Дальтона.
Закон Бойля-Мариотта: для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная: pV = const
при Т = const, m = const. (1.1)
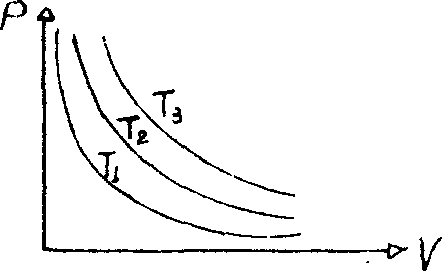
Рис. 46 |
Кривая, изображающая зависимость между величинами р и V, характеризующими свойства вещества при постоянной температуре, называется изотермой (рис 46 ).
|
Изотермы представляют собой гиперболы, расположенные на графике тем выше, чем выше температура, при которой происходит процесс.
Закон Гей–Люссака: 1) объем данной массы газа при постоянном давлении изменяется линейно с температурой:
V=V0(1+t) при p=const, m=const, (1.2) 2) давление данной массы газа при постоянном объеме изменяется линейно с температурой:
p=p0(1+t)
при
V=const, m=const. (1.3)
В
этих уравнениях t
-температура по шкале Цельсия, р0
и V0
– давление и объем при 0° С, коэффициент
= .
.
Процесс, протекающий при постоянном давлении, называется изобарным. На диаграмме в координатах V, t (рис. 47) этот процесс изображается прямой, называемой изобарой. Процесс, протекающий при постоянном объеме, называется изохорным. На диаграмме в координатах p, t (рис.48) он изображается прямой, называемой изохорой.
Рис. 47 |
Рис. 48 |
Из
(1.2) и (1.3) следует, что изобары и изохоры
пересекают ось температур в точке
![]() = -273.15°С, определяемой из условия 1+t=0.
Если сместить начало отсчета в эту
точку, то происходит переход к шкале
Кельвина (рис. 48), откуда
= -273.15°С, определяемой из условия 1+t=0.
Если сместить начало отсчета в эту
точку, то происходит переход к шкале
Кельвина (рис. 48), откуда
Т
= t
+
![]() .
.
Вводя в формулы (1.2) и (1.3) термодинамическую температуру, законам Гей-Люссака можно придать более удобный вид:

или
 (1.4)
(1.4)
при р = const, m = const ,
 при
V = const, m = const.
при
V = const, m = const.
где индексы 1 и 2 относятся к произвольным состояниям, лежащим на одной изобаре или изохоре.
Закон Авогадро: моли любых газов при одинаковой температуре и давлении занимают одинаковые объемы. При нормальных условиях этот объем равен 22,4110-3 м3/моль.
По определению в одном моле различных веществ содержится одно и то же число молекул, называемое постоянной Авогадро:
![]() .
.
Закон Дальтона: давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов, т.е.
p=р1+р2+…+рn,
где р1, р2, …рn – парциальные давления – давления, которые оказывали бы газы смеси, если бы они одни занимали объем, равный объему смеси при той же температуре.
13. Уравнение Клайперона – Менделеева.