
- •Класифікація методів очищення від сірководню
- •Хінонні методи очищення газів від сірководню
- •Процес Перокс.
- •Процес Стретфорд.
- •Процес Такахакс
- •Хінгідронний метод
- •Методи з електрохімічною регенерацією
- •Електрохімічна регенерація хінгідронного поглинального розчину
- •Вплив замісників в положенні 2 на окисно-відновний потенціал
Класифікація методів очищення від сірководню
Для вилучення сірководню із газів і перероблення його в сірку або інші сірковмісні продукти застосовують різні фізико-хімічні способи, які відрізняються природою поглинача H2S, його фізичним станом, технологічними умовами здійснення. Незважаючи на розмаїття способів, їх можна поділити на дві великі групи: сухі та мокрі.
Сухі методи полягають у поглинанні сірководню із газів твердими речовинами – сорбентами (інколи у розплавленому стані). При тому адсорбція може бути суто фізичною (сухі фізичні методи) або одночасно з адсорбцією сірководень вступає у хімічну взаємодію (сухі фізико-хімічні методи). У першій підгрупі сухих методів сорбентами є силікагель, активоване вугілля, природні і синтетичні цеоліти, оксиди та гідроксиди заліза тощо. Процес складається із стадії адсорбції H2S із газу (як правило цю стадію здійснюють за звичайних температур і підвищених тисків) і регенерації сорбента (десорбції H2S) шляхом його оброблення гарячим інертним газом, перегрітою водяною парою або підігрітою водою. При тому одержують не чистий сірководень, а його суміш з газом-десорбентом або у вигляді розчину.
У мокрих методах поглиначем сірководню є рідини, розчини або суспензії. Залежно від сутності процесів, які при тому відбуваються, ці методи поділяють на:
Фізичні;
Фізико-хімічні;
Хімічні або рідинно-окисні.
Фізичні методи очищення газів від сірководню ґрунтується на різній його розчинності у рідинах залежно від парціального тиску Н2S над ними і температури.
Фізико-хімічні методи ґрунтуються на оборотності процесів хемосорбції сірководню із газів різними хімічними речовинами або розчинами, передбачає фізичне поглинання сірководню, хімічну взаємодію його з рідким абсорбентом і подальше виділення сірководню із розчину.
Хімічні методи (рідинно-окисні) полягають у хемосорбції сірководню із газів різними розчинами лужної природи і окисненні хемосорбованого Н2S до сірки різними окисниками, які перебувають у розчиненому стані або у формі суспензії.
До відомих хімічних методів належать арсено-содовий, хінонні та ін.
Хінонні методи очищення газів від сірководню
Найбільше розповсюдження в промисловості отримали процеси Перокс, Стретфорд, Такахакс, Фумакс-Родакс і ін. [1-3].
Перевагами цих методів є:
висока селективність;
високий ступінь очищення газів від сірководню (98% і більше) в присутності СО2;
незначний вихід пари завдяки тому, що регенерація розчину здійснюється за звичайних температур;
можливість одержання товарного продукту – сірки безпосередньо в процесі очищення газу (без спеціальної установки для перероблення сірководневого газу);
сірка не містить шкідливих домішок і має високу дисперсність.
Очищення газів від сірководню хінонними методами включає три основні стадії. Перша стадія процесу – хемосорбція сірководню із газу поглинальним розчином
Na2CO3 + H2S ↔ NaHS + NaHCO3. (2.1)
На другій стадії натрій гідрогенсульфід вступає в реакцію з окисненою формою органічного каталізатора, в результаті чого відбувається виділення елементарної сірки, регенерація соди і відновлення каталізатора
N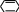
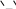 aHS+NaHCO3+
O=
=О →
Na2CO3+
HO-
-OH
+S.
(2.2)
aHS+NaHCO3+
O=
=О →
Na2CO3+
HO-
-OH
+S.
(2.2)
Третя стадія процесу включає регенерацію поглинального розчину, тобто переведення каталізатора з відновленої форми в окиснену, і відділення одержаної сірки. Регенерацію розчину здійснюють продуванням його повітрям. Під час цього відбувається флотація сірки, яка у вигляді «піни» збирається у верхній частині, а каталізатор з відновленої форми переходить в окиснену. Схематично цей процес можна представити так
C6H6O2 + 0,5O2 → C6H4O2 + H2O. (2.3)
Регенерований розчин повертається знову у процес очищення газу від сірководню. Під час процесу очищення, крім основних реакцій, відбувається побічна, яка призводить до утворення натрію тіосульфату за рівнянням
2NaHS + 2O2 → Na2S2O3 + H2O. (2.4)
З накопиченням у розчині продуктів побічних реакцій зростає густина і в’язкість розчину, в результаті чого знижується його поглинальна здатність і ефективність очищення.
Газ надходить на очищення в абсорбер, де піддається протитечійному промиванню поглинальним розчином, в результаті чого сірководень практично повністю поглинається. Утворений натрію гідрогенсульфід частково окиснюється в абсорбері хіноном з утворенням елементарної сірки. Для повного завершення цієї реакції насичений розчин із абсорбера надходить в спеціальну реакційну ємність, об’єм якої розрахований на певний час перебування розчину[1-4].
