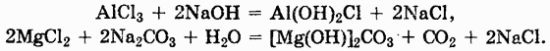- •Классификация простых и сложных веществ.
- •Кислоты
- •Номенклатура кислот.
- •Получение кислот. Бескислородные кислоты могут быть получены при непосредственном соединении неметаллов с водородом:
- •Основания (гидроксиды металлов)
- •Получение оснований. Общим методом получения оснований является реакция обмена, с помощью которой могут быть получены как нерастворимые, так и растворимые основания:
- •Химические свойства оснований.
- •Свойства основных оксидов.
- •Амфотерные оксиды обладают двойственной природой: они одновременно способны к реакциям, в которые вступают как основные, так и кислотные оксиды, т.Е. Реагируют и с кислотами, и с щелочами:
ГБОУ СПО Колледж связи №54
Самостоятельная работа по химии № 1
Тема: КЛАССИФИКАЦИЯ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ И ИХ СВОЙСТВА.
(соли, кислоты, основания, оксиды)
Выполнил работу:
Першаков Алексей
студент группы МТС 9-4
Москва
- 2013-
Классификация простых и сложных веществ.
Под классификацией понимают объединение разнообразных и многочисленных соединений в определенные группы или классы, обладающие сходными свойствами. С проблемой классификации тесно связана проблема номенклатуры, т.е. системы названий этих веществ.
Индивидуальные химические вещества принято делить на две группы: немногочисленную группу простых веществ (их, с учетом аллотропных модификаций, насчитывается около 400) и очень многочисленную группу сложных веществ.
Сложные вещества обычно делят на четыре важнейших класса: оксиды, основания (гидроксиды), кислоты, соли.
Приведенная первичная классификация является несовершенной. Например, в ней нет места для аммиака, соединений металлов с водородом, азотом, соединений неметаллов с другими неметаллами и т.д.
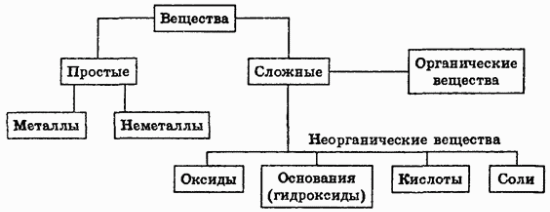
Перед тем, как рассмотреть более детально каждый из классов неорганических соединений, целесообразно взглянуть на схему, отражающую генетическую связь типичных классов соединений.
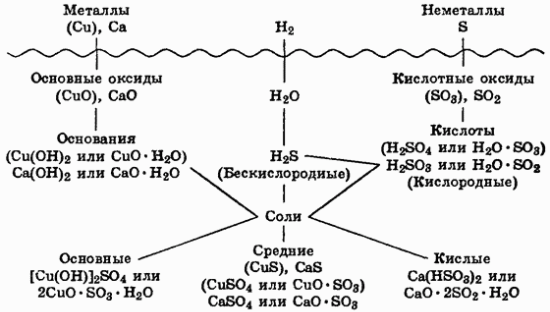
В верхней части схемы помещены две группы простых веществ — металлы и неметаллы, а также водород, строение атома которого отличается от строения атомов других элементов. На валентном слое атома водорода находится один электрон, как у щелочных металлов; в то же время, до заполнения электронного слоя оболочки ближайшего инертного газа — гелия — ему недостает также одного электрона, что роднит его с галогенами.
Волнистая черта отделяет простые вещества от сложных; она символизирует, что пересечение этой границы, т.е. любая реакция простых веществ со сложными, будет обязательно затрагивать валентные оболочки атомов в простых веществах, следовательно, любая реакция с участием простых веществ будет окислительно-восстановительной.
В левой части схемы под металлами помещены их типичные соединения — основные оксиды и основания, в правой части схемы помещены соединения, типичные для неметаллов, — кислотные оксиды и кислоты. Водород, помещенный в верхней части схемы, дает очень специфический, идеально амфотерный оксид — воду H2O, которая в комбинации с основным оксидом дает основание, а с кислотным — кислоту. Водород в сочетании с неметаллами образует бескислородные кислоты. В нижней части схемы помещены соли, которые, с одной стороны, отвечают соединению металла с неметаллом, а с другой — комбинации основного оксида с кислотным.
Приведенная схема до некоторой степени отражает и возможности протекания химических реакций — как правило, в химическое взаимодействие вступают соединения, принадлежащие к разным половинам схемы. Так, основные оксиды реагируют с кислотными оксидами, кислотами и кислыми солями; кислоты реагируют с металлами, основными оксидами, основаниями, основными и средними солями. Естественно, что такая схема не дает исчерпывающей информации обо всех возможных реакциях, однако она отражает основные типы реакций.
Соли
Соли принято делить на три группы: средние, кислые и основные. В средних солях все атомы водорода соответствующей кислоты замещены на атомы металла, в кислых солях они замещены только частично, в основных солях группы ОН соответствующего основания частично замещены на кислотные остатки.
Существуют также некоторые другие типы солей, например двойные соли, в которых содержатся два разных катиона и один анион: CaCO3*MgCO3 (доломит), KCl*NaCl (сильвинит), KAl(SO4)2 (алюмокалиевые квасцы), или смешанные соли, в которых содержится один катион и два разных аниона: CaOCL2 (или Ca(OCl)Cl)
Соли представляют собой ионные соединения, и их названия строятся по названиям катионов и анионов. Для солей бескислородных кислот к названию неметалла добавляется суффикс –ид например: хлорид натрия NaCl, сульфид железа (II) FeS и др.
При наименовании солей кислородсодержащих кислот к латинскому корню названия элемента добавляется окончание –ат для высших степеней окисления, -ит для более низких (для некоторых кислот используется приставка гипо- для низких степеней окисления неметалла; для солей хлорной и марганцовой кислот используется приставка пер-): карбонат кальция CaCO3, сульфат железа (III) Fe2(SO4)3, сульфит железа (II) FeSO3, гипохлорит калия KOCl, хлорит калия KClO2, хлорат калия KClO3, перхлорат калия KClO4, перманганат калия KMnO4, дихромат калия K2Cr2O7.
Способы получения. Соли тесно связаны со всеми остальными классами неорганических соединений и могут быть получены практически из любого класса.
Химические свойства. Многие соли устойчивы при нагревании. Однако соли аммония, а также некоторые соли малоактивных металлов, слабых кислот и кислот, в которых элементы проявляют высшие или низшие степени окисления, при нагревании разлагаются:
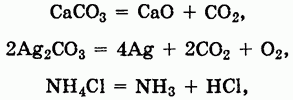
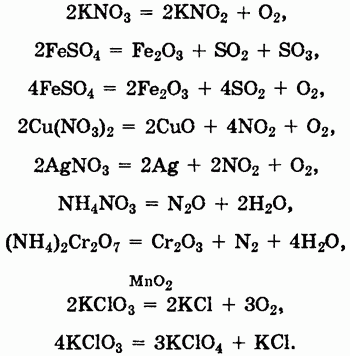
При химических реакциях солей проявляются особенности как катионов, так и анионов, входящих в их состав. Ионы металлов, находящиеся в растворах, могут вступать в реакции с другими анионами с образованием нерастворимых соединений или же в окислительно-восстановительные реакции:
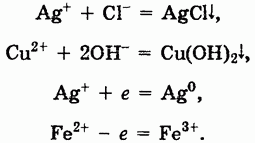
Первые две реакции показывают, что соли могут реагировать с кислотами, солями или основаниями, а вторые две указывают на окислительные и восстановительные свойства солей.
С другой стороны, анионы, входящие в состав солей, могут соединяться с катионами с образованием осадков или малодиссоциированных соединений, а также участвовать в окислительно-восстановительных реакциях:
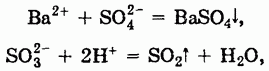
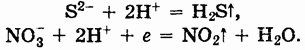
Таким образом, соли могут реагировать с солями, кислотами (по типу обмена), металлами и неметаллами.
Кислые и основные соли.
Эти соли можно рассматривать как продукт неполного превращения кислот и оснований. По международной номенклатуре атом водорода, входящий в состав кислой соли, обозначается приставкой гидро-, а группа ОН — приставкой гидрокси-: NaHS — гидросульфид натрия, NaHSO3 — гидросульфит натрия, Mg(OH)Cl — гидроксихлорид магния, Al(OH)2Cl — дигидроксихлорид алюминия.
Способы получения и свойства. Кислые соли могут быть получены либо неполной нейтрализацией кислот, либо действием избытка кислот на средние соли, щелочи, оксиды или соли:
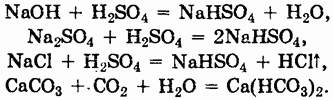
При нагревании многие кислые соли разлагаются:
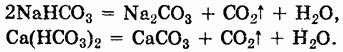
Основные соли часто получаются при осторожном добавлении небольших количеств щелочей к растворам средних солей металлов, имеющих малорастворимые основания, или при действии солей слабых кислот на средние соли: