
- •БиоОрганичесКая химИя
- •Часть I
- •060101 – «Лечебное дело»
- •Оглавление
- •Введение
- •1. Классификация и номенклатура биологически важных органических соединений
- •Вопрос 1. Как классифицируются органические соединения?
- •Вопрос 2. Какие виды номенклатуры органических соединений используются в настоящее время?
- •Вопрос 3. Как правильно назвать органическое соединение по систематической номенклатуре?
- •Вопрос 4. Какие признаки положены в основу классификации органических соединений?
- •Вопрос 5. Как правильно отнести данный углеводород
- •Вопрос 7. Как определить класс и дать название по систематической номенклатуре следующему соединению:
- •Вопрос 8. Как определить класс и дать название по систематической номенклатуре следующему соединению:
- •Вопрос 9. Как определить класс и дать название по систематической (международной) и рациональной номенклатурам следующим соединениям:
- •Вопрос 10. Как правильно написать формулу и дать название вторичного спирта, содержащего 4 атома углерода?
- •Вопрос 11. Как написать формулу и название (по международной номенклатуре) тиола, содержащего 3 атома углерода и отметить в этом соединении вторичный атом углерода?
- •Вопрос 12. Как написать формулу и название амида кислоты, содержащей 4 атома углерода?
- •Вопрос 13. Как из представленных формул выбрать те, которые изображены неправильно?
- •Вопрос 14. Как из предложенных названий:
- •Вопрос 15. Соответствует ли правилам Международной номенклатуры название 2-метил-4-бутанол?
- •2. Строение органических соединений
- •Вопрос 16. Как можно охарактеризовать понятие: строение органических соединений?
- •Вопрос 22. Что такое конфигурация молекулы?
- •Вопрос 23. Что такое конформация молекулы?
- •Вопрос 24. Что такое гомологический ряд?
- •Вопрос 25. Как написать формулу гомолога бутановой кислоты, имеющего на два атома углерода больше?
- •Вопрос 26. Как написать формулу гомолога бутаналя, имеющего на четыре атома водорода меньше?
- •Вопрос 27. Как написать формулу изомера пентановой кислоты по строению углеродной цепи?
- •Вопрос 28. Как написать формулу изомера 1-пентена по положению кратной связи?
- •Вопрос 29. Как написать формулу изомера бутаналя по функциональной группе?
- •Вопрос 31. Как определить, к какому типу изомеров относятся олеиновая и элаидиновая кислоты?
- •Вопрос 32. Как определить, к какому типу изомеров относятся соединения: бутановая кислота и метиловый эфир пропановой кислоты?
- •Вопрос 33. Как определить, к какому типу изомеров относятся соединения: 1-бутанол и 2-бутанол?
- •Вопрос 34. Как определить, являются ли изомерами лейцин и изолейцин?
- •3. Общие закономерности реакционной способности органических соединений
- •Вопрос 35. Как определить, какой тип реакций наиболее характерен для соединений, относящихся к тому или иному классу органических соединений?
- •Вопрос 36. Как по уравнению реакции определить, к какому типу химических реакций она относится?
- •Вопрос 37. Как правильно написать уравнение реакции и определить её механизм?
- •Вопрос 38. Какой продукт преимущественно образуется в результате реакции бромирования 3-метилпентана?
- •Вопрос 39. Назовите продукт взаимодействия 2-бутеновой кислоты с бромоводородом в присутствии перекиси и без неё.
- •Вопрос 40. В процессе метаболизма в живых организмах фумаровая кислота превращается в яблочную. Каким путем можно получить яблочную кислоту из фумаровой in vitro?
- •Вопрос 41. R-2-бромбутан может реагировать с водным раствором гидроксида натрия по механизмам sn1 и sn2. Опишите стереохимический результат реакции в каждом случае.
- •Вопрос 44. Каков внешний эффект взаимодействия олеата натрия с бромной водой?
- •4. Аминокислоты, пептиды, белки
- •Вопрос 45. Какие соединения относятся к - аминокислотам? Какова роль -аминокислот в функционировании живых организмов?
- •Вопрос 46. Как построить формулы стереоизомеров (энантиомеров) -аминокислот? Все ли природные -аминокислоты оптически активны?
- •Вопрос 47. Как проявляются кислотно-основные свойства и амфотерность -аминокислот? Какие свойства -аминокислот обуславливает их ионное строение?
- •Вопрос 48. Как определить, какую реакцию среды имеют растворы -аминокислот в дистиллированной воде?
- •Вопрос 49. Что такое «изоэлектрическая точка - аминокислоты»? Каким образом - аминокислоты перемещаются в электрическом поле?
- •Вопрос 51. С помощью какой реакции можно превратить изолейцин в 3-метил-2-пентеновую кислоту? а серин в 2- аминоэтанол?
- •Вопрос 53. Какие соединения образуются при взаимодействии в организме валина и пировиноградной кислоты?
- •Вопрос 54. Что представляют собой пептиды? в чём состоит их отличие от белков? в результате каких реакций образуются пептиды в организме?
- •Вопрос 56. Охарактеризуйте первичную, вторичную, третичную и четвертичную структуры белков.
- •Вопрос 57. Как классифицируются белки?
- •Вопрос 58. Какие качественные реакции используют для определения аминокислот и белков?
- •Вопрос 59. Можно ли с помощью ксантопротеиновой реакции (с азотной кислотой) отличить фенилаланин от тирозина? Если да, то в чем будет состоять различие? Если нет, объясните, почему.
- •Литература
Вопрос 44. Каков внешний эффект взаимодействия олеата натрия с бромной водой?
Ответ. Рассмотрим строение субстрата в данной реакции. Олеат натрия – это натриевая соль олеиновой кислоты. Олеиновая кислота относится к высшим непредельным кислотам. Бромная вода – это раствор брома в воде. Бром представляет собой жидкость коричневого цвета, бромная вода поэтому окрашена, возможные оттенки – от коричневого до светло-жёлтого в зависимости от концентрации. Во взаимодействие с бромом вступает двойная связь в радикале олеиновой кислоты:
СН3(СН2)7СН=СН(СН2)7СООН + Br2
СН3(СН2)7СНBr–СНBr(СН2)7СООН
В результате реакции концентрация брома в бромной воде снижается и бромная вода становится светлее или совсем обесцвечивается. Обесцвечивание бромной воды является внешним эффектом качественной реакции на непредельные соединения.
4. Аминокислоты, пептиды, белки
Вопрос 45. Какие соединения относятся к - аминокислотам? Какова роль -аминокислот в функционировании живых организмов?
Ответ. -Аминокислоты – гетерофункциональные соединения, молекулы которых содержат две функциональные группы: карбоксильную группу (–СООН) и аминогруппу (–NH2), причём обе группы связаны с одним и тем же атомом углерода. Называют -аминокислоты по Международной номенклатуре, при этом атом углерода, с которым связана аминогруппа имеет второй порядковый номер. Для многих - аминокислот, особенно тех, которые входят в состав белков, чаще используются названия по тривиальной номенклатуре.
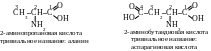
М ногочисленные
пептиды и белки, присутствующие в живых
организмах, построены из остатков
двадцати -аминокислот.
Молекулы всех -аминокислот
содержат один и тот же фрагмент, группу
H2N–СН–СООН,
второй атом углерода в котором связан
с углеводородным радикалом –R.
Углеводородный радикал может иметь
различную химическую природу.
ногочисленные
пептиды и белки, присутствующие в живых
организмах, построены из остатков
двадцати -аминокислот.
Молекулы всех -аминокислот
содержат один и тот же фрагмент, группу
H2N–СН–СООН,
второй атом углерода в котором связан
с углеводородным радикалом –R.
Углеводородный радикал может иметь
различную химическую природу.
Современная рациональная классификация аминокислот основана на полярности радикалов, т.е. способности их к взаимодействию с водой при физиологических значениях рН (близких к рН 7,0). Различают аминокислоты, содержащие следующие радикалы: 1) неполярные (гидрофобные); 2) полярные (гидрофильные); 3) ароматические; 4) отрицательно заряженные и 5) положительно заряженные. Ниже приведены структурные формулы аминокислот, их названия по тривиальной номенклатуре, сокращенные английские и русские обозначения и однобуквенные символы, принятые в зарубежной и отечественной литературе.

-Аминокислоты в обычных условиях представляют собой бесцветные кристаллические вещества, растворимые в воде.
Синтез белка в организме возможен только в том случае, если присутствуют все 20 -аминокислот. Основным источником -аминокислот для живого организма служат пищевые белки. Некоторые -аминокислоты могут синтезироваться в организме (из других аминокислот или иных продуктов метаболизма), но часть -аминокислот в организме человека не синтезируются и могут поступать только с пищей, поэтому так важно сбалансированное разнообразное белковое питание человека. Такие -аминокислоты называют незаменимыми: валин, лейцин, изолейцин, лизин, треонин, метионин, фенилаланин, триптофан).
При некоторых заболеваниях заменимые аминокислоты могут перейти в разряд незаменимых. Например, при фенилкетонурии организм перестаёт синтезировать аминокислоту тирозин.
Многие -аминокислоты используются в медицине. Так, глицин улучшает обменные процессы в тканях мозга и мышц. Глутаминовая кислота применяется при лечении заболеваний центральной нервной системы, метионин и гистидин для лечения заболеваний печени и т.д.
