
- •Інструкція з охорони праці в лабораторії хімічного аналізу
- •У разі нещасного випадку негайно звертайтеся до викладача !
- •Практична робота
- •Вимоги щодо виконання практичної роботи
- •Приклад оформлення письмового звіту
- •Завдання до практичної роботи
- •Хід роботи
- •Хід роботи
- •Хід роботи
- •Хід роботи
- •Тема 1. Відбір і підготовка проб для аналізу Практична робота
- •Вимоги щодо виконання практичної роботи
- •Завдання до практичної роботи
- •Хід роботи
- •Тема 2. Хімічні реактиви Практична робота
- •Вимоги щодо виконання практичної роботи
- •Інструкція з охорони праці
- •Завдання до практичної роботи
- •Хід роботи
- •Хід роботи
- •Тема 3. Зважування Практична робота
- •Вимоги щодо виконання практичної роботи
- •Завдання до практичної роботи
- •Хід роботи
- •Вихідні та дослідні дані
- •Обчислення
- •Тема 4. Хімічний посуд та допоміжне приладдя Практична робота
- •Вимоги щодо виконання практичної роботи
- •Інструкція з охорони праці
- •Завдання до практичної роботи
- •Хід роботи
- •2.1. Перевірка ємності піпетки на … мл Хід роботи
- •Вихідні та дослідні дані
- •Обчислення
- •2.2. Перевірка ємності мірної колби на … мл Хід роботи
- •Вихідні та дослідні дані
- •Обчислення
- •2.3. Калібровка бюретки Хід роботи
- •Вихідні та дослідні дані
- •Обчислення
- •Хід роботи
- •Хід роботи
- •Тема 5. Методи очищення речовин Практична робота
- •Вимоги щодо виконання практичної роботи
- •Інструкція з охорони праці
- •Завдання до практичної роботи
- •Хід роботи
- •Хід роботи
- •Хід роботи
- •Хід роботи
- •Хід роботи
- •Вихідні та дослідні дані
- •Обчислення
- •Хід роботи
- •Тема 6. Обробка осадів Практична робота
- •Вимоги щодо виконання практичної роботи
- •Інструкція з охорони праці
- •Завдання до практичної роботи
- •Хід роботи
- •Вихідні та дослідні дані
- •Обчислення
- •Хід роботи
- •Тема 7. Розчини в об’ємному аналізі Практична робота
- •Вимоги щодо виконання практичної роботи
- •1. Як приготувати 250 мл 0,1 н. Розчину перекристалізованої чистої двоводної щавлевої кислоти (н2с2о4 ˑ 2н2о), яку використовують для титрування лугу? Яку наважку її треба узяти?
- •2. Як приготувати 200 мл 0,05 н. Розчину кМnO4 для титрування методом перманганатометрії?
- •3. Приготувати 1 л 0,2 н. Розчину нСl, використовуючи наявну в лабораторії концентровану нСl з густиною 1,15.
- •Хід роботи
- •Вихідні та дослідні дані
- •Обчислення
- •Хід роботи
- •Вихідні та дослідні дані
- •Обчислення
- •Вихідні та дослідні дані
- •Обчислення
- •4. Перелік навчально-методичної літератури
- •1. Основна
- •2. Додаткова
Хід роботи
Дослід слід проводити у витяжній шафі.
1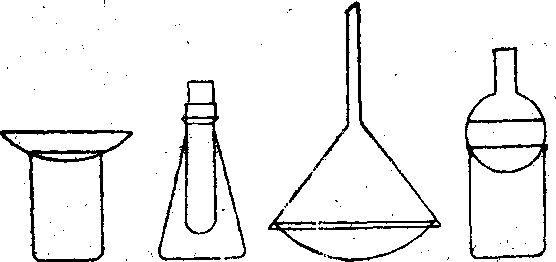 .
Для
сублімації можна скористатися одним
із приладів, що зображені на рис. 6. Ми
розглянемо прилад, що складається із
хімічного стакана і круглодонної колби.
.
Для
сублімації можна скористатися одним
із приладів, що зображені на рис. 6. Ми
розглянемо прилад, що складається із
хімічного стакана і круглодонної колби.
2. На техно-хімічних вагах зважити близько 0,3 г кристалічного йоду і помістити в стакан, який поставити на піщану баню. Стакан закрити круглодонною колбою з холодною водою. Рис. 6.
3. Обережно нагріти піщану баню, щоб пари йоду не виходили на зовні, а осідали на холодну поверхню колби.
4. Коли сублімація закінчиться, вимкнути газ на піщаній бані і після повного охолодження зняти колбу із стакана і звернути увагу на отримані кристали йоду.
5. Обережно, сухим фільтрувальним папером зняти з колби йод у чистий сухий бюкс з притертою кришкою.
6. Зробити рисунок приладу, що застосовувався для сублімації. Відмітити колір парів, колір і форму кристалів сублімованого йоду. Записати особливості процесу сублімації.
Завдання 5. Перекристалізація натрій хлориду (метод висолювання)
При перекристалізації речовин, розчинність яких мало змінюється із зміною температури, застосовують метод висолювання. До розчинів таких речовин додають речовини, що знижують розчинність.
Хід роботи
1. Приготувати насичений розчин натрій хлориду NaCl. Для цього, у попередньо зваженому алюмінієвому бюксі відважити на аналітичних вагах близько 10 г кухонної солі з точністю до 0,01 г.
2. Розтерти наважку солі в ступці і висипати у хімічний стакан.
3. Додати 25 мл дистильованої води, поставити стакан на азбестовану сітку і нагріти розчин до кипіння.
4. Профільтрувати гарячий розчин через складчастий фільтр у чистий стакан.
5. Відміряти мензуркою 10 мл концентрованої хлоридної кислоти (густина 1,19 г/см3).
6. Стакан із теплим насиченим розчином кухонної солі перенести у витяжну шафу і повільно невеликими порціями додавати в нього концентровану хлоридну кислоту при безперервному помішуванні скляною паличкою.
4. Охолодити розчин до кімнатної температури.
5. Відфільтрувати через складчастий паперовий фільтр кристали, що випали.
6. Лійку з фільтром і кристалами солі помістити у сушильну шафу і висушити при температурі 110° С.
7. Вийняти лійку з фільтром із сушильної шафи і залишити на деякий час у штативі для охолодження.
8. Зважити фільтр із перекристалізованим натрій хлоридом на аналітичних вагах.
9. З фільтра скляною паличкою ретельно видалити кристалики солі в окремий бюкс, а сам фільтр знову зважити на аналітичних вагах.
10. Обчислити вихід продукту – перекристалізованого натрій хлориду.
Вихідні та дослідні дані
m(бюксу) –
m(бюксу з наважкою NaCl) –
m(наважки NaCl) = m(бюксу з наважкою NaCl) – m(бюксу) =
m(фільтру) –
m(перекристалізованого NaCl) = m(фільтру з перекристалізованим NaCl) – m(фільтру) =
Обчислення
Відносний вихід перекристалізованого натрій хлориду (η) обчислюють за формулою:
η
=
![]() 100%.
100%.
Висновок: (Який відносний вихід перекристалізованого натрій хлориду? Яка роль концентрованої хлоридної кислоти у процесі перекристалізації?)
Завдання 6. Добування газу СО2 в апараті Кіппа. Очищення газу
