
- •6.051701 “Харчова технологія та інженерія”
- •Київ нухт 2012
- •Лабораторна робота №1 природні вуглеводи – носії солодкого смаку. Синтетичні підсолоджувачі
- •Якісне визначення сахарину в напоях
- •1.2. Кількісне визначення сахарину в напоях
- •1.3. Фотометричний метод визначення аспартама
- •Робочі розчини аспартама для побудови калібрувального графіка
- •1.3. Поляриметричний метод визначення фруктози
- •1.4. Резорциновий метод визначення кетоз
- •Лабораторна робота №2 визначення природи барвника та вмісту речовин, що корегують колір у харчових продуктах.
- •2.1. Експрес-метод визначення природи барвника
- •2.2. Експрес-ідентифікація штучних барвників
- •2.3. Визначення сірчистої кислоти в кондитерських виробах (гост 26 811-86) Хід визначення
- •2.4. Визначення вмісту сірчистої кислоти в соках Хід визначення
- •2.5. Визначення вмісту нітриту натрію у ковбасних виробах
- •Хід визначення
- •Лабораторна робота №3 консерванти у харчових технологіях
- •3.1. Визначення вмісту сірчистої кислоти в мармеладі, пастильних виробах, карамелі з фруктовими начинками та цукерках з плодово-ягідними корпусами. Хід визначення
- •3.2. Визначення вмісту бензойної кислоти в харчових продуктах
- •Хід визначення
- •3.3. Визначення наявності мінеральних кислот у рослинному маслі (маринаді консервів) Хід визначення
- •3.4 Визначення масової частки хлориду натрію у ковбасних виробах
- •Хід визначення
- •3.5 Визначення наявності хлориду натрію у твердих сирах, бринзі методом з азотнокислим сріблом.
- •3.6 Визначення хлориду натрію в твердому сирі
- •Лабораторна робота №4 регулятори рН середовища харчових систем
- •4.1. Визначення вмісту оцтової кислоти при визначенні міцності препарату Хід визначення
- •4.2. Визначення вмісту оцтової кислоти в маринованій рибі Хід визначення
- •4.3. Визначення вмісту лимонної та яблучної кислот у рослинній сировині при застосуванні трилону б.
- •4.4. Визначення молочної кислоти в хлібі та заквасці Хід визначення
- •Лабораторна робота № 5. Роль емульгаторів, піноутворювачів та стабілізаторів у виробництві продуктів харчування.
- •5.1. Одержання харчової емульсії ( майонезу )
- •5.2. Одержання харчової піни (зефір )
- •5.3. Вивчення властивостей основних поверхнево активних речовин у виготовленні харчових продуктів.
- •5.3.1. Визначення желюючої здатності желатини у залежності від рН середовища Хід роботи
- •5.3.2. Приготування мармеладу Хід роботи
- •Лабораторна робота №6 визначення кінетичних властивостей ферменту амілази
- •6.1. Визначення гідролітичної активності амілази рослинних тканин
- •Колориметричний метод визначення активності α- та β- амілази.
- •6.3. Визначення константи Міхаеліса
- •6.4. Визначення типу інгібірування
- •6.3. Визначення оптимуму температури і рН ферментативного каталізу
- •Лабораторна робота №7 кількісне визначення амінокислот
- •7.1. Кількісне та якісне визначення амінокислот методом розподільної хроматографії на папері
- •7.1.1. Якісне визначення амінокислот
- •7.1.2. Кількісне визначення амінокислот
- •7.2. Метод формольного титрування
- •7.3. Визначення амінного азоту мідним способом
- •7.3. Визначення аміногрупи за реакцією з нінгідрином (метод Лі та Такахамі)
- •Лабораторна робота №8 білки. Отримання та аналіз білків тваринного і ролинного походження
- •8.1. Отримання кристалічного яєчного альбуміну
- •8.2. Виділення казеїну з молока і визначення його властивостей
- •8.4 Визначення розчинного білка за Лоурі та спектрофотометричним методом
Робочі розчини аспартама для побудови калібрувального графіка
Найменування параметра |
Номер пробірки |
||||||||
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
Об'єм базового розчину аспартама, см3 |
2,0 |
2,5 |
3,0 |
3,5 |
4,0 |
4,5 |
5,0 |
5,5 |
- |
Об'єм дистильованої води, см3 |
8,0 |
7,5 |
7,0 |
6,5 |
6,0 |
5,5 |
5,0 |
4,5 |
10,0 |
Концентрація ааспартама в робочих, мг/ см3 |
4,0 |
5,0 |
6,0 |
7,0 |
8,0 |
9,0 |
10,0 |
11,0 |
- |
Робочі розчини готують у пробірках об'ємом 15 см3, відмірюючи необхідні обєми базового розчину та дистильованої води піпетками (9 пробірок). Для побудови калібрувального графіка із пробірок з робочими розчинами піпеткою відбирають по 6 см3 розчину й поміщають у пробірки об'ємом 10 см3. Потім до них додають 3 см3 нінгідринового розчину й витримують 16 хв. в киплячій бані протягом 20 хв. Далі пробірки охолоджують до 20°С, після чого з кожної пробірки переносять по 3 см3 розчину, додають по 5 см3 60% етилового спирту та колориметрують.
Оптичну густину розчинів визначають на ФЕК при довжині хвилі 582 нм (фільтр №6) в кюветі з довжиною граней мм. Контрольним розчином слугує розчин пробірки №9 (нульовий розчин) та 60%-ного етилового спирту, змішаних в такій же кількості, як і в інших пробах.
Калібрувальний графік будують на міліметровому папері, відкладаючи по осі абсцис вміст аспартама, а по осі ординат величину оптичної густини.
Із досліджуваного зразка напою при температурі не вище 20°С видаляють вуглекислий газ і фільтрують через фільтр із розміром пор не більше 0,5 мкм.
До мірної колби місткістю 100 см3 піпеткою вносять 20 см3 фільтрату й доводять дистильованою водою до риски.
У пробірки місткістю 10 см3 переносять по 6 см3 кожного розчиненого зразка і до них додають по 3 см3 нінгідринового реактиву. Пробірки витримують 10 хв у киплячій водяній бані, потім протягом 20 хв охолоджують до 20°С, після чого з кожної пробірки в окрему пробірку переносять по 3 см3 розчину та додають по 5 см3 60% розчину етилового спирту.
Оптичну густину розчинів досліджуваних зразків визначають у порівнянні з нулевою пробою на ФЕК при довжині хвилі 582 нм (фільтр №6).
Вміст аспартаму визначають за оптичною густиною зразків, інтерполюючи за калібрувальним графіком.
Концентрацію аспартаму в напої визначають за формулою:
С=СР
х
К, (1.1)![]()
де Ср – концентрація аспартама в розчинених зразках, мг/100 см3;
С – концентрація аспартама в напої, мг/100 см3;
К – ступінь розчинення, що дорівнює 5.
Підрахунок проводять до другого знаку. За результат беруть середнє арифметичне двох паралельних визначень і виражають цілим числом із одним десятковим знаком.
1.3. Поляриметричний метод визначення фруктози
В основу методу визначення фруктози покладено властивість її розчинів відхиляти промінь поляризованого світла, на відміну від розчинів глюкози та сахарози, не вправо, а вліво.
Хід визначення
Для визначення вмісту фруктози в кристалічному продукті беруть наважку масою 5 г або 8 г високофруктозного сиропу. Дослідні зразки зважують у нейзильберовій чашці на технічних терезах і, розчиняючи у дистильованій, кількісно переводять у мірну колбу об'ємом 100 см3. Доводять об'єм розчину до риски і фільтрують. Фільтрат заливають у поляриметричну трубку (l = 200 мм) з кожухом. Трубку під'єднують до термостату і встановлюють у фільтраті температуру 20 оС.
Після досягнення в фільтраті заданої температури приступають до знімання показів поляриметра (П).За кінцевий результат приймають середнє значення трьох паралельних вимірювань поляризації. Після цього в досліджуваному розчині за допомогою рефрактометра вимірюють вміст сухих речовин (СР).
Вміст фруктози, тобто доброякісність продукту за фруктозою, визначають за формулою (1.2):
![]() ,% (1.2)
,% (1.2)
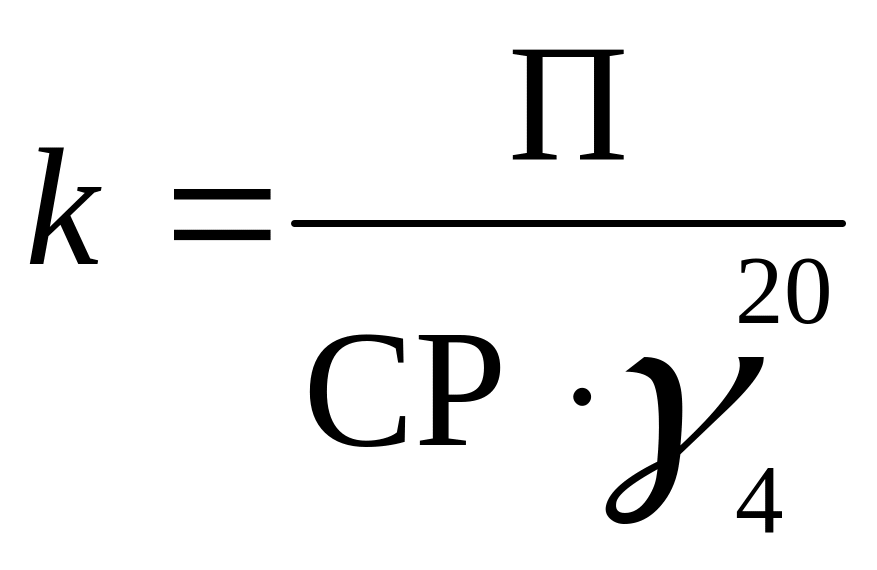 , (1.3)
, (1.3)
де П – покази поляриметра;
СР – сухі речовини фільтрату;
g – фактор обертання глюкози (дані додаток 1);
f – фактор обертання фруктози (дані додаток 1);
γ420 – питома вага фруктозних розчинів (дані додаток 1).
