
- •Поняття вищої біології у школі.
- •3. Факультативи, індивідуальні факультативи. Поглиблене вивчення хімії.
- •4. Іонні рівняння.
- •2. Поурочне планування по темі:Птахи
- •3.Поглиблене вивчення хімії. Факультативні заняття. Види факультативів
- •1. Проблемне навчання хімії, його застосування при вивчення органічної хімії
- •2. Методика проведення порівняльної характеристики підгрупи лужних металів Пояснити, чому літій розпочинає електрохімічний ряд напруг.
- •1.Екологічне виховання.
- •2.Комбінований урок
- •Зміст і структура програми з хімії.
- •4.Окисно – відновні реакції
- •1. Масова робота учнів з біології в школі.
- •2.Біологічні диктанти. Складіть текст біологічного диктанту з теми :. Екосистем
- •4. Взаємодія металів з нітратною кислотою.
- •4. Методика вивчення особливостей взаємодії нітратної кислоти з металами. Написати рівняння можливих реакцій взаємодії міді з нітратною кислотою різної концентрації.
- •1. Нетрадиційні уроки
- •2. Організація самостійної роботи учнів з біології
- •3. Основні дидактичні принципи навчання хімії
- •4. Формування понять гомології та ізомерії в шкільному курсі органічної хімії. Методичний прийом складання формул ізомерів
- •2. Ізомери відрізняються будовою вуглецевого скелету молекул
- •1.Розкрийте особливості викладання біології в середніх загальноосвітніх закладах на сучасному етапі.
- •Навчально-методична робота вчителя. Шкільне планування.
- •4.Методика розв’язування задач на виведення молекулярної формули речовини за масовими частками елементів.
- •Самостійна робота зпідручником. Розробіть завдання для роботи з текстом підручника по вибраній вами темі.
- •Методика використання комп’ютерних технологій при вивченні шкільного курсу хімії.
- •1. Масова позакласна робота з біології в школі.
- •2. Тематичне оцінювання з біології
- •4. Електронна природа хімічних зв’язків в органічних сполуках, гібридизація.
- •Методичні особливості вивчення органічної хімії на прикладі одного класу сполук
- •3. Інтерактивні методи навчання у біології (теор)
- •4.Тематичне оцінювання з біології
- •1. Біологічний кабінет
- •3.Методи дослідження, що використовуються в мвх. Нові педагогічні технологі
- •1. Генетичний зв'язок між вуглеводами,спиртами і альдегідами
- •3. Урок узагальнення і систематизація знань.
- •4. Усна перевірка учнів з біології.
- •Позаурочна робота з біології як обов'язкова
- •2. Дидактичний матеріал з біології. Розробіть дидактичну картку для перевірки знань учнів по темі «Пластичний обмін», «Біосинтез білка».
- •3. Роль хімічної мови в процесі навчання хімії. Обсяг і зміст мовних знань та вмінь у шкільному курсі хімії. Систематична хімічна термінологія та номенклатура
- •4. Методика вивчення хімічних властивостей бензену
- •1.Галогенування
- •2.Нітрування
- •1. Організація території та дослідницької роботи учнів на шкільній ділянці.(29)
- •2. Обґрунтуйте важливість такого етапу уроку як актуалізація опорних знань та чуттєвого досвіду. Запропонуйте свій варіант проведення цього етапу уроку.(23)
- •4. Електронна природа хімічних зв’язків в органічних сполуках, гібридизація.
- •5. Методика вивчення хімічних властивостей бензену
- •1.Галогенування
- •2.Нітрування
- •Вивчення національних традицій та елементів народознавства на уроках біології.
- •Лабораторні та практичні роботи з біології, методика їх проведення на прикладі конкретної
- •Урок – основна форма організації навчання хімії. Вимоги до уроку з хімії. Типи уроків з хімії.
- •Урок засвоєння нових знань і набуття нових вмінь.
- •Структура комбінованого уроку. Запропонувати тему.
- •2. Трудове виховання.
- •3..Розвиток початкових хімічних понять у вивченні теми: « Оксиген. Кисень. Оксиди. Окиснення. Горіння». Системний підхід до вивчення теми.
- •4.Експериментальна перевірка знань. Як за допомогою одного реактиву можна визначити де є спирт, альдегід та глюкоза.
- •1.Екологічне виховання при вивченні біології в школі.(3)
- •2.Аналіз шкільного підручника для 7 класу.(3)
- •1. Аналіз тексту
- •2.Аналіз методичного апарату
- •3.Організаційні форми навчальної роботи з хімії (22)
- •4.Методика складання та розв»язування розрахункових задач за хім. Рівнянням (45)
- •Зміст і структура біологічної освіти у школі.
- •2. Роль наочності при викладанні в школі. Порівняльна характеристика прокаріот та еукаріот.
- •3.Методи контролю знань.
- •Сутність, функції, види контролю при викладанні біології.
- •Характеристика підручника з біології за 8 клас.
- •Словесно-навчальні методи
- •Формування системи понять про хімічні реакції. Класифікація хімічних реакцій
- •Методи письмового контролю
- •2. Нестандартний урок
- •3. Предмет і завдання методики викладання хімії
- •4. Формулювання поняття про валентність елементів. Алгоритм визначення валентності елементів за формулою
- •1.Методи навчання та їх класифікація.(10)
- •2. Навчально – виховні завдання вивчення біології в школі. Сформулюйте завдання уроку вибраної вами теми (1)
- •4. Зв’язок методики викладання хімії з методологією хімічної науки, педагогікою, психологією та іншими науками.
- •1. Екскурсії з біології. Їх значення та методика проведення.
- •3. Матеріальна база навчання біології
- •4. Прості і складні речовини.
- •Предмет,методи і завдання мвб.
- •Практичні і лабораторні роботи.
- •Карбонатна кислота.
- •Визначте масову частку Na і Na2o.
- •Моль. Стала Авогадро. Маса та об’єм аміаку.
- •3. Державні нормативні документи, що відображають зміст хімічної осівти.
- •4.Характеристика хімічних елементів малих періодів за їх місцем у періодичній системі та будовою електронних оболонок атомів (р, n)
- •1. Поняття та їх роль у формуванні біологічних знань. Загальнобіологічні та спеціальнобіологічні поняття. Формування і розвиток біологічних понять при виченні біології.
- •2.Досліди на уроках біології. Методика їх демонстрування. Запропонуйте методичну розробку доліду по вибраній темі з біології.
- •3.Загальнологічні методи пізнання хімії. Використання прийомів логіки при вивченн інеорганічної хімії.
- •4.Особливості вивчення механізму електролітичної дисоціації йоних, ковалентних, полярних сполук
- •1. Екскурсії, їх значення, та методика викладання
- •1. Аналіз шкільного підручника для 10 кл.
- •2. Методи навчання хімії, що застосовуються у процесі удосконалення знань
- •1.Навчально – наочні посібники з біології та їх використання на уроках.(13)
- •2.Формування пізнавального інтересу учнів до біології на прикладі конкретної теми
- •4.Процес навчання хімії, його основні компоненти і засоби
- •2. Методи організації та здійснення навчально-пізнавальної діяльності.
- •4. Періодичний закон д. І. Менделєєва
- •1.Навчально – наочні посібники з біології та їх використання на уроках.(13)
- •2.Формування пізнавального інтересу учнів до біології на прикладі конкретної теми
- •4.Процес навчання хімії, його основні компоненти і засоби
4. Формування понять гомології та ізомерії в шкільному курсі органічної хімії. Методичний прийом складання формул ізомерів
Ізомерія та гомологія органічних сполук
Ізомерія. Хімікам давно відомі речовини, що мають однаковий склад, але рі-зні властивості. Такі речовини отримали назву ізомерів, тобто речовин, які скла-даються з однакових частин. Пояснения причин ізомерії було дуже важким за-вданням, що стояло перед вченими більш 30 років. Тільки Бутлерову вдалось впе-рше пояснити це явище. Відповідно його теорії, хімічні властивості речовин визна-
чаються їх складом та будовою. Різницю у властивостях двох або більше органіч-них речовин, що мають однаковий склад, можна пояснити різницею в їх хімічній будові. Таке геніально просте вирішення проблеми ізомерії намічене Бутлеровим ще в 1862 році в статті "Про різні пояснения деяких випадків ізомерії".
На основі праць Бутлерова стало можливим систематичне і вичерпне виве-дення структурних формул органічних сполук, що відповідають емпіричній формуле Схема таких висновків, що базується на поняттях хімічної будови молекул і валентное^ елементів, була дана Бутлеровим в 1864 році. Застосовуючи цю схему, він прийшов до висновку про існування трьох ізомерних пентанів:
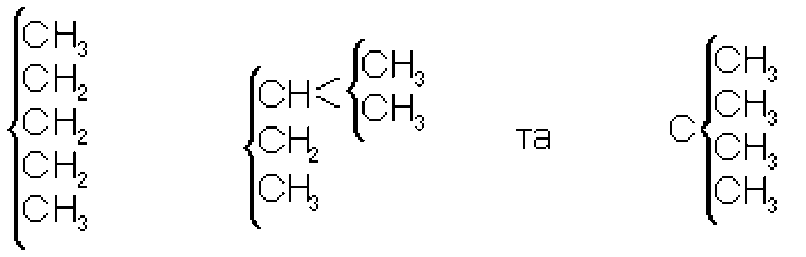
Виведення формул теоретично можливих ізомерів допомогло визначити бу-дову багатьох вже відомих сполук, а в ряді випадків виявити тотожність речовин, о вважались раніше різними; він полегшив планомірний синтез органічних сполук і, що особливо важливо, дозволив виявити факти, які суперечать теорії і призво-дять до її подальшого розвитку.
Серед органічних сполук зустрічаються такі основні класи ізомерії. 1. Вуглецевий скелет ізомерів однаковий.
А. Однакова і функціональна трупа, але вона знаходиться в різних положениях молекули, що спостерігається, наприклад, для гліцеринового альдегіду та діо-ксіацетону:

В. Різна функціональна трупа ізомерів, як це видно при порівнянні оцтової ки-слоти та гліколевого альдегіду:

2. Ізомери відрізняються будовою вуглецевого скелету молекул
А. Ізомери мають спільне вуглецеве ядро:



Ізомерія — одна з причин різноманітності та численності органічних сполук.

Гомологія органічних сполук, або закон гомологів, полягає в тому, що речовини однієї хімічної функції і однакової будови, що відрізняються один від одного за своїм атомного складом лише на nCH2, виявляються зведеними і в усьому своєму іншому хім.характері, а відмінність їх фізичних властивостей зростає або взагалі змінюється правильно в міру збільшення різниці у складі, що визначається числом n груп СН2. Такі хім. подібні сполуки утворюють так зв.гомологічний ряд, атомний складу всіх членів якого можливо висловити загальною формулою залежно від складу першого члена ряду і числа атомів вуглецю; напр.ряд граничних вуглеводнів виражається формулою СnH2n +2, ряд олефінів СnH2n, ряд ацетилену СnH2n-2, ряд бензолу СnH2n-1, ряд граничних одноатомних спиртів СnH2n +2 O, амінів СnH2n +3 N, нітрилів CnH2n-1N, альдегідів CnH2nO, одноосновних кислот СnH2nО2, двоосновних кислот CnH2n-2O4 і т. п.Для прикладу наведемо кілька членів ряду граничних вуглеводнів: метан СН4, етан C2H6, пропан С3Н8, бутан С4Н10, пентан С5H12, гексан C6H14 і т. д.Подібність між членами (гомологами) кожного ряду таке, що, знаючи властивості і перетворення одного, можна наперед знати властивості та перетворення і всіх інших членів цього ряду.З іншого боку, якщо маємо гомологічний ряд, в якому бракує деяких проміжних членів,то на підставі правильності зміни фізичних властивостей при послідовному переході від нижчих членів ряду до вищим є можливість з точністю передбачити всі властивості цих відсутніх і ще невідомих членів.Звідси - важливість закону гомологів, бо він не тільки узагальнює склад з'єднань, дозволяючи зображувати ряди їх загальними формулами, але і їх властивості і приводить їх у закономірну залежність від складу.Всі члени гомологічних рядів виробляються від найпростішого за складом через послідовне заміщення водню в ньому гуртом СН3 (метил) і не тільки чисельно, але й фактично, на досвіді, можуть бути отримані з нього таким шляхом, чим встановлюється генетичний зв'язок між усіма членами одного Г.ряду. Фізичні властивості в рядах гомологів змінюються таким чином, що здебільшого питомі ваги і обсяги, температури кипіння і плавлення, теплоти горіння і освіти, еквіваленти променезаломлення і пр. зростають поступово від члена до члена, у міру збільшення числа атомів вуглецю;іноді відбувається і зворотне, приклади чого представляються у зменшенні питомих ваг бензольних вуглеводнів, граничних одноосновних кислот і ін зі збільшенням числа атомів С;іноді, нарешті, властивість змінюється так, що для перших членів ряду величина його падає, а потім знову зростає, як це спостерігається для питомої ваги граничних одноатомних спиртів або для температури плавлення нормальних граничних одноосновних кислот,де вплив складу видається ще більш складним.Часто перший член ряду представляє відступ від загальної правильності. Так, гомологічних різниця температури кипіння граничних спиртів взагалі наближається до 19 °, дуже повільно зменшуючись зі збільшенням С, а різниця між температурою кипіння СН4O і C2H6O дорівнює 14 °;то ж являє питома вага бензолу, занадто великий порівняно з іншими членами його ряду.Так як в міру ускладнення частинок внаслідок введення метильних груп на місце водню гомологічних різниця складу СН2, залишаючись постійною, все менш і менш відбивається на процентний склад,то й величина зміни фізичних властивостей між двома сусідніми членами (гомологічних різниця їх властивостей) стає все меншою і меншою при переході від нижчих гомологів до вищих;тому при графічному зображенні зміни фізичних властивостей в залежності від складу за допомогою прямокутної системи координат, завдаючи склад по осі абсцис, а властивості по осі ординат, виходять здебільшого криві, які прагнуть стати паралельними осі абсцис. Г.органічних сполук була з'ясована в 50 роках Жераром (див.). Їм були вперше встановлені гомологічні ряди, які й лягли в основу його системи класифікації органічних сполук. Згодом Г. ускладнилася внаслідок відкриття численних випадків ізомерії.Гомологічні ряди Жерара розчленували в гомологічні порядки. Так, напр., Г.ряд граничних одноатомних спиртів CnH2n +2 O розпався на порядки первинних, вторинних і третинних спиртів CnH2n +1 CH2 (ПЗ), (CnH2n +1) 2-CH (ПЗ) і (СnH2n +1) 3C (ПЗ), які, у свою чергу , в залежності від ізомерії залишків СnH2n +1 дають нові порядки, напр.первинні спирти утворюють порядки нормальних СН3-(СН2) n-СН2 (ПЗ) і ізоспіртов (СН3) 2-CH (СН2) n-СН2 (АЛЕ) (n = 0, 1, 2 ...) і т. д.
Варіант 6
