
- •Раздел 1. Введение в курс.
- •Комплексное использование сырья
- •Совершенствование методов выделения целевых продуктов и очистки всех потоков, которые попадают в окружающую среду.
- •Комбинирование производств
- •Повышение степени энергосбережения на предприятиях химической промышленности
- •Создание агрегатов большой единичной мощности
- •Интенсификация хтп
- •Раздел 2. Разработка химической концепции метода.
- •Время пребывания исходных веществ в реакционной зоне.
- •Объемная скорость
- •Алгоритм разработки химической концепции хтп
- •Термодинамический анализ
- •Изобарно-изотермический потенциал (энергия Гиббса)
- •Связь константы с равновесным выходом
- •Связь константы равновесия с энергией Гиббса
- •Анализ зависимостей изменения константы равновесия от температуры при различных знаках ∆н и ∆s реакции.
- •Качественная оценка условий проведения процесса.
- •Влияние температуры
- •Влияние соотношения реагентов на их степень превращения и выход продукта
- •Соотношение реагентов – стехиометрическое
- •Один из реагентов - в избытке
- •Влияние величины общего давления
- •Влияние введения в систему инертного компонента (d), при сохранении величины общего давления
- •Вывод продукта из зоны реакции
- •Понятие элементарной реакции
- •Простые по механизму и стехиометрически простые реакции
- •Зависимость константы скорости элементарной реакции от температуры
- •Зависимость дифференциальной селективности от концентраций реагирующих веществ
- •Зависимость дифференциальной селективности от температуры
- •Особенности кинетики окисления оксида азота (II) в оксид азота (IV)
- •Скорость обратимых реакций
- •Обратимая эндотермическая реакция
- •Раздел 3. Химическое производство как химико-технологическая система (хтс).
- •Раздел 4. Основные принципы разработки хтс и способы их реализации.
- •Принцип наилучшего использования сырья.
- •Избыток реагентов ускоряет как химическую, так и диффузионную стадии процессов.
- •Подавление побочных реакций.
- •Принцип наибольшей интенсивности процесса.
- •Принцип наилучшего использования энергии.
- •Принцип экологической безопасности химических производств.
- •Раздел 5. Реализация основных принципов разработки и организации хтс на примерах конкретных производств.
- •Производство технологических газов конверсией метана.
- •Паровая конверсия
- •Термодинамика процесса
- •Кинетика процесса
- •Выбор оптимальных условий для проведения паровой конверсии метана
- •Катализатор и температура
- •Соотношение исходных веществ
- •Паровоздушная конверсия метана
- •Паровая конверсия монооксида углерода
- •Термодинамика процесса
- •Кинетика процесса
- •Выбор оптимальных условий для проведения паровой конверсии монооксида углерода
- •Катализаторы и температура
- •Соотношение исходных веществ
- •Очистка от диоксида углерода
- •Моноэтаноламиновая очистка
- •Карбонатная очистка
- •Очистка от монооксида углерода
- •Промывка жидким азотом
- •Тонкая очистка метанированием
- •Катализаторы синтеза аммиака.
- •Производство метанола.
- •5.6. Производство этанола.
-
Время пребывания исходных веществ в реакционной зоне.
На выход целевого продукта и интенсивность работы аппарата влияют не только температура, давление, концентрации исходных веществ, но и длительность пребывания этих веществ в зоне реакции. В аппаратах периодического действия время пребывания реагентов — это интервал времени между загрузкой и выгрузкой аппарата. В аппаратах непрерывного действия время пребывания исходных веществ в реакционной зоне определяют следующим образом:
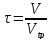
где V – реакционный (полезный) объем аппарата, Vt,p - расход исходных веществ, поступающих в реакционный аппарат при температуре и давлении в аппарате.
Для каталитических
процессов рассчитывают время
соприкосновения
исходных веществ с
катализатором.
Его называют временем
контактирования.
Время контактирования находят из
отношения свободного объема катализатора
Vсв
к расходу исходных веществ Vt,p,
проходящих через катализатор при
условиях процесса.
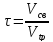
Свободный объем катализатора — это объем пустот между зернами и в сетках катализатора. Свободный объем Vсв рассчитывают, как произведение объема катализатора Vk на долю свободного объема ε:
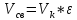
При расчете времени контактирования во взвешенном слое катализатора свободный объем находят как разность между объемом, занимаемым катализатором во взвешенном состоянии, Vвзв, и объемом твердых частиц катализатора Vk (1- ε):
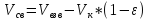
Если катализатор выполняется в виде сетки, его свободный объем рассчитывают по формуле:
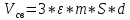
где ε - доля свободного объема катализатора, m - число сеток, S - рабочая площадь сетки, d - диаметр нити сетки, 3 - числовой коэффициент, учитывающий увеличение толщины сетки при переплетении нитей.
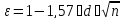
где d - диаметр нити сетки, см; n – число плетений сетки на 1 см2.
-
Объемная скорость
Объемная скорость W — это объем исходных веществ, поступающих в реакционный аппарат в единицу времени в фазовом состоянии, соответствующем условиям проведения процесса (для газофазных процессов – в газообразном состоянии), отнесенный к единице реакционного объема.
Для нахождения объемной скорости расход исходных веществ берут как при условиях проведения процесса (температуре и давлении в реакторе), так и при нормальных условиях (условная объемная скорость):
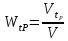 или
или
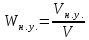
где V - объем реактора.
Объемная скорость
и время пребывания исходных веществ в
реакционной зоне связаны соотношением:
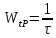 .
.
В каталитических процессах вместо реакционного объема в расчете объемной скорости используют объем катализатора Vk:
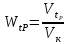
-
Алгоритм разработки ХТП. Термодинамический анализ. Константа равновесия и изобарно-изотермический потенциал. Связь константы равновесия с равновесной степенью превращения и свободной энергией Гиббса. Анализ зависимостей изменения константы равновесия от температуры при различных знаках ∆Н и ∆S реакции.
-
Алгоритм разработки химической концепции хтп
Необходимо: обосновать выбора условий проведения процесса, катализатора, реактора, решение проблем теплоподвода и теплоотвода и т.п.
Первым этапом является выбор сырья и метода его переработки.
Термодинамический анализ позволяет по справочным данным оценить вероятность получения приемлемого выхода целевого продукта в доступных для химической технологии условиях.
Если результаты анализа указывают на то, что данный процесс не является запрещенным с термодинамической точки зрения, то переходят к следующему этапу разработки ХТП.
Если оказывается, что в доступных условиях выход целевого продукта из данных реагентов слишком мал, то выбирают другое сырье.
В случае положительного результата термодинамического анализа (может быть получен приемлемый выход) нужно установить необходимость применения катализатора. Если возможно обойтись без использования катализатора, то переходят к изучению кинетических закономерностей процесса.
При необходимости применения катализатора устанавливают тип катализатора, его фазовое состояние, т.е. будет ли это гомогенный или гетерогенный катализатор и, соответственно, каталитический процесс.
Как в случае каталитического, так и некаталитического процесса важен вопрос о фазовой характеристике системы. Отметим, что термодинамика процесса будет также различна при различном фазовом состоянии веществ системы.
В результате изучения кинетических закономерностей необходимо создать кинетическую модель процесса, которая позволит описать зависимость скорости процесса от таких условий как температура, концентрации реагентов, давление и т.п. или зависимости концентраций участников процесса от времени его протекания.
Математическая модель процесса с учетом массообмена и теплообмена служит основой для оптимизации ХТП, то есть поиска таких условий его реализации, при которых достигается максимальная степень превращения реагентов, максимальная селективность и выход продукта.
Данные лабораторных исследований служат основой для создания пилотной, опытной, опытно-промышленной установки. Так как такие стороны ХТП как массообмен и теплообмен плохо масштабируются, то результаты лабораторных исследований нельзя, как правило, напрямую применить к промышленным установкам. Это и вызывает необходимость промежуточных ступеней исследования.
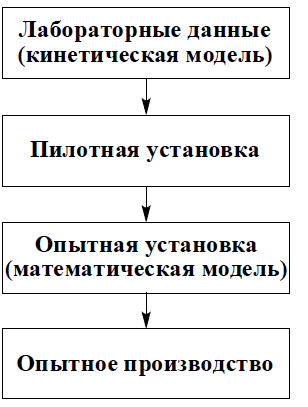
Схема примерного алгоритма разработки физико-химической концепции метода:

