
- •Лекция № 4 (тобт 1)
- •Стадии биосинтеза в клетках продуцентов
- •2. Биосинтез низкомолекулярных соединений в клетках продуцентов: аминокислот, жирных кислот, нуклеотидов.
- •Организация и регуляция метаболизма в клетках продуцентов.
- •6. Конечные продукты метаболизма в клетках продуцентов. Продукты анаэробного метаболизма (брожения) в клетках продуцентов
- •7.Частичное окисление и его конечные продукты в клетках продуцентов. Синтез вторичных метаболитов в клетках продуцентов
Лекция № 4 (тобт 1)
Стадии биосинтеза в клетках продуцентов.
Биосинтез низкомолекулярных соединений в клетках продуцентов: аминокислот, жирных кислот, нуклеотидов.
Превращение веществ-предшественников в нуклеотиды и дезоксирибонуклеотиды в клетках продуцентов. Участие высокоэнергетических трифосфатов нуклеозидов в различных путях биосинтеза в клетках продуцентов.
Организация и регуляция метаболизма в клетках продуцентов.
Регуляция метаболитами, на ферментативном уровне в клетках продуцентов. Взаимосвязь регуляторных механизмов и их реализация в клетках. Влияние состава питательной среды на системы клеточной регуляции.
Конечные продукты метаболизма в клетках продуцентов. Продукты анаэробного метаболизма (брожения) в клетках продуцентов.
Частичное окисление и его конечные продукты в клетках продуцентов. Синтез вторичных метаболитов в клетках продуцентов.
Стадии биосинтеза в клетках продуцентов
Большинство процессов в мире микроорганизмов характеризуются 1) утилизацией субстратов или питательных веществ, 2) ростом клеток и 3) выделением в среду продуктов их метаболизма. Биосинтез связан со всеми этими тремя сторонами жизнедеятельности клеток. Необходимость в питательных веществах определяется потребностями клетки в веществах-предшественниках, запасах химической энергии и восстанавливающих эквивалентах. Некоторые продукты биосинтеза клетка выделяет в среду. Наконец, скорость биосинтеза определяет скорость образования новых компонентов клетки и, таким образом, темпы клеточного роста. Для биосинтетических целей клетка использует химические ресурсы, образующиеся в процессах катаболизма. Как правило, реакции синтеза термодинамически невыгодны и протекают только одновременно с гидролизом АТР до ADP или AMP. При гидролизе образующегося в последнем случае пирофосфа-та (Р~Р) выделяется дополнительная свободная энергия (ΔG°'~7 ккал/моль), также использующаяся для «запуска» реакций синтеза. Поскольку питательные вещества обычно окислены в большей степени, чем необходимые клетке соединения, то для биосинтеза последних нужны и восстанавливающие эквиваленты.
Основные стадии биосинтеза представлены на нижеприведенной схеме. Как видно из рисунка последовательность биохимических превращений в клетке следующая:
-поступление питательных веществ в клетку;
-расщепление питательных веществ на более простые;
-синтез низкомолекулярных соединений (аминокислот, жирных кислот, нуклеотидов);
синтез макромолекул (белков, углеводов, ДНК, РНК);
-включение макромолекул в структуру клетки и в системы жизнеобеспечения.

2. Биосинтез низкомолекулярных соединений в клетках продуцентов: аминокислот, жирных кислот, нуклеотидов.
Биологически важные низкомолекулярные соединения в основном являются мономерами и используются клеткой для построения биополимеров. Для этой цели необходимо в общей сложности примерно 70 различных соединений: 4 рибонуклеотида, 4 дезоксирибонуклеотида, 20 аминокислот, около 15 моносахаридов и около 20 жирных кислот и других предшественников липидов. Кроме того, в реакциях второго типа должны синтезироваться ATP, NAD, другие соединения-переносчики и коферменты. Все эти вещества называют центральными промежуточными метаболитами.
Аминокислоты можно разделить на четыре группы (семейства), различающиеся химическим строением и природой биосинтетических предшественников. Биосинтез всех аминокислот начинается с промежуточных соединений в метаболизме углерода (схема – семейства аминокислот и их предшественники - углеводы).

Живые клетки усваивают азот путем его включения в аминокислоты глутамин и глутаминовую кислоту. Сначала при взаимодействии аммиака с α-кетоглутаровой кислотой (одним из промежуточных веществ в цикле трикарбоновых кислот) образуется глутаминовая кислота:
глутаматдегидрогеназа
H OOC(CH2)2COCOOH
+ NH4+
+ NADH
OOC(CH2)2COCOOH
+ NH4+
+ NADH
HOOC(CH2)2CHNH2COOH + NAD+ + H2O
Глутаминовая кислота может связать еще один аммониевый ион и превратиться в глутамин:
глутаминсинтаза
H OOC(CН2)2CHNH2COOH
+ NH4+
+ ATP
OOC(CН2)2CHNH2COOH
+ NH4+
+ ATP
H2NОС(CH2)2CHNH2COOH+ADP + P,+H+
ΔG0 =— 3,9 ккал/моль
Вторая реакция, происходящая с поглощением метаболической энергии, осуществляется при недостатке аммиака в среде. В некоторых бактериях с участием NADH происходит непосредственное аминирование пирувата до аланина, а другие бактерии способны превращать фумарат в аспартат. Ряд микроорганизмов усваивает азот в виде нитрата NO3- и свободного азота N2; сейчас известно, однако, что эти питательные вещества сначала трансформируются в аммиак, который; затем и ассимилируется клетками по описанным выше путям.
Все другие аминокислоты образуются из глутамата или на основе его углеродного скелета, или путем переноса аминогруппы к другим молекулам (реакция переаминирования). Все реакции переаминирования происходят только в присутствии кофермента пиридоксальфосфата, производного витамина B6 (пиридоксаля).
В биосинтезе жирных кислот и других предшественников липидов роль исходных веществ выполняют ацетил-СоА и глицерин. Рассмотрим путь биосинтеза самой обычной из жирных кислот – пальмитиновой СН3(СН2)14СООН. Первая стадия этого пути заключается в карбоксилировании ацетил-СоА, в результате чего образуется малонил-СоА:
ацетил-СоА- карбоксилаза
 Ацетил-СоА + АТР + СО2
Ацетил-СоА + АТР + СО2
Малонил -СоА + ADP + Pi
(HOOCCH2COSCoA)
Обратите внимание на то, что в этом процессе на каждую молекулу образующегося малонил-СоА расходуется одна молекула макроэргического фосфата.
Далее из семи молекул малонил-СоА и одной молекулы ацетил-СоА образуется пальмитат. Этот процесс осуществляется ступенчато, а его конечный результат можно выразить следующим уравнением:
А цетил-СоА
+ 7 малонил-СоА + 14 (NADPH
+ Н+)
цетил-СоА
+ 7 малонил-СоА + 14 (NADPH
+ Н+)
Пальмитат + 7 СО2 + 8 НSCoA + 14 NADP+ + 6H2O
3. Превращение веществ-предшественников в нуклеотиды и дезоксирибонуклеотиды в клетках продуцентов. Участие высокоэнергетических трифосфатов нуклеозидов в различных путях биосинтеза в клетках продуцентов.
Продукты катаболизма глюкозы являются важнейшими предшественниками в биосинтезе аминокислот, нуклеотидов и жирных кислот. Следовательно, организмы, растущие на других источниках углерода, например СО2, должны превращать их в глюкозу или а один из ближайших продуктов ее метаболизма. Кроме того, при избытке соединений углерода (по сравнению с другими питательными веществами) многие клетки превращают глюкозу в резервные углеводы и хранят их для последующего использования. Схематично пути синтеза нуклеотидов и дезоксирибонуклеотидов из веществ-предшественников представлены на рисунке:
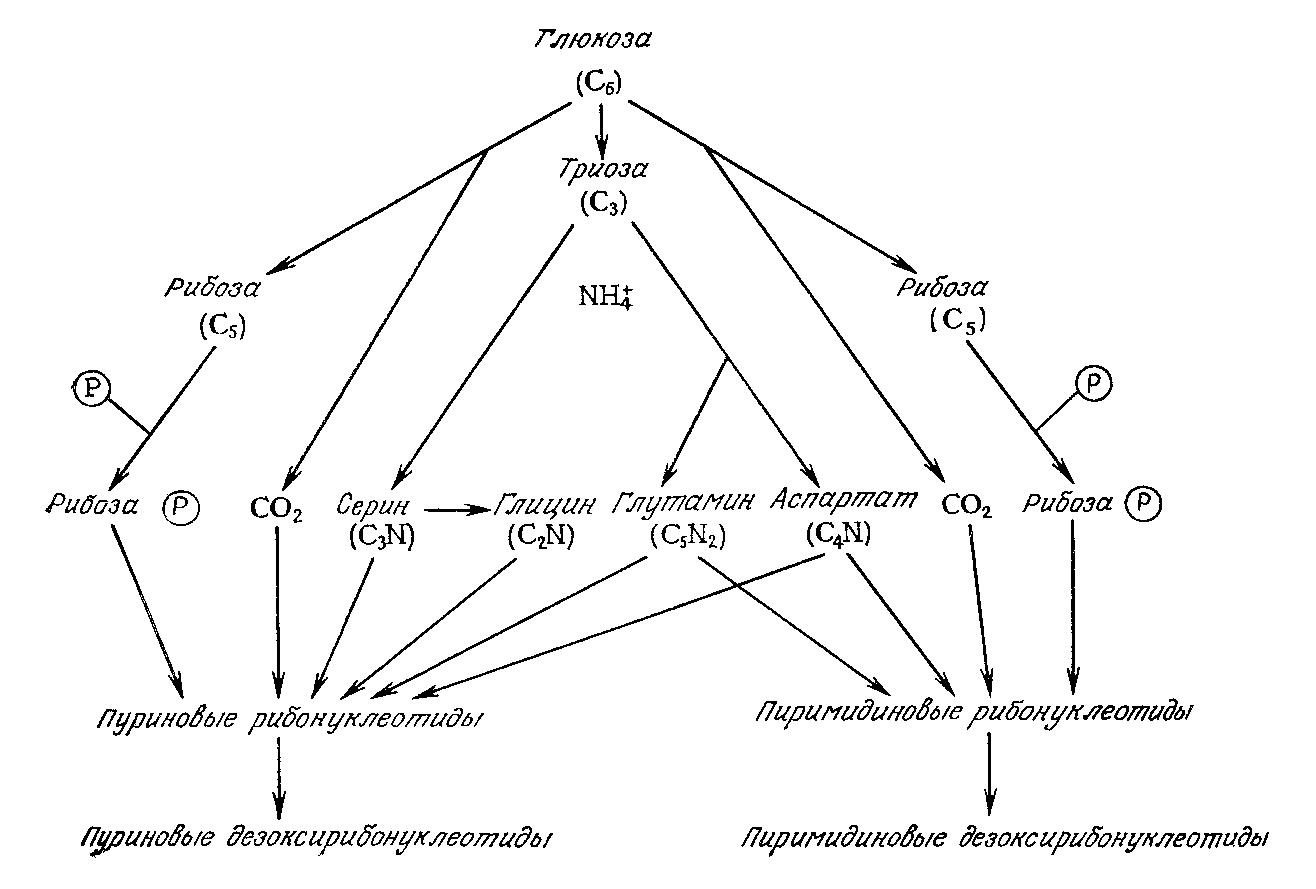
Из мономерных веществ-предшественников далее строятся полимерные компоненты клетки. Для этой цели требуется большое количество метаболической энергии, поскольку любая реакция конденсации сопровождается повышением свободной энергии. Более того, чрезвычайно большие запасы свободной энергии являются той движущей силой, которая резко смещает общее равновесие в сторону образования необходимых полимеров.
Хранящаяся в фосфатных связях АТР энергия при посредстве трифосфатов других нуклеотидов утилизируется в биосинтезе четырех классов биополимеров. Для биосинтеза макромолекулярных соединений типично сочетание реакции конденсации с гидролизом двух высокоэнергетических фосфатных связей, причем сначала нуклеозидтрифосфат превращается в нуклеозидмонофосфат и пирофосфат, который также подвергается гидролизу. Таким путем высвобождается примерно в 2 раза больше свободной энергии (около 14 ккал/моль), чем при превращении нуклеозидтрифосфата в соответствующий дифосфат.
Участие высокоэнергетических трифосфатов нуклеозидов в различных путях биосинтеза схематично можно изобразить следующим образом:
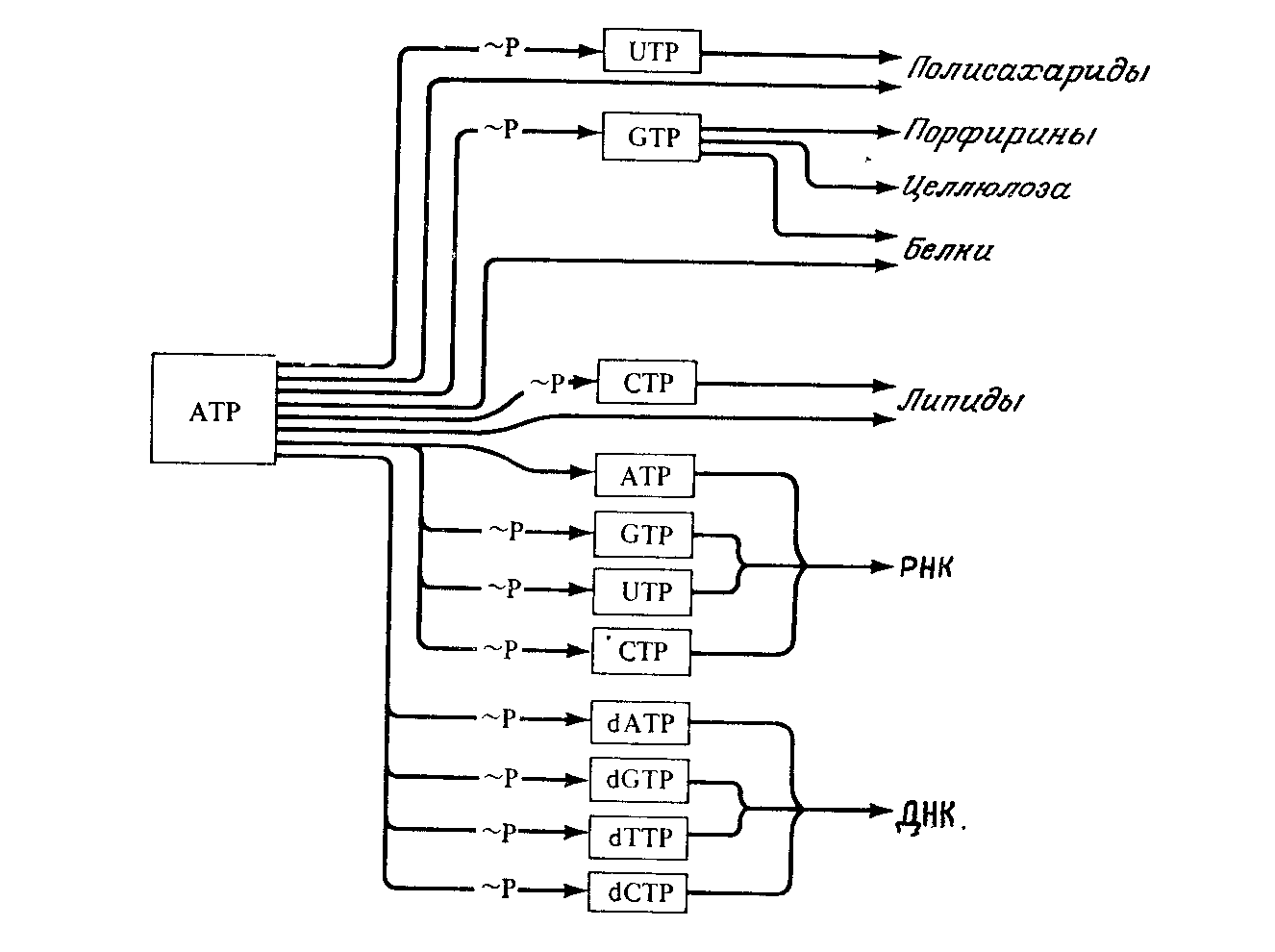
UTP – уридин трифосфат; GTP – гуанозин трифосфат;
CTP – цитидин трифосфат; TTP – тимидин трифосфат.
Естественно, синтез информационных полимеров (РНК, ДНК и белков) представляет собой гораздо более сложный процесс. И в том и в другом случае, однако, наращиванию полимерной цепи предшествует активация мономера. В схему синтеза РНК и ДНК нуклеотиды входят в виде нуклеозидтрифосфатов, а присоединяется к соответствующей полимерной цепи монофосфат; реакция сопровождается образованием пирофосфата. Таким образом, для присоединения одного моиомерного остатка необходимо затратить 14 ккал/моль энергии. Активация аминокислот в ходе синтеза белков осуществляется в соответствии со следующей схемой:
А минокислота
+ АТР аминоацил-АМР +
Р~Р
минокислота
+ АТР аминоацил-АМР +
Р~Р
(активированная аминокислота)
Кроме того, процесс присоединения аденилата аминокислоты к пептидной цепи сопровождается гидролизом GTP; следовательно, для присоединения одного аминокислотного остатка к белковой цепи необходимо гидролизовать в общей сложности три высокоэнергетические фосфатные связи.
