
- •1 Вариант
- •2 Вариант
- •Закон Шарля
- •Увеличивается
- •3 Вариант
- •Не изменяется
- •4 Вариант
- •Не изменяется
- •5 Вариант
- •Первого закона термодинамики
- •Уменьшается
- •6 Вариант
- •Первого закона термодинамики
- •Увеличивается
- •7 Вариант
- •Первого закона термодинамики
- •17 Вариант
- •3. Молекулой вещества называют:
- •4.При кристаллизации температура вещества:
- •18Вариант
- •19 Вариант
- •20Вариант
- •21Вариант
- •22 Вариант
- •23Вариант
- •24 Вариант
- •23 Вариант
- •3. Молекулой вещества называют:
- •4.При кристаллизации температура вещества:
- •5. Количество вещества ν определяется по формуле:
- •25 Вариант
- •3. Молекулой вещества называют:
- •4.При кристаллизации температура вещества:
- •5. Количество вещества ν определяется по формуле:
- •27 Вариант
- •28Вариант
- •29 Вариант
- •30 Вариант
1 Вариант
1.Единицей количества вещества в СИ является:
кг
моль
г
кмоль
2. При постоянном давлении, для постоянной массы идеального газа справедлив закон:
закон Шарля
закон Бойля-Мариотта
закон Гей-Люссака
закон Дальтона
3. Молекулой вещества называют:
наименьшую частичку, которая может быть отделена от этого вещества.
мельчайшую частичку вещества, сохраняющую все физические свойства этого вещества.
мельчайшую частичку вещества, сохраняющую химические свойства данного вещества.
мельчайшую частичку вещества, сохраняющую физические и химические свойства этого вещества.
мельчайшую частичку вещества, которая самопроизвольно хаотически движется.
4.При кристаллизации температура вещества:
увеличивается
уменьшается
не изменяется
равна 0 °С
5.Количество вещества ν определяется по формуле:
ν = n/NA
ν = NA/N
ν = N/NA
ν = NA/n
Задача. Определить среднюю кинетическую энергию поступательного движения одной молекулы воздуха при нормальных условиях. Концентрация молекул воздуха при нормальных условиях n0 = 2,7·1025 м–3.
2 Вариант
1.Абсолютная температура измеряется в:
°C
°F
°R
К
2.Объем данного количества газа при постоянной температуре обратно пропорционален его давлению.
Закон Шарля
закон Бойля-Мариотта
закон Гей-Люссака
закон Дальтона
3.Моль — это:
количество вещества, все молекулы которого движутся с одинаковыми скоростями.
количество вещества, все молекулы которого одинаковы.
количество вещества, содержащее столько молекул, сколько их содержится в 0,012 кг углерода.
количество вещества, в котором содержится при любых условиях одно и то же число молекул, равное 6,02·1023.
количество вещества, молекулы которого движутся с одинаковыми по модулю, но различными по направлению скоростями.
4.При конденсации температура вещества:
Увеличивается
уменьшается
не изменяется
равна 0 °С
5.Массу mo одной молекулы вещества с молярной массой М можно вычислить по формуле:
mo = M/NA
mo = m/NA
mo = M/N
mo = m/n
Задача. Определить температуру идеального газа, если средняя кинетическая энергия поступательного движения его молекул равна 7,87·10–21 Дж.
3 Вариант
1.Концентрация частиц идеального газа измеряется в СИ:
1/м3
1/моль
1/л
см3
2.Три макропараметра (давление, объем и температура) для 1 моля вещества связаны законом:
Шарля
Бойля-Мариотта
Менделеева-Клапейрона
Клапейрона
3.Молярная масса — это:
масса всех молекул, входящих в состав данного вещества
масса молекул, состоящих из атомов только этого вещества
масса молекул углерода, содержащихся в 0,012 кг
масса всех молекул данного вещества
масса одного моля вещества
4.При плавлении внутренняя энергия вещества:
Не изменяется
увеличивается
уменьшается
равна 0 °С
5.Средняя квадратичная скорость хаотического движения молекулы равна:
<v> =

<v> =
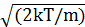
<v> =

<v> =

Задача. Какой объем занимает 1 кг кислорода при температуре 273 K и давлении 8·105 Па? Молярная масса кислорода M = 32·10–3 кг/моль.
