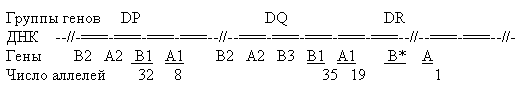Электив на тему Сахарный диабет (текст) / 8 Предсказание и предупреждение сахарного диабета
.docVIII. Предсказание и предупреждение сахарного диабета
В настоящее время ИЗСД рассматривается как многофакторное заболевание, обусловленное и наследственной предрасположенностью, и влияниями среды обитания. В западных странах примерно один из 300 индивидов случайной выборки заболевает ИЗСД, а среди родственников первой степени родства больных ИЗСД заболевает один из 20 индивидов. Если один из монозиготных близнецов болен ИЗСД, то риск заболевания другого близнеца оценивается в 30 - 50% в течение шести лет (по другим данным - до 90%). Т.о. предрасположенность к болезни имеет генетическую основу. В целом, по примерным оценкам, заболеваемость на 80% определяется генотипом и на 20% - факторами среды.
ИЗСД является полигенной болезнью; у мышей найдено более десяти генных локусов, определяющих предрасположенность. У человека в наибольшей мере восприимчивость к ИЗСД зависит от генов ГКГ, и в особенности - от полиморфизма HLA-генов, кодирующих белки класса II (гены DP, DQ и DR в коротком плече хромосомы 6). Гены HLA являются наиболее полиморфной генетической системой популяций человека. С нарушением функций этой системы связаны многие аутоиммунные заболевания, и в том числе ИЗСД.
На рисунке представлена область генов ГКГ класса II. В отличие от генов групп DP и DQ, каждый из которых представлен одним локусом (локус DPB2, локус DPA2 и т. д.), в группе DR участок B* (DRB*) содержит 9 локусов (DRB 1 - 9), из которых 5 - псевдогены (не экспрессируются). Действующие гены 1, 3, 4 и 5 кодируют каждая особую -цепь. Кроме того, эти гены полиморфны: например, известно около 200 аллелей гена DRB1:
|
Область генов ГКГ класса II. А - гены a-цепей, В - гены -цепей белков ГКГ. Подчеркнуты действующие гены, не подчеркнутые - псевдогены (не экспрессируются). Указанное число аллелей не окончательно: продолжают обнаруживаться все новые аллели. |
Ген DRA - единственный и не полиморфный, так что у всех индивидов все белки ГКГ, кодируемые областью DR, имеют одинаковую -цепь: DR1, DR3, DR4 и DR5. Еще раз отметим, что гены B и соответственно -цепи полиморфны. Например, может быть 200 разных белков DR1, по числу аллелей гена DRB1.
Метод полимеразной цепной реакции позволяет быстро и точно определять наличие того или иного аллеля в геноме и проводить массовые исследования распределения аллелей среди индивидов популяции. При этом обнаружилось, что у больных ИЗСД встречаемость аллелей ГКГ класса II существенно отличается от встречаемости тех же аллелей у здоровых людей. Некоторые аллели ассоциированы с ИЗСД, т.е. часто встречаются у больных; очевидно, они и определяют предрасположенность к болезни. И наоборот, есть аллели, которые почти не встречаются у больных ИЗСД; их рассматривают как снижающие предрасположенность, протективные аллели. Интересно, что протективные аллели являются доминантными по отношению к предрасполагающим. Еще более ясно связь между генотипом и ИЗСД проявляется, если учитывать распределение не отдельных генов, а комбинаций нескольких генов. В таблице приведены примеры таких генотипов.
Предрасположенность к ИЗСД в зависимости от генотипа (число после звездочки - шифр аллеля)
|
|
Результаты исследований генома позволяют надеяться, что можно будет с высокой вероятностью предсказывать, заболеет ли ИЗСД данный индивид. Однако предстоит еще очень большая работа по изучению влияния отдельных генов и их комбинаций на предрасположенность к ИЗСД. Дело осложняется тем, что предрасполагающие и протективные генотипы неодинаковы у разных этнических групп. Давно известна неравномерность распространения ИЗСД в разных регионах мира. Например, в Японии больны 1,7% населения, в России около 5%, в большинстве стран Европы и в США 5 - 12%, в Скандинавских странах Европы около 20%, а в Финляндии даже 35%. Теперь выясняется, что такая неравномерность в значительной мере связана с особенностями распространения аллелей генов HLA в геноме разных этносов. Например, в Эндокринологическом Научном Центре РАМН выполнены исследования по распространенности аллелей локусов DR и DQ у больных ИЗСД и здоровых доноров трех этнических групп - европеоидной (русские), монголоидной (буряты) и смешанной евро-монголоидной (узбеки). Заболеваемость ИЗСД у русских и узбеков от 1,5 до 5 на 10000, у бурят примерно в 10 раз ниже. Найдены генотипы предрасположенности к ИЗСД как общие для всех трех групп, так и этноспецифические. К последним относятся следующие генотипы:
|
|
Таким образом, необходимо определять генотип каждой этнической группы, а нарастающее смешение этносов вносит дополнительные сложности. Тем не менее, это направление исследований, безусловно, перспективно. Оно, в частности, может оказаться полезным для выяснения механизма развития аутоиммунной реакции, ведущей к гибели -клеток, и могут быть обнаружены молекулярные мишени для лекарственного воздействия на процесс. Возможность предсказания ИЗСД позволит применять методы генетической консультации для предупреждения рождения детей, предрасположенных к заболеванию ИЗСД. Наконец, эти исследования перемещают задачу предупреждения ИЗСД у детей, родившихся с предрасполагающим генотипом, в разряд самых актуальных, и одновременно создают основу для решения этой задачи. В настоящее время больной ИЗСД попадает в поле зрения врача при появлении клинических признаков, т.е. после того, как в течение нескольких лет до этого в результате аутоиммунного процесса уже погибло около 80% -клеток. Если проводить обследование всех новорожденных на генетическую предрасположенность к ИЗСД, то детей с неблагоприятным генотипом можно взять под наблюдение и принимать предупредительные меры при угрозе начала аутоиммунного процесса.
Способы предупреждения диабета тоже еще только предстоит разработать. В экспериментах на животных такие результаты уже получаются, причем довольно простыми методами. Например, у мышей линии NOD с высокой генетической предрасположенностью к диабету удается предотвратить болезнь диетой, не содержащей некоторых белков, инфицированием многими вирусами, однократным введением адъюванта Фрейнда или BCG, введением пептидов инсулина. В более отдаленной перспективе могут быть разработаны методы генотерапии.