
Ответы на Коллоквиум № 5 по теме Обмен аминокислот / 4 вариант
.docОтветы на Коллоквиум по Биохимии № 5
4 вариант

1.
а) Не будет, потому что нет соответствующих аминокислот, на которые действует данный пептид
б) Смотри стрелки под формулой пептида наверху.
 в)
в)
2. а)
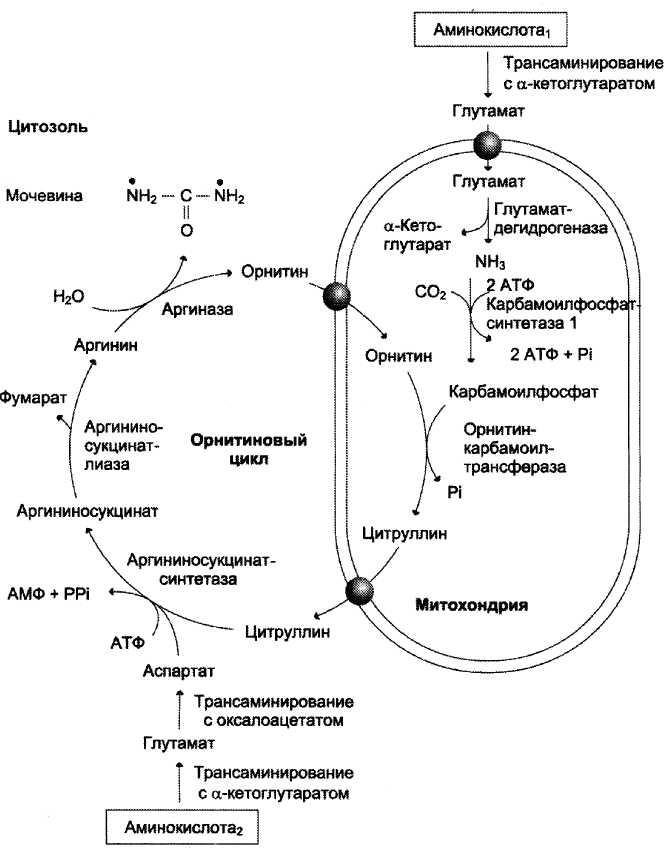
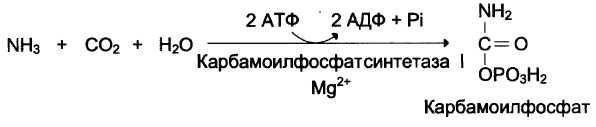
б)
в) Аммиак, глутамин, ион аммония NH4+.
г) Высокие концентрации аммиака стимулируют синтез глутамина из глутамата в нервной ткани (при участии глутаминсинтетазы): Глутамат + NH3 + АТФ → Глутамин + АДФ + Н3РО4.
Накопление глутамина в клетках нейроглии приводит к повышению осмотического давления в них, набуханию астроцитов и в больших концентрациях может вызвать отёк мозга. Снижение концентрации глутамата нарушает обмен аминокислот и нейромедиаторов, в частности синтез γ-аминомасляной кислоты (ГАМК), основного тормозного медиатора. При недостатке ГАМК и других медиаторов нарушается проведение нервного импульса, возникают судороги.
Ион NH4+ практически не проникает через цитоплазматические и митохондриальные мембраны. Избыток иона аммония в крови способен нарушать трансмембранный перенос одновалентных катионов Na+ и К+, конкурируя с ними за ионные каналы, что также влияет на проведение нервных импульсов.
д) Малобелковая диета и введение кетоаналогов аминокислот.
3. а)
1. Метионин - незаменимая аминокислота, необходимая для синтеза белков. Метионил-тРНКМет участвует в инициации процесса трансляции. Как и многие другие аминокислоты, метионин подвергается транс- и дезаминированию.
2. Особая роль метионина заключается в том, что метальная группа этой аминокислоты используется для синтеза целого
ряда соединений в реакциях трансметилирования.
3. Примеры реакций трансметилирования: Синтез фосфатидилхолина, Синтез адреналина, Синтез креатина.
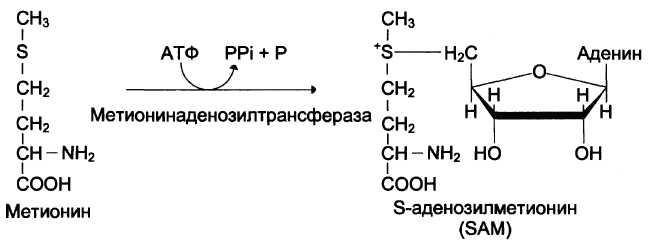 4.
Метионин необходим для синтеза условно
заменимой аминокислоты цистеина, причем
он является донором атома серы.
4.
Метионин необходим для синтеза условно
заменимой аминокислоты цистеина, причем
он является донором атома серы.
б)

в) Холин может пойти на образование фосфатидилхолина, либо на синтез ацетилхолина

4. а) 1. Трансаминирование тирозина с ос-кетоглу-таратом катализирует тирозинаминотрансфе-раза (кофермент ПФ) — индуцируемый фермент печени млекопитающих. В результате образуется п-гидроксифенилпируват.
2. В реакции окисления п-гидроксифенилпи-рувата в гомогентизиновую кислоту происходит декарбоксилирование, гидроксилирование ароматического кольца и миграция боковой цепи. Реакцию катализирует фермент п-гид-роксифенилпируватдиоксигеназа, кофакторами которого выступают витамин С и Fe2+.
3. Превращение гомогентизиновой кислоты в фумарилацетоацетат сопровождается расщеплением ароматического кольца. Эта реакция катализируется диоксигеназой гомогентизиновой кислоты, в качестве кофермента содержащей Fe2+.
4. Гидролиз фумарилацетоацетата при действии фумарилацетоацетатгидролазы приводит к образованию фумарата и ацетоацетата.
б) Реакция № 4 на рисунке сверху.
5. а) Гистамин образуется путём декарбоксилирования гистидина в тучных клетках соединительной ткани.
Гистамин образует комплекс с белками и сохраняется в секреторных гранулах тучных клеток. Секретируется в кровь при повреждении ткани (удар, ожог, воздействие эндо- и экзогенных веществ), развитии иммунных и аллергических реакций. Гистамин выполняет в организме человека следующие функции:
• стимулирует секрецию желудочного сока, слюны (т.е. играет роль пищеварительного гормона);
• повышает проницаемость капилляров, вызывает отёки, снижает АД (но увеличивает внутричерепное давление, вызывает головную боль);
• сокращает гладкую мускулатуру лёгких, вызывает удушье;
• участвует в формировании воспалительной реакции — вызывает расширение сосудов, покраснение кожи, отёчность ткани;
• вызывает аллергическую реакцию;
• выполняет роль нейромедиатора;
• является медиатором боли.
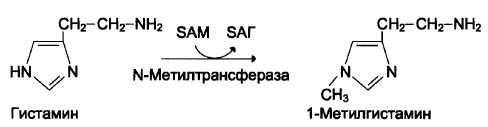 б
б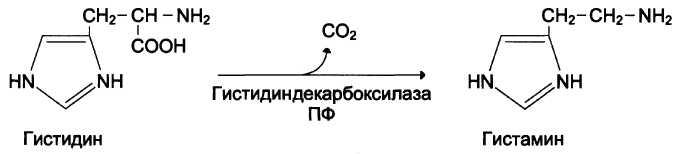 )
Схема синтеза: Схема инактивации:
)
Схема синтеза: Схема инактивации:
