- •22 Лекция 10
- •10. Физико-химические основы химических и электрохимических методов нанесения и травления тонких пленок и материалов
- •10.1. Основы электрохимии Жидкие растворы и электролиты
- •Электрохимический процесс
- •Электролиз и его законы
- •10.2. Электрохимическое осаждение
- •10.3. Химическое осаждение пленок из растворов и паровой фазы Химическое осаждение пленок из растворов
- •Осаждение из паровой фазы
- •10.4. Коррозия
- •10.5. Химические методы травления
- •Кинетика процесса химического травления
- •Механизм травления
10.2. Электрохимическое осаждение
В основе электрохимического осаждения металлических пленок лежит явление электролиза, при котором происходит катодное восстановление катионов. Впервые явление восстановления катионов металла исследовал русский физик и электротехник Б.С.Якоби, работы которого легли в основу гальваностегии (осаждение тонких пленок металлов) и гальванопластики (изготовление рельефных металлических копий с предметов).
Электрохимическое осаждение применяют для создания контактных систем на диэлектрических подложках с предварительно нанесенной тонкой проводящей пленкой, получения объемных омических контактов-выводов к активным областям полупроводниковых структур, изготовления свободных масок, получения покрытий на деталях корпусов, обеспечивающих качественную герметизацию и в некоторых случаях защиту от коррозии.
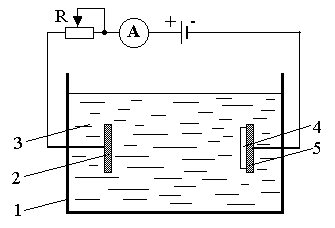
Для осаждения пленок подготовленные подложки помещают в электролитическую ванну на катоде (рис.10.2). Анод обычно изготавливают из того же металла, что и осаждаемая пленка. В состав электролита входит соль осаждаемого металла. Процесс осаждения пленок сопровождается растворением анода, что предотвращает обеднение электролита ионами металла. Площадь поверхности анода приблизительно в 1,5 раза превышает площадь поверхности, на которую осаждается пленка.
Электрохимическое осаждение металлов согласно современным представлениям происходит в четыре стадии:
1) электролитическая диссоциация соли в растворе;
2) перенос ионов из объема электролита к электроду;
3) переход ионов на границе фаз из объема электролита к металлу;
4) диффузия адсорбированных атомов по поверхности электрода к местам роста пленки и встраивание атомов в кристаллическую решетку.
В электролитической ванне (рис.10.2) происходит два вида превращений.
|
|
Рис.10.2. Конструктивная схема электролитической ванны: 1 – ванна; 2 – анод; 3 – электролит; 4 – осаждающаяся пленка; 5 - катод |
В результате одного из них освобождаются электроны на аноде:
2Х - - 2е - = Х2, (10.7)
где Х -- галлоид-, сульфат-, нитрат- и т.п. ионы. В результате другого - электроны присоединяются на катоде:
Ме2+ + 2е - =Ме. (10.8)
В растворе электролита при диссоциации возникают ионы:
МеХ2 Ме2+ + 2Х -. (10.9)
Если реакции (10.7) и (10.8) пространственно разделены друг от друга, то освобождающиеся на аноде при окислении электроны переносятся к катоду в зону восстановления через внешнюю цепь. Процессы электроосаждения пленок довольно сложны, так как на них влияет большое число трудно учитываемых факторов (степень пассивирования, структура и неоднородность поверхности, на которую осаждается пленка металла; характер адсорбции катионов, анионов и других частиц, а также скорость их переноса; режимы электролиза, влияющие на неоднородность концентрационного и электрического полей вблизи подложки и др.).
10.3. Химическое осаждение пленок из растворов и паровой фазы Химическое осаждение пленок из растворов
В сравнении с электрохимическим осаждением метод отличается большой простотой оборудования и проведения процесса. Метод основан на вытеснении металлов из растворов их солей или на восстановлении ионов металлов в растворах. Существуют четыре различных типа подобных реакций: некаталитические; каталитические; каталитические реакции в присутствии активаторов; каталитические реакции в присутствии активаторов и сенсибилизаторов.
Некаталитическиереакцииимеют место в том случае, когда некоторая поверхность погружена в восстановительный раствор. В состав рабочего раствора могут входить несколько компонентов: водные растворы солей одного или нескольких осаждаемых металлов; комплексообразователи; стабилизаторы растворов; буферирующие добавки; вещества, обеспечивающие необходимую кислотность растворов, и т.д.
Каталитические реакцииприменяют в случае затруднений при осаждении металлов на некоторые поверхности. Осаждаемый металл может осаждаться только на подложках из металлов, играющих роль катализаторов.
Каталитические реакции в присутствии активаторовприменяют в случаях неприменимости поверхностей металлов в виде катализаторов. В этом случае поверхность металла обрабатывается специальными веществами - активаторами. Активаторы применяют с целью понижения энергии активации, что стимулирует протекание реакций в отдельных точках на поверхности, причем эти точки становятся центрами роста осаждаемой пленки. Необходимое количество активатора в растворе обычно невелико и может составлять сотые доли процента.
Каталитические реакции в присутствии активаторов и сенсибилизаторов обычно применяют для нанесения покрытий на стеклянные или другие непроводящие поверхности. Перед активированием поверхности ее необходимо сенсибилизировать, т.е. «очувствить».