
- •11 Основные модели роста кристаллов
- •6. Физико-химические основы зарождения и роста новой фазы в виде тонких пленок в технологических процессах
- •6.1. Основные модели роста кристаллов
- •6.2. Атомная структура кристаллической поверхности. Классификация поверхностей
- •Дефекты поверхности
- •6.3. Движущие процессы кристаллизации Термодинамический анализ процесса зарождения
- •Молекулярно-статистическая модель зарождения
- •Кинетические модели зарождения
- •Коалесценция и образование сплошного слоя
6.2. Атомная структура кристаллической поверхности. Классификация поверхностей
Все кристаллические поверхности можно подразделить по их термодинамическим свойствам, атомному строению, особенностям кинетики процессов на них на три типа:сингулярные, вицинальные и диффузные, или несингулярные. Такую классификацию предложили Кабрера и Франк.
Рассмотрим классификацию с термодинамических позиций. Возможность такого рассмотрения основана на том, что различные кристаллические поверхности характеризуются различной поверхностной энергией σ. Это означает, что поверхностная энергия границы кристалла с любой средой анизотропна, т. е. зависит от кристаллографической ориентации этой границы. Основной вклад в поверхностную энергию вносят цепочкинаиболее сильных связей между атомами. По этой причинезначения σ минимальны для тех поверхностей, в которых находится наибольшее число цепочек сильных связей. Для простой кубической решетки это, прежде всего, грани куба (100). Они параллельны двум из трех систем цепочек связей между первыми ближайшими соседями и перпендикулярны цепочкам третьей системы, а также пересекаются всеми четырьмя системамицепочек вторых соседей.
Грани любой решетки, параллельные, по крайней мере, двум системам цепочек наиболее сильных связей, называют F-гранями; грани, параллельные одной такой системе, - S-гранями; грани, не содержащие ни одной из них, -К-гранями. Поверхностная плотность атомов обычно наибольшая для F-граней, поэтому они наиболее плотноупакованные. ОбозначенияF, S иК происходят от начальных букв английскихслов flat (плоский), stepped (ступенчатый) и kinked (покрытый изломами). Для термодинамического анализа используют зависимость поверхностной энергии от наклона при ориентации поверхности Р (рис. 6.4).
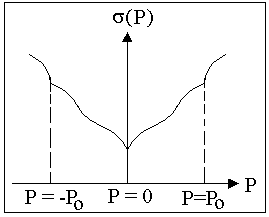
Рис.6.4. Зависимость энергии поверхности от ее кристаллографической ориентации
Поверхности, которым на зависимости поверхностной энергии от ее ориентировкиР отвечает острый минимум или излом (рис. 6.4, Р=0 и р = ±рo), называются сингулярными. Направления в непосредственной близости от ориентировки для сингулярной поверхности соответствуют вицинальным поверхностям. Для случая вицинальных поверхностей поверхностная энергия практически линейно изменяется с изменением ориентировки поверхности. Диффузная, или несингулярная, поверхность характеризуется тем, что ее поверхностная энергия плавно изменяется с изменением ориентировки.
С позиций атомного строения сингулярная поверхность представляет собой гладкую поверхность, на которой атомы поверхности располагаются в одной плоскости (рис. 6.5). Вицинальная поверхность состоит из плоских террас, высота которых зависит от наклона этой поверхности к сингулярной. Диффузная поверхность характеризуется наличием изломов.Изломы на такой поверхности распределены по всей площади равномерно и имеют значительно большую плотность, чем навицинальных гранях.
Различия рассмотренных типов поверхностей существенно влияют на процесс роста кристалла. Сингулярная поверхность может расти только за счет движения атомного слоя вдоль поверхности, тогда как несингулярная граница раздела междуфазами может перемещаться в направлении, перпендикулярном поверхности. Всем ориентировкам с рациональными миллеровскими индексами должны соответствовать острые минимумы на диаграмме изменения поверхностной энергии от ориентировки, и соответствующие им поверхности должны быть сингулярными.

Рис.6.5. Схемы профилей кристаллической поверхности: а - сингулярная; б – вицинальная; в – диффузная
Поверхности с другими ориентировками являются в этом случае вицинальными. Однако большинство из этих острых минимумов размывается из-за колебаний атомовуже при очень низких температурах, и сохраняются лишь наиболее важные минимумы, соответствующие поверхностям с более высокой симметрией решетки. В общем случае для всех граней должна существовать критическая температура, выше которой исчезает острый минимум поверхностной энергии; область перехода в этом случае увеличивается бы от одного до нескольких атомных слоев. Чаще всего все поверхности по своей атомной структуре подразделяются на атомно-гладкие (рис. 6.6, а) и атомно-шероховатые (рис.6.6, б). Атомно-шероховатой называют поверхность, на которой доля поверхностных узлов, занятых атомами и вакансиями, в первом приближении составляет ~50%.
Рассмотрим однокомпонентный кристалл с простой кубической решеткой, граничащей с паровой фазой. В случае атомно-гладкой поверхности граница между фазами составлена плоскостями, в которых идеальная упаковка атомов (или молекул) нарушена вакансиями и адсорбированными атомами. Края недоукомплектованных плоскостей образуют ступени. Следовательно, поверхности, ориентировка которых мало (на несколько градусов) отличается от ориентировки поверхностей с плотнейшей упаковкой, должны быть ступенчатыми всилу геометрической необходимости. Ступень — одномерная система и при температурах, отличных от абсолютного нуля, должна быть не прямолинейной, а извилистой, поскольку вследствие теплового движения атомы или молекулы могут покидать торец ступени (как и поверхностный слой) и переходить либо в окружающую среду, либо на поверхность.

Рис. 6.6. Схема атомной структуры поверхности: а – атомно-гладкая поверхность; б – атомно-шероховатая
Извилистость определяется изломами (рис. 6.6, а).Присоединение новой частицы к излому не ведет к его исчезновению и потому изломы называют активными местами роста. Это означает, что к излому присоединяетсябольшинство частиц, встраивающихся в кристаллическую решетку.
Аналогичный анализ структуры границы раздела кристалл - расплав требует уже определенной модели для жидкой фазы.
Наиболее проста решеточная модель, когда атомы жидкости считаются расположенными в той же решетке, что и в кристалле, но энергия их связей между собой Eж-жотлична от энергий связи атомов в кристаллеЕк-к и на поверхностираздела кристалл — жидкость Ек-ж.
Для рассматриваемой однокомпонентной системы кристалл — расплав при постоянном давлении в условиях фазового равновесия температура поверхности (и кристалла) равна температуре плавления. Равновесная структура поверхности в этом случае будет либо гладкой, либо шероховатой. В бинарной системе ситуация иная: меняя концентрацию компонентов расплава, можно менять как равновесную температуру, так иэффективную поверхностную энергию. Это может изменить атомную структуру поверхности кристалла. Расчеты для границы раздела однокомпонентный кристалл — идеальный бинарный растворпоказали, что, действительно, на линии ликвидуса фазовой диаграммы существует такая точка, по однусторону от которой поверхность атомно-шероховатая, а по другую — атомно-гладкая.
Процесс роста кристаллов с атомно-гладкими гранями происходит послойно путем тангенциального движения ступеней, причем непрерывность роста реализуется путем возникновенияступеней. Шероховатая поверхность равномерно покрыта изломами, и присоединение новых частиц происходит на ней практически в любом месте; грань растет в перпендикулярном направлении — нормальный механизм роста.
