
- •Тесты к модулю № 3
- •42. Какое соединение относится к гидроксикислотам?
- •2) Отрицательный -;
- •3) Нулевой
- •Определите пары энантиомеров среди приведенных ниже стереоизомеров аминокислоты треонина:
- •101 .Какое соединение образуется при декарбоксилировании фенилаланина н5с6–h2c–(nh2)hc–cooh:
- •109. Назовите продукт реакции:
- •2) Пировиноградная кислота;
- •3) Фумаровая кислота;
- •1) Этанол;
- •Какое из приведенных соединений обладает большими основными свойствами
- •2) Глицин
- •3) Холин
- •4) Этаноламин
- •1) Этаноламин;
- •2) Холин;
- •Укажите название приведенной ниже восстанавливающей биозы
- •Укажите систематическое название приведенной ниже восстанавливающей биозы
- •Укажите систематическое название приведенной ниже восстанавливающей биозы
- •1) Ксилит
- •2) Маннит
- •4) Сорбит
- •1) Сахарозы
- •1) Сахарозы
Определите пары энантиомеров среди приведенных ниже стереоизомеров аминокислоты треонина:
-
I
II
III
IV
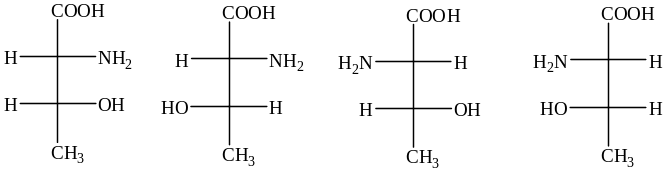
1) I и III; II и IV
2) I и II; III и IV
3) I и IV; II и III
4) I и II; II и III
91. Укажите формулу глутаминовой кислоты (2-аминопентандиовая кислота)
1) HOOC–H2C–(NH2)HC–CONH2;
2) H2N – (H2C)4 –(NH2)HC–COOH;
3) H2NOC–(H2C)2 –(NH2)HC–COOH;
4) HOOC – (H2C)2–(NH2)HC–COOH
92.Укажите формулу треонина (2-амино3-гидроксибутановая кислота)
1) HOH2C–(NH2)HC–COOH;
2) H3C–HOHC–(NH2)HC–COOH
3) HОH2C–(NH2)HC–COOH;
4) H2N–CH2–COOH
93. Какие из перечисленных аминокислот относят к гетероциклическим:
1) валин (2-амино-3-метилбутановая кислота);
2) фенилаланин (2-амино3-фенилпропановая кислота);
3) гистидин (2-амино-5-имидазолилпропановая кислота);
4) цистеин (2-амино3-меркаптопропановая кислота)
94. Какие аминокислоты обладают основными свойствами:
1) цистеин (2-амино3-меркаптопропановая кислота)
2) фенилаланин (2-амино3-фенилпропановая кислота)
3) треонин (2-амино3-гидроксибутановая кислота)
4) лизин (2,6-диаминогексановая кислота)
95. Какие аминокислоты обладают кислотными свойствами:
1) аспарагиновая кислота (2-аминобутандиовая кислота);
2) глицин (2-аминоэтановая кислота);
3) лейцин (2-амино-4-метилпентановая кислота);
4) фенилаланин (2-амино-3-фенилпропановая кислота)
96. В водном растворе аминокислоты существуют в виде:
1) катионной формы;
2) биполярного иона;
3) анионной формы;
4) равновесной смеси биполярного иона, катионной и анионной форм
97. Изоэлектрическая точка белка рI=5,5. Какой заряд имеет этот белок в растворе с рН=3,9?
1) положительный -
![]() ;
;
2) отрицательный -
![]() ;
;
3) нулевой
4) нейтральный
98. Изоэлектрическая точка аминокислоты - это значение PH, при котором:
1) концентрация катионных форм максимальна;
2) концентрация анионных форм минимальна;
3) концентрация биполярных ионов максимальна;
4) концентрация катионных и анионных форм максимальна
99. Карбоксильная группа α-аминокислот вступает в реакции:
1) с альдегидами;
2) с кислотами;
3) со щелочами;
4) с простыми эфирами
100. По карбоксильной группе аминокислота α-аланин взаимодействует:
1) с этиловым спиртом, C2Н5ОН
2) с йодистым метилом, СН3CI;
3) с азотистой кислотой, HNO2;
4) с уксусным ангидридом, (СН3СОО)2О
101 .Какое соединение образуется при декарбоксилировании фенилаланина н5с6–h2c–(nh2)hc–cooh:
1) 2-аминоэтанол;
2) фенилэтиламин;
3) фенилпропановая кислота;
4) 2-аминопропановая кислота
102. По аминогруппе α-аминокислот протекают реакции:
1) образования эфиров;
2) ацилирования;
3) этерификации;
4) образования амидов
103. γ-аминокислоты при нагревании подвергаются реакции внутримолекулярной дегидратации с образованием:
1) лактамов;
2) дикетопиперазинов;
3) ненасыщенных карбоновых кислот;
4) лактидов
104. Продуктом взаимодействия глицина H2N–CH2–COOH с уксусным альдегидом является соединение:
1) H2N–CН2–COOCН3; 2
2) H2C=N–CН2–COOH;
3) Н3С –HC=N–CН2–COOH;
4) H2N–CН2–CO–CН3
105. При взаимодействии α-аминокислот с альдегидами образуются:
1) эфиры;
2) замещенные имины (основания Шиффа);
3) кетокислоты;
4) галогенангидриды
106. Ксантопротеиновая реакция является качественной для обнаружения аминокислот:
1) серусодержащих;
2) ароматических и гетероциклических;
3) алифатических
4) непротеиногенных
107. Серусодержащие аминокислоты выявляют с помощью:
1) конц. HNO3;
2) р-ра Cu(OH)2;
3) Pb(CH3COO)2;
4) AgNO3
108. Предшественником биосинтеза α-аланина является:
1) молочная кислота;
2) ацетон;
3) пировиноградная кислота;
4) аминоэтанол.
