
- •Фармацевтична хімія
- •Вступ. Загальні положення про аналіз лікарських засобів
- •Методи аналізу лікарських препаратів
- •Загальні реакції на тотожність
- •Визначення функціональних груп
- •Питання для самоконтролю
- •Аналіз чистоти лікарських засобів
- •Кількісне визначення лікарських засобів
- •1. Похідні галогенів
- •1. Препарати гідроген пероксиду
- •Аналіз сполук вісмуту, цинку, купруму, аргентуму, феруму, платини і гадолінію.
- •Загальні реакції, які використовуються в аналізі
- •Сполуки купруму Купруму сульфат
- •Сполуки аргентуму
- •Колоїдні розчини срібла
- •Сполуки феруму Феруму сульфат
- •Органічні фармацевтичні препарати
- •Лікарські речовини – галогенопохідні вуглеводнів аліфатичного ряду
- •Хлороформ (Chloroformium)
- •Фізичні властивості
- •Йодоформ (Iodoformium)
- •Трийодметан
- •Добування
- •Етилхлорид (Aethylii chloridum)
- •Добування
- •Лікарські речовини – похідні спиртів
- •Спирт етиловий (Spiritus aethylicus)
- •У процесі отримання побічними продуктами можуть бути піровиноградна кислота, ацетальдегід, гліцерин, сивушні масла. Для очищення від домішок етиловий спирт переганяють.
- •Гліцерин (Glycerinum)
- •Лікарські речовини – феноли та їх похідні
- •Ф енол чистий (Phenolum purum)
- •Т имол (Thymolum)
- •Ф енолфталеїн (Phenolphtaleinum)
- •Д ля ідентифікації фенолфталеїну використовують реакцію з лугом, при додаванні якого розчин препарату забарвлюється у малиновий колір:
- •Лікарські речовини – похідні альдегідів
- •Розчин формальдегіду 40 %-вий (Solutio Formaldehydi) ф ормалін (Formalinum)
- •Х лоралгідрат (Chloralum hydratum)
- •Лікарські речовини – похідні карбонових кислот аліфатичного ряду
- •Калію ацетат (Kalii acetas)
- •Кальцію лактат (Calcii lactas)
- •Кальцію глюконат (Calcii gluconas)
- •Натрію цитрат (Natrii citras)
- •Лікарські речовини – амінокислоти аліфатичного ряду
- •Кислота глутамінова (Acidum glutamicum)
- •Ц истеїн (Cysteinum)
- •Лікарські речовини, похідні етерів
- •Питання для самоконтролю
- •Лікарські речовини, похідні естерів
- •Лікарські речовини – похідні барбітурової кислоти
- •Лікарські речовини– похідні ароматичних кислот та фенолокислот
- •К ислота бензойна (Acidum benzoicum)
- •С аліцилова кислота (Acidum salicylicum)
- •Н атрію саліцилат (Natrii salicylas) Натрію 2-гідроксибензолкарбоксилат
- •К ислота ацетилсаліцилова (Acidum acetylsalicylicum) Саліциловий естер оцтової кислоти
- •Зберігання
- •Ф енілсаліцилат (Phenylii salicylas) Феніловий естер саліцилової кислоти
- •Органічні фармацевтичні препарати – похідні ароматичних амінів
- •К сикаїн (Xycainum) Лідокаїн (Lidocainum)
- •П арацетамол (Paracetamolum)
- •Лікарські речовини, похідні біс-(β-хлоретил)аміну
- •Сарколізин
- •Лікарські речовини – похідні ароматичних амінокислот
- •А нестезин (Anaesthesinum)
- •Новокаїн (Novocainum)
- •Дикаїн (Dicainum)
- •Лікарські речовини – похідні піразолу
- •Ф еназон (Phenasone)
- •Метамізолу натрієва сіль (Metamizolum natricum) а нальгін (Analginum)
- •Лікарські речовини – похідні гідразиду ізонікотиновоі кислоти
- •Лікарські речовини – похідні 8-оксихіноліну
- •Лікарські речовини з групи алкалоїдів
- •Загальні алкалоїдні реактиви:
- •Спеціальні алкалоїдні реактиви:
- •Похідні тропану
- •А тропіну сульфат (Atropini sulfas)
- •Скополаміну гідробромід (Scopolamini hydrobromidum)
- •Похідні хіноліну : хінін та його солі
- •Хімічні властивості і аналіз якості
- •Похідні бензилізохіноліну : папаверіну гідрохлорид
- •П апаверину гідрохлорид (Papaverini hydrochloridum)
- •Похідні фенантренізохіноліну
- •М орфіну гідрохлорид (Morphini hydrochloridum)
- •Е тилморфіну гідрохлорид
- •Похідні імідазолу: пілокарпіну гідрохлорид, дибазол, метронідазол, клонідину гідрохлорид п ілокарпіну гідрохлорид
- •Похідні пурину
- •Т еобромін (Theobrominum)
- •Лікарські речовини – вітаміни
- •Тотожність
- •Тотожність
- •Лікарськіречовини групи антибіотиків та їх напівсинтетичних аналогів
- •І. Метацикліну гідрохлорид (Methacyclini hydrochloridum). Рондоміцин.
- •Іі. Антибіотики ароматичного ряду Левоміцетин
- •IV. Цефалоспорини
- •V. Антибіотики – глікозиди Стрептоміцину сульфат (Streptomycini sulfas) (дфу)
- •VI. Антибіотики – аміноглікозиди
- •Viі. Лінкоміцини Лінкоміцину гідрохлорид (Lyncomycini hydrochloridum) (дфу)
- •Т ерпінгідрат
- •К амфора
- •Б ромкамфора.
- •Лікарські речовини - комплексоутворюючі сполуки
- •Ф ерамід
- •Етилендіамінтетраацетати
- •Препарат добувають конденсацією етилендіаміну з надлишком монохлороцтової кислоти:
- •О сарсол
- •Металоорганічні сполуки.
- •М еркурійсаліцилова кислота
- •Лікарcькі речовини, продукти переробки нафти
- •Лікарські речовини – гормони та гормоноподібні препарати
- •Гормони мозкового шару наднирників
- •Гормони стероїдної структури
- •1. Реакції, які ґрунтуються на відновних властивостях препаратів:
- •Дезоксикортикостерону ацетат
- •Кортизону ацетат
- •Преднізолон (Prednisolonum)
- •Статеві гормони
- •Андростан
- •Прогестерон (Progesteronum)
- •Література
- •Фармацевтична хімія
- •За загальною редакцією професора і. Ф. Мещишена Українською мовою
Лікарські речовини – феноли та їх похідні
Феноли, на відміну від спиртів, є похідними ароматичних вуглеводнів, що містять в молекулі одну або декілька гідроксильних груп, безпосередньо пов’язаних з ароматичним ядром. За числом гідроксильних груп розрізняють одноатомні, двоатомні та триатомні феноли:
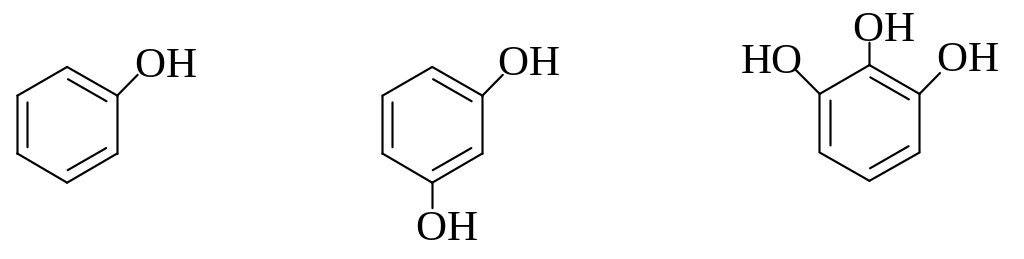 Фенол
Резорцин
Пірогалол
Фенол
Резорцин
Пірогалол
Хімічні властивості фенолів зумовлені як наявністю в молекулі гідроксильної групи з рухливим атомом водню, так і ароматичними властивостями бензольного ядра. Внаслідок взаємодії електронної пари атому кисню гідроксильної групи з π-електронами ароматичного ядра феноли проявляють (на відміну від спиртів) кислотні властивості.
При розчиненні в лугах феноли утворюють феноляти:
Р озчини
фенолятів у воді дуже сильно гідролізовані
і нейтралізуються навіть диоксидом
карбону. Тому карбонати лужних металів
не утворюють феноляти. Цим феноли
відрізняються від кислот.
озчини
фенолятів у воді дуже сильно гідролізовані
і нейтралізуються навіть диоксидом
карбону. Тому карбонати лужних металів
не утворюють феноляти. Цим феноли
відрізняються від кислот.
Феноли легко вступають у реакції конденсації, які використовують для аналізу препаратів фенолів, а також для добування їх похідних (фенолфталеїн, флуоресцеїн).
Наявність фенольного гідроксилу в молекулі надає специфічні хімічні властивості цим сполукам. Більшість з них легко окислюються навіть киснем повітря. Нижчі феноли при окисленні киснем змінюють забарвлення (до жовтого або червоного).
Подібно до спиртів феноли можуть утворювати прості та складні ефіри. Реакцію етерифікації застосовують для добування ліків похідних фенолів, а реакцію омилення – для їх аналізу.
На відміну від бензолу фенол легко вступає в реакцію заміщення, утворюючи галоген-, нітро-, сульфопохідні та ін. При цьому заміщуються атоми гідрогену, розташовані в орто- і пара-положенні по відношенню до фенольного гідроксилу. Ці реакції використовуються для аналізу препаратів фенолів і синтезу їх похідних.
В медичній практиці застосовують препарати: фенол чистий, тимол, а також похідне фенолу – фенолфталеїн.
Ф енол чистий (Phenolum purum)
Фізичні властивості
Фенол чистий – це безбарвні, тонкі, довгі голкоподібні кристали або кристалічна маса своєрідного запаху. Температура кипіння 178-182°С; температура затвердіння не нижче 39,5°С. Під впливом світла та кисню фенол легко окислюється і набуває рожевого забарвлення. Препарат добре розчинний у воді, спирті, ефірі і жирних оліях.
Добування
Ф енол
добувають сульфуванням бензолу з
подальшим лужним плавленням :
енол
добувають сульфуванням бензолу з
подальшим лужним плавленням :
Тотожність
1. Кольорова реакція з феруму (ІІІ) хлоридом.
Розчин фенолу при додаванні до нього розчину феруму (ІІІ) хлориду забарвлюється в синій або фіолетовий колір. Тимол, через просторові утруднення в молекулі, не утворює забарвлених продуктів з розчином феруму (ІІІ) хлориду .
2. Реакція окиснення (реакція індофенолової проби)
При дії на фенол гіпохлоритів або бромної води в присутності аміаку утворюється індофенол і розчин забарвлюється у синій колір:
 Індофенол
Індофенол
3. Реакції заміщення.
При взаємодії розчину фенолу з бромною водою утворюється білий осад 2,4,6-трибромфенолу:
К ількісне
визначення
ількісне
визначення
1. Для кількісного визначення фенолу ДФХ рекомендує броматометричний метод. Визначення проводять зворотним титруванням 0,1н. розчином калію бромату в присутності калію броміду:
Н адлишок
титрованого розчину калію бромату
призводить до утворення еквівалентної
кількості брому. Надлишок брому
встановлюють йодометрично:
адлишок
титрованого розчину калію бромату
призводить до утворення еквівалентної
кількості брому. Надлишок брому
встановлюють йодометрично:
2
 .
Кількісно фенол можна також визначати
йодометричним методом. Відбувається
йодування фенолу надлишком титранту:
.
Кількісно фенол можна також визначати
йодометричним методом. Відбувається
йодування фенолу надлишком титранту:
Надлишок йоду титрують розчином натрію тіосульфату.
Зберігання
Фенол зберігають в добре закритій тарі, в місці, захищеному від світла, під впливом якого в присутності кисню повітря препарат окиснюється, набуваючи рожевого забарвлення. Фенол зберігають із застереженням за списком Б.
Застосування
Фенол застосовують в якості антисептичного засобу. Розчин фенолу (3-5%) застосовують головним чином для дезинфекції (інструментів, білизни і т.п.). Для лікування шкірних захворювань його призначають рідко через його токсичність. Фенол застосовують у фармацевтичній практиці в якості консерванту деяких рідких лікарських форм.
