
- •Конспект лекций по дисциплине «Коллоидная химия»
- •Значение коллоидной химии
- •Основные признаки дисперсных систем
- •Изменение удельной поверхности
- •Классификация дисперсных систем
- •Классификация дисперсных систем по
- •Лекция 2. Получение коллоидных систем (кс) и их очистка.
- •Методы конденсации.
- •Методы диспергирования.
- •Метод пептизации.
- •Очистка коллоидных растворов.
- •Очищаемый раствор, 2 – растворитель (вода),
- •Оптические свойства коллоидных систем.
- •Броуновское движение.
- •Диффузия
- •Осмотическое давление коллоидных растворов.
- •Седиментация в дисперсных системах.
- •Оптические свойства дисперсных систем
- •Явление рассеяния света.
- •Поглощение (адсорбция) света.
- •Теории образования и строения дэс.
- •Электрокинетический потенциал.
- •Влияние электролитов на электрокинетический потенциал
- •Строение мицеллы.
- •Электрокинетические явления.
- •Коагуляция
- •Действие электролитов на коагуляцию
- •Совместное действие электролитов при коагуляции
- •Теория устойчивости гидрофобных дисперсных систем длфо
- •Скорость коагуляции
- •Концентрации электролита
- •Старение золей
- •Защитное действие молекулярных адсорбирующих слоев
- •Оценка пн жидкостей из родственных характеристик
- •Межфазное натяжение на поверхности раздела твердое тело-жидкость. Смачивание.
- •Краевой угол является мерой смачивания. Он определяется как угол между твердой поверхностью и касательной в точке соприкосновения трех фаз. Угол отсчитывается в сторону жидкой фазы.
- •Адсорбция. Изотерма адсорбции. Уравнение Гиббса.
- •Построение изотермы адсорбции и нахождение величин .
- •Теории адсорбции.
- •Комплекс
- •Полимолекулярная сорбция
- •Частные случаи адсорбции. Адсорбция на границе жидкость-газ.
- •Адсорбция на границе раствор-газ
- •Применение пав
- •Адсорбция на границе твердое тело-раствор
- •Молекулярная адсорбция из растворов
- •Влияние природы среды
- •Ионная адсорбция
- •Обменная адсорбция
- •Адсорбция на границе твердое тело-газ
- •Системы (молекулярные коллоиды)
- •Общая характеристика растворов полимеров
- •Набухание полимеров
- •Осмотическое давление и вязкость растворов полимеров
- •- Для раствора низкомолекулярного вещества;
- •Классификация студней
- •Условия образования студней
- •Механизм процессов гелеобразования и структура полимерных гелей
- •Реология гелей
- •Реологические теории.
- •Теория Эйринга
- •Структурные теории.
- •Гидродинамические теории
- •Теория Грессли
Теории адсорбции.
Теория мономолекулярной адсорбции. Лэнгмюр - американский физико-химик, 1915г.)
В теории Лэнгмюра исходят из следующих положений:
Адсорбция является локализованной и обеспечивается силами, близкими к химическим, таковыми Лэнгмюр считал все силы, обеспечивающие когезионную прочность вещества.
Адсорбция протекает на активных центрах поверхности.
В результате адсорбции образуется мономолекулярный слой адсорбтива на поверхности.
Адсорбция сопровождается десорбцией, т.е. молекулы могут через время отрываться от поверхности. Их место занимают новые молекулы. Время пребывания молекул адсорбтива в адсорбированном состоянии зависит от температуры.
Процесс адсорбции представляется как образование адсорбционного комплекса между адсорбентом и адсорбтивом:
адсорбтив + адсорбент адсорбционный
Комплекс
Исходя из приведенных положений Лэнгмюр получил уравнение адсорбции, которое имеет вид:
![]() (гиперболическая функция)
(гиперболическая функция)
где
![]() -
величина адсорбции;
-
величина адсорбции;
![]() -
емкость адсорбционного монослоя, или
число адсорбционных центров, приходящихся
на единице площади поверхности или на
единицу массы адсорбента.
-
емкость адсорбционного монослоя, или
число адсорбционных центров, приходящихся
на единице площади поверхности или на
единицу массы адсорбента.
Для сорбции газов и паров, уравнение Лэнгмюра имеет вид:
![]() .
.
Т
Г
Г![]()


с (р)
Рис. 7.2. Изотерма адсорбции Лэнгмюра.
Уравнение Лэнгмюра преобразуется в уравнение прямой:
![]()
Такая зависимость позволяет графически
определить оба постоянных параметра
адсорбционной изотермы. На рис. 7.3
представлена типичная изотерма адсорбции
в линейных координатах. Экстраполяция
зависимости до оси ординат дает отрезок
равный
![]() ,
а тангенс угла наклона прямой равен
,
а тангенс угла наклона прямой равен
![]() .
.
![]()

![]()
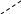

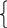

Рис. 7.3. Изотерма адсорбции Лэнгмюра в прямолинейных координатах.
Изотерма адсорбции может иметь ступенчатый вид:
Г


Рис. 7.4. Изотерма ступенчатой адсорбции
Изотерма адсорбции Фрейндлиха (1880-1941гг., немецкий физико-химик).
Представления Лэнгмюра идеализируют и упрощают действительную картину адсорбции. В действительности поверхность большинства адсорбентов неоднородна и адсорбция не ограничивается образованием мономолекулярного слоя, вследствие чего уравнение адсорбции усложняется.
Фрейндлих предположил, что адсорбция зависит от давления и концентрации и предложил эмпирическое уравнение, которое имеет вид степенной функции:
![]() или
или
![]() ,
,
где
![]() - масса адсорбированного вещества, п
- масса адсорбированного вещества, п
иходящаяся на 1 г адсорбирующего материала, г.;
![]() - давление;
- давление;
![]() - концентрация;
- концентрация;
![]() и
и
![]() - константы, которые не имеют физического
смысла и играют роль подгоночных
коэффициентов. Для большинства случаев
- константы, которые не имеют физического
смысла и играют роль подгоночных
коэффициентов. Для большинства случаев
![]() .
.
В логарифмической форме уравнение имеет вид:
![]() ,
,
т.е.
сорбция выражается линейной зависимостью.
Наклон прямой прямо пропорционален
,
на оси ординат отсекается отрезок,
равный
![]() .
.
Позже Зельдович теоретически вывел уравнение, эмпирически предложенное Фрейндлихом.
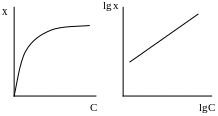
Рис. 7.5. Изотермы адсорбции Фрейндлиха.
