
- •Глава I
- •Потребление этиленпропиленовых каучуков в основных капиталистических странах, тыс. Те
- •Растворимость (%) полиэтилена, полипропилена и этиленпро-пиленового сополимера в различных растворителях
- •1) Образование нестабильных ванадиевых соединений
- •Изменение содержания этилена в сополимере в зависимости от парциального давления водорода
- •Сравнительные данные расчет того и экспериментального состава скэпт
- •Влияние различных каталитических систем на относительные активности этилена и пропичена
- •Свойства вулканизатов в зависимости от содержания водорода в газовой фазе
- •5Тилсн в жидкой фазе, мол, 96
- •5. Сополимеризация этилена в 4-метилпентеном-1
- •6. Получение эластомеров на основе этилена и гексена-1
- •VoCl3-f дибах
- •7. Некоторые особенности этилен- а -0лефин0выл эластомеров
- •FAcAc;3v-f дибах
- •Глава III
- •1. Вулканизация скэп в присутствии перекиси дикумила
- •2.Радиационная вулканизация
- •3 Переработка двойных скэп
- •5 Модификация скэп
- •Глава IV
- •1. Этилиденнорборнен
- •3. Димеризация и содимеризация диенов
- •4. Теплостойкость скэпт
- •6. Способы производства этиленпропиленовых эластомеров
- •7. Определение состава этилен-?-олеф и новых сополимеров
- •8. Деструкция этиленпропиленовых сополимеров
- •Сеидов h. M., Далин m. А., Бахши-Заде а. А., Арутюнов и. А., Кам-
- •Каучков
- •Глава I. Производство и потребление этиленпропиленового каучука 5
- •Глава 11. Сополимеры этилена с а-олефинами 12
- •Глава 111: Вулканизация этиленпропиленового эластомера ....
- •Глава IV: Ненасыщенные этиленпропиленовые эластомеры ... 13.
ВУЛКАНИЗАЦИЯ
ЭТИЛЕНПРОПИЛЕНОВОГО
ЭЛАСТОМЕРА
СКЭП
является полностью насыщенным аморфным
продуктом. Отсутствие двойных связей
в макромолекулярной цепи этиленпропиленового
сополимера обусловливает высокую
стойкость полимера к окислению, к
действию повышенной температуры и
химических агентов, с одной стороны,
невозможность сшивания под действием
обычных вулканизующих агентов,
применяемых в случае непредельных
эластомеров, — с другой.
Существует
несколько методов вулканизации
насыщенных эластомеров, из которых
наиболее распространена вулканизация
органическими перекисями [307].
Гидроперекисные соединения для этой
цели непригодны: они опасны в обращении,
являются неэффективными сшивающими
агентами, сочетание их с перекисными
соединениями нарушает структурирующее
действие последних. Эффективны такие
перекисные соединения, которые
стабильны и безопасны при обработке
на резиновом оборудовании (вальцы,
резиновые смесители, каландр) и легко
разрушаются в интервале температур
вулканизации.
Разложение
перекисей обычно происходит под
действием температуры, облучения
светим, излучения высокой энергии или
же при реакции с другими веществами.
Обычно распад перекисей типа Х:У
(ковалентно
связанных) можно представить в 3
направлениях:
Х+
+
У X :
У - Х~
+
У+
I
хт
+
у-
гетеролнтический
гемолитический гетеролитическин
распад распад распад
Известно,
что механизм вулканизации насыщенных
эластомеров является радикальным
процессом, поэтому наибольший интерес
представляют такие перекиси, у которых
преобладает гемолитическое разложение.
Скорость
вулканизации в основном зависит от
скорости распада перекисей на
радикалы, стабильность которых
обусловлена преимущественно характером
углеродных атомов, с которыми они
связаны. Перекиси у первичного углеродного
атома разлагаются при низких
температурах. В присутствии вторичных
углеродных атомов повышается
стабильность органических перекисей,
однако температура их разложения в
большинстве случаев лишь немного выше
комнатной. Поэтому эти перекиси также
не находят применения для вулканизации
каучуков. Наиболее
стабильны
такие органические перекиси, у которых
перекисные группы связаны с третичным
углеродным атомом. Стабильность нх
достаточна для практического пользования.
Электродонор-ные заместители у перекисных
групп (например,—ОН, —СН3)
приводят
к понижению стойко- -св.о,
сти,
а электроакцепторные (па-
пример,
С1), наоборот обуслов- ^-
ливают
повышенную стойкость ~ перекисных
соединений.
Таким
образом, быстро разлагающиеся
перекиси, которые имеют низкую температуру
распада (перекись бензола,третичный
бутилпербензоат), являются
неэффективными вулканизующими
агентами, так как они
разлагаются
при относительно Рис.
40. Период
полураспада перенизких
температурах и при ис- кисеи:
/—перекись бензоила, 2—
пе-пользовании
их наблюдается Рекись
д^У-^а,
3-2,5-бис-(третбу-
тилперокси!-2,5-диметилгексан,
4—
преждевременная
вулканиза- 2,5-Диметил-2,5-ди-(третбутил-перок-
ция.
Эффективны же третичные сигексин-3)
алкилперекиси,
например, ди-
кумил-,
третбутилкумил, дитретбутил—перекиси
и т. д.
В
инертных растворителях был определен
период полураспада различных
перекисных соединений [307,308] (рис. 40).
Радикалы, образующиеся при разложении
перекисей, имеют высокую реакционную
способность и эффективно вулканизуют
этиленпропиленовые каучуки. Для
сшивания насыщенных полимеров
наиболее широко используется перекись
дикумила.
Перекись
дикумила можно синтезировать нагреванием
диме-тилфенилкарбинола с гидроперекисью
изопротшлбензола при температуре 95°С
без катализатора [309]:
СН3 СН3
^\.-С-ОН-г
ОН-О-С- /\
1 I
"
СН3 СН3
СН3 СН3
^\-с-о-о-с-^\
I
II
1
1
СН3
сн,
н2о.

Глава III
1. Вулканизация скэп в присутствии перекиси дикумила

Чистая
перекись дикумила представляет собой
кристаллический продукт с температурой
плавления ЗГС. При длительном нагревании
до 100°С не разлагается, дальнейшее же
повышение температуры сильно активизирует
разложение. По данным [307], период
полураспада перекиси дикумила составляет
744 мин
прн
115°С; 110 мин
при
149°С; 0,7 мин
при
177°С; 0,1 мин
при
193°С.
В
процессе вулканизации СКЭП перекись
дикумила под действием температуры
разлагается с образованием свободных
кумилокси-радикалов по схеме:
СН3 СН3
СН3
I
-с-о-
I
СН3
сн.
Образовавшиеся
кумилокси-радикалы отрывают водород
от молекулы этиленпропиленового
сополимера, образуя полимерные
радикалы, которые рекомбинируют
между собой,
а сам радикал превращается в кумиловый
спирт:
~СН2-СН2--СН2-СН2-
Таким
образом в процессе вулканизации
образуются побочные продукты:
кумиловый спирт, ацетофенон, метан.
Помимо
основной реакции структурирования
СКЭП в процессе вулканизации имеет
место также и Ь-распад
полимерных цепей:
~СН2-СН-СН2-СН,:
СН2—
С -СН2-СН2~
-
! ! t
I
СН3 СН3
-
— СН2-СН-СН2-СН2~
-г сн2
- с-сн2-сн2~
I I
СН3 СН3
Несмотря
на низкую концентрацию полимерных
радикалов (10~(i
молей)
во
время вулканизации наблюдается
интенсивное стуктурирование
этиленпропиленового сополимера.
Робинсоном с сотрудниками [310] такое
эффективное структурирование объясняется
близким расположением друг к другу в
момент реакции 2 полимерных радикалов,
получаемых в разультате разложения
одной молекулы перекиси. Эффективность
структурирования этиленпропиленового
сополимера существенно зависит от его
состава. Повышение содержания пропилена
от 30 до 75% вес. приводит к уменьшению
модуля, твердости, прочности на разрыв
и увеличению удлинения при разрыве,
напряжения деформации (табл. 58).
\-C-0-
-о-с-сн
сн3
I
-с-о-
I
-
СН3
СН3
I
-сн-сн,
сн3
!
-сн--сн-
I
сна
сн9
-сн2--сн2-
-сн2—
-сн2~+2
-сн-сн,-сн9
сня
сня
сн.
— ~СН2—СН2—
сн—сн,—сн.>—сн—сн2—сн2
I
- СН2
- СН2
- СН - СН2
— СНо-СН—сы,-сн
Во
время вулканизации часть кумилокиси-радикалов
распадается на ацетофенон и метальные
радикалы. В свою очередь, метальные
радикалы также отрывают атом водорода
от полимерной цепи и превращаются
в метан
СН,
■^-С
--= О
1
I +сн3.
СН,
Такое
существенное влияние состава сополимера
на эффективность вулканизации
вызывает изменение механизма
свобод-норадикальной реакции, приводящее
к повышению поперечных связей [311].
Рассмотрим
данные анализа продуктов разложения
перекиси дикумила:
+
х
х—с—о-
СН,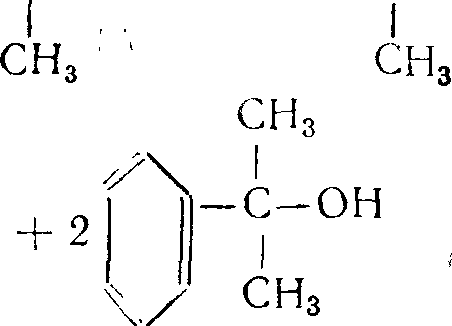

СКЭП,
мол. % пропилена
25
50
100
Перекись
дикумила, моль
0,286
0,286
0,286
Полученные
продукты, моль
Кумиловый
спирт
0,130
0,149
0,091
Ацетофенон
0,192
0,175
0,150
Метан
0,172
0,209
0,197
Как
видно, количество этих продуктов
изменяется в зависимости от содержания
пропилена в сополимере. Согласно данным
[1],
при
распаде перекиси дикумила в минеральном
масле при повышенной температуре кроме
указанных продуктов выделяются
также ацетон и с-метилстирол.
Наполнители
и другие ингредиенты смеси могут также
существенно влиять на характер
перекисной вулканизации. Если, например,
наполнитель является активным донором
протонов и способен насыщать радикалы
перекиси до начала дегидрирования
СКЭП, то это может частично или полностью
исключить возможность сшивания. Поэтому
выбор составных частей резиновых
смесей должен быть произведен очень
тщательно. Следует учитывать также
индивидуальные структурные особенности
перекиси [312].
Так,
перекиси, содержащие кислотные группы
(например, перекись бензоила), менее
чувствительны к кислым ингредиентам
резиновой смеси, чем перекиси без
кислотных групп (например, перекись
дикумила). Поэтому при применении
перекиси дикумила в качестве
вулканизирующего агента не рекомендуют
вводить минеральные наполнители и
канальные сажи, поверхностная
кислотность которых способствует
гетероли-тическому расщеплению перекиси,
что нарушает процесс вулканизации.
В
большинстве случаев перекисные
соединения в резиновую смесь вводятся
не в чистом виде, а вместе с инертными
наполнителями, в качестве последних
можно использовать карбонат кальция,
например, дикуп-40—40%-ная перекись
дикумила с карбонатом кальция. Такой
же подход требуется и для подбора типа
мягчителей, в качестве которых
рекомендуется применять алифатические
неразветвленные продукты.
Перекись
дикумила, несмотря на широкое применение
для вулканизации этиленпропиленового
эластомера, имеет следующие недостатки:
Чувствительность
ко многим компонентам резиновой
смеси (каолин, ароматические
масла, некоторые антиоксиданты и
др.), в результате чего нарушается
процесс вулканизации, это затрудняет
применение многих ингредиентов
для улучшения того или иного
свойства вулканизата.
Как
известно, скорость вулканизации
зависит от скорости разложения
перекисей; для перекиси дикумила
оптимал'-"^ впе-
мя
вулканизации
при данной температуре в 5—10 раз больше,
чем скорость полураспада перекиси
дикумила.
3.
В
результате образования побочных
продуктов (ацетофенон, кумиловый
спирт) при разложении перекиси дикумила
в
процессе
вулканизации вулканизаты этиленпропиленового
каучука имеют трудноустранимый
неприятный запах.
Это
обусловило интенсивные исследования
в области синтеза новых перекисей,
которые увеличивают скорость вулканизации
и способствуют получению вулканизатов
этиленпропиленового сополимера и
гораздо меньшим запахом. К числу таких
перекисей относятся циклические
моно- и диперекиси общей формулы {313].
R
R
R
Ю—0-Х
-о-о—
Ненасыщенные
диперекиси этиленового [314] и ацетиленового
1315] типов
R
R R
R
(CH3)s-C-0-0-C-CH С-С-О-О-С
(СН3)3
I' II!
(СНз)3-С-0-0-С-СН С-С-О-О-С
(СН3)3
/\ /\
R
R R
R
обеспечивают
протекание вулканизации за 25—70 сек
и
очень удобны для получения вулканизатов
в кабельной промышленности.
В
табл. 59
приведены
основные перекиси, используемые при
вулканизации СКЭП. Применяются и другие
перекисные соединения, предложенные
различными фирмами [316]. К их числу
относятся 2,5-диметил-2,5-ди-
(требутилперокси) -гексан (варокс 50);
2,2-бис-4,4-бис-(третбутилперокси)-циклогексинпропан
(пер-кадокс 12/40);
з,а -ди-(требутилперокси)-1,4-диизопропилбензол
перкадокс 14);
перкадокс
14/40; нироксимон-1—40;
1,1-бис-(третбутилперокси)-«3,3,5-триметилциклогексан
(тригонокс 28/40); н-бутиловый эфир
3,3-ди-(третбутилперокси)-масляной
кислоты (тригонокс 17/40); перекись
третбутилкумила (тригонокс-50);
ДБЦ-1,1-ди-(третбутилперокси)-циклогексан;
циклогексиловый эфир оксиметилтретбутилперокси.
Смеси СКЭП с указанными перекисями
обладают высокой скоростью вулканизации
даже при температуре 130—140°С.
R
R
R
R
или
-О-О—
Продолжение
табл.59
Днкуп
на инертном накополни-теле
Люперко
101XL
иа
инертном
на-нолнителе
Люперко
130ХЬиа инертном капол-
Перекись
дитретбутила
СН3 Снз
I I
НВС,-С—0-0-С-СвН5
! I
СНз СНз
СН,
н3с-с-сн3-сн2-с
-СН3
I I
о о
A
i
[ I
Н3С-С-СН3
Н3С-С-СН3
сн2
сн,
Н3С-С-С=С_С-^-СН3
4
4
i о
I
I
нас-с-снэ
н3с-с-сн,
СНз СНз
СН3 СН3
Н3С—С—О—О—С—сн3
! I
СНз СН3
сн.
СН,
сн.
Перекись
дикумила
2,5-Днметил-2.5-дн-(
трет бутнлп ерокси)-гексан
2,5-Диметнл-2,5-ди-(трет-
бутилперокси)-гек-
сан-3
Перекись
дитретбутила
о
со
«О
S
£
К
■л
CU
с
а>
с
s
S
Я
5"
_ X О
х
-е-
м
<и
а4
О
О
о
ч
СП
с
о
U
к
о
с
LO
ос
со
ю
— CN
CN
—■
Ю
CN
—'
CN
о —'
cd
t ^ tp
Таким
образом, в зависимости от типа и
количества перевей можно изменить
в широких пределах скорость вулканизации
и скорчинга.
В
табл. 60 показаны свойства вулканизата
СКЭП с различными перекисями.
Представляют
интерес также перекиси, содержащие
более одной иерекисной группы, например,
алифатические или цикло-алифатические,
которые придают очень слабый запах
вулкани-затам, полученным на их основе
[317].
В
работе Рапчинской, Блох и др. [318] изучено
влияние азотсодержащих перекисей
на структурирование СКЭП. Исследовалось
структурирующее действие ряда
перекисей—N-третбутилпе-рокеиметилпиперидина,
диизопропилтретбутилпероксиметила-мина
и др. Полученные вулканизаты характеризуются
высокой плотностью поперечных связей,
отсутствием реверсии.
Резиновые
смеси обладают сравнительно высоким
сопротивлением к под вулканизации
при 120°С. Устойчивость этих смесей
значительно увеличивается, если перекиси
вводятся на цеолитах. Показано, что
такое введение перекисей облегчает
равномерное распределение их в
смеси, а также позволяет в значительной
мере избавиться от неприятного запаха,
характерного для перекисных вулканизатов.
со
Is-"



С g
(Т) <
К о
U с
да та
о о.
л s
* §
Я О
g S
да н
л т
X к
£ «,
си
о
и a
s
оз
(-и
«я
о в о
с
с—
ngtr
CU
О
U
о
CO
4<J
m
^ to
л
— н
Ss
H
к
§1
s
«5
со
— CN
3
о
о со
s
1
с
3-
^
cu
cu
в
к
ч
cu
S
<-»
n
=
«
X
я
о
о
ф о
я
в с
о о
о л
s
га ■
га к
° >,
н сс
га w
cj *
О СП
о.
с
с с
Влияние
соагента на перекисную вулканизацию
При
перекисной вулканизации Js-распад
полимерных цепей приводит к разрушению
макрорадикалов, вследствие которого
уменьшается эффективность структурирования
этиленпропиленового эластомера.
Это отрицательно сказывается на
физико-механических свойствах
вулканизатов. Для устранения этого
явления вулканизацию проводят в
присутствии небольшого количества
веществ, называемых соагентами
вулканизации.
Введение
небольших количеств соагента увеличивает
эффективность вулканизации,
способствует как образованию свободных
радикалов, так и сшиванию полимерных
цепей, устраняется и неприятный
запах вулканизата.
К
кислу таких соагентов относится сера.
С увеличением количества серы
степень структурирования быстро
возрастает и Достигает максимума при
концентрации серы 0,2% от веса полимера.
Дальнейшее увеличение количества серы
способствует росту скорости вулканизации
[319].
По
мнению Натта с сотрудниками, роль серы
заключается в Защите этиленпропиленового
эластомера от деструкции. Более
"^дробное исследование механизма
действия серы совместно с
си
s
к
си
S
Si
g-s
о
*
и
09
•oJoHoJHdx
![]()
перекисями
в модельных реакциях показало, что роль
серы » процессе вулканизации более
сложная.
В
качестве модельной системы для выяснения
механизма вулканизации Вей [320] использовал
взаимодействие соединений состоящих
из 2,4-диметилпентена, серы и
дитретбутилперекиси Анализ показал,
что основными продуктами реакции (80%)
яй.
ляются
полисульфиды типа:
_
C7H15-S5-C7H15)
C7Hls-S4-C7HIr,
C7H,5-S,-C7H1„
V
C7H15-S2-C7H15,
C7H15—Sj-QH9,
C4H9-S3-C<H9.
Моносульфиды
в
продуктах
реакции
не обнаружены.
Таким
образом, механизм перекисной вулканизации
с участием серы можно представить
следующим образом. Кумилокси-радикалы,
образующиеся при распаде перекиси,
отрывают водород от молекулы полимера
и образуют полимерные радикалы:
ROOR
-
2RO',
RO-
-f-
RH
ROH4
R-.
Затем
полимерный радикал взаимодействует с
элементарной серой, образуя персульфенильный
радикал R—S,,
или
вступает во взаимодействие с
полисульфидами. В итоге уменьшается
степень сульфидности поперечных связей.
Персульфенильные
радикалы могут присоединяться к двойным
связям, возникающим в полимерных цепях
в результате протекания реакции
диспропорционирования: образуются
полисульфидные радикалы с неспаренным
электроном у углеродного атома, способным
оторвать водород от молекул исходного
полимера:
R'
+
S. RSZ
R"
+
RS,R
-
RSrR
+
RSy
где
z
=
x
+
у Обрыв цепи происходит рекомбинацией
полимерных радикалов с образованием
поперечных связей и полисульфидных
мостиков:
xyRS,R-
RS
4-
R
z
^RS7H-r-R"
основная
реакция
RS.;
+ RSV
-
RS,R
/R-R
2R\
XRH
+
R'
-'основная
реакция.
Однако
вулканизующая система с
применением
перекиси дикумила и серы имеет
существенные недостатки—неприятный
за*
пах, малая скорость
вулканизации и
т.
д. Поэтому рядом иссле'
дователей
[321,322] предприняты попытки применять в
качестве соагентов перекисной
вулканизации этиленпропиленовых
каучуков различные органические
соединения с одной или несколькими
функциональными группами, отличающимися
небольшой упругостью пара при повышенной
температуре. Среди них монофункциональные
мономеры: винилтолуол, винилпиридин,
цикло-гексилметакрилат, акриловая
кислота, хонондиоксим, динитро-бензол,
дифенилгуанидин, диаллилмеламин;
полифункциональные мономеры:
этилендиметакридат, полиэтиленгликольдиме-такрилат
Р-211, триметилпро-пантриметакрилат,
аллилмета- " " '
крилат,
дивинилбензол, диал- w
j
лилтоконат,
триаллилцианурат, ^//2;-
диаллилфталат,
дивинилади- ^ пат; полифункциональные
по- ^ ^ лимеры: бутадиена с соотноше- §
нием 1, 2-бутадиена и 1,4-бута ^ 56
диена,
равным 3:1 (батон-150), §- " бутадиенстирольный
сополи- ;« мер (батон-100), ненасыщен- ^ 23
ная эпоксидная смола (окси- ^ рон-2002),
ненасыщенная полиэфирная смола
(люминак-4192), цис-1,4-полубутадиен
(диен-35),
смесь 30% 1.2-
и
. Ai
п
4Хп7
,
л * Рис.
41. Скорость
вулканизаяии эт1*-
70%
1,4-полибутадиена
(поли- денпропиленового
сополимера /-си-
бутадиен-Р-15). стема
дикумила с
серой,
2—система
Из
указанных мономеров дикумила
с батоном-150 этилендиметакрилат,
а из полимерных соагентов
полибутадиеновая смола (батон-150)—наиболее
эффективные структурирующие агенты.
Батон-150 и вязкие смолы являются самыми
дешевыми структурирующими соаген-тамн
для смесей этиленпропиленового каучука.
Они удобны вследствие нетоксичности,
отсутствия запаха и способствуют
хорошему распределению ингридиентов
резиновой смеси. Скорость вулканизации
с применением батона-150 больше, если в
качестве соагента берется сера (рис.
41).
Кроме
перечисленных соагентов были опробованы
нитрозан К(Ы,4-динитрозо-^метиланилин),
продукты конденсации фурфурола с
ацетоном (VP-4),
гексаметилендиаминбифургин,
окислы азота [323], диизоцианаты,
производные фурана [324,325],
актиламиды [326], триалкилфосфат [327],
диалкилфталат [321], являющиеся эффективными
заменителями серы. Лучшими соа-гентами
являются дималеинмиды, диазонилцианурат,
триамил-цитрат—применение их значительно
повышает скорость вулканизации и
позволяет проводить процесс при более
низких температурах и меньшей
продолжительности вулканизации, а
также снизить содержание перекиси в
смесях.
0
5
/0/5
^0
Врет
ёулнанахщиинри 1М%тН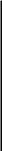
x
я
ч
ю
СП
s—
CU
go
7;
(*^'j.oei
'вих
-вжэ
%QZ)
нипви
с!офэ1Г
BBHhoj.eJ.30
я
>,~
u
S
2
о
g
о
2 £
со
с-о -
О
<
а-:
-э-ОС
cn
X
о
-
о
К
=
а-
X
Л S
н
4
5 о
си
■=!
Ях и
^
О
Ч D,
и
,
со сп
^<
О
s сп
1й
н с
си
с^о 5
s's
*
о 5
я
-J
«
СО ^
X ,~
л:
с
о
со
О
СО
CN
ГО
СО CN
О
ОО СО О
о
cd
с.
оо—
со cd
о
ОС
О
CD СО
Ю
20
СО
00
СО
СС О
о
о' о" о" о" о
СО
Ю ^ Т ^
)
О Ю сс
со
СО со
CD
—
О CN
СМ
см
см
оо
о
О
иО
о
о
оо
(MN
COCOLO^
СО
г^-СМ
Ю -чр ^
Г0
СО
СМ
1/3
иО Tf
иО
г- "-С1
О О CD
CD CD
S
я
со
сч
о
2
С-
о х
нот.
сп
ir:
э*
о, я .
>,
Ч X Я X СП
О
О
§
«а
Ч
сп
„ Ю
сп X • Ч О Н X m
ч
ч х ч
я я
я о°_
я
. .
о.
я
Е-
«
о
СО
Однако
сопротивление разрыву таких вулканизатов
ниже, чем
вулканизатов, содержащих серу (табл.
61).
Интерес
представляют также некоторые ненасыщенные
кислоты и их ангидриды. Особенно
активны при перекисной вулканизации
малеиновая кислота и ее ангидрид.
Механические
свойства резин можно улучшить добавлением
к смеси кроме перекисных и непредельных
кислот небольших количеств окиси цинка,
причем с повышением количества окиси
увеличивается прочность на разрыв
(табл. 62).
Влияние
непредельных кислот на процесс
вулканизации показано в табл.СЗ.
Механизм
действия соагентов перекисной
вулканизации сложен и полностью не
изучен. По мнению Робинсона и его
сотрудников [310], активные соагенты
сначала реагируют с полимерными
радикалами. Например, соагент типа
хинондиоксима ингибирует реакцию, в
результате которой происходит деградация
макроцепи благодаря быстрому
присоединению к ней соагента с
образованием стабильных промежуточных
радикалов. Последние могут
быть структурированы (за счет поперечных
связей), но не способны отрывать от
молекулы сополимера атом водорода
ОН ОН
I
[Rl]
+
N С<(
У
=
N
ОН ОН
ОН ОН
-
R.-N-N==)-N-Ra
Интересна
роль дивиниладипата при вулканизации.
В противоположность хинондиоксиму,
который присоединяется к полимерным
радикалам с образованием устойчивых
промежуточных радикалов, дивиниладипат
образует реакционноспособные радикалы,
эффективные в
реакциях
подавления деструкции, но могущие и
продолжать процесс структурирования:
[Ri]
+
С
= С—J—С
=
С - [R,-C—C-J-C
= C-]
—"
Н
I
кз
R,-C-C-J-C
=
C-f
R'2 ►Ri-C-C-J-C-C-Rg
:'..
I I
H H
о о
я И
и
т. д. J=[-0-C-(CH2)4-C-0-l
В
присутствии триаллилцианурата [328]
полимерный радикал может реагировать
с его аллильной группой. За счет
взаимодействия двойной связи с
радикалом полимерной цепи или с другим
Го
О
СО — О
со
сс со о о о"
СМ
О
со
СО
СО
о
см оо со
ОО
со
е
я
ш
о
^о,
аЗ
S
я
га
о.
н
о •&
О
о
ТО
Ch
CU
CU
X
CI
о.
4
н
%
'эинэн
\il'VЈ
э0ньо1в1ээ
Влияние
непредельных кислот на процесс
вулканизации
(сополимер
этилена и пропилена 100 г, перекись
дибензола 2 г, вулканизация 30 мин
при
160°С)
Модуль
при 300%-ном удлинении,
%
присоединившимся
к цепи радикалом цианурата происходит?
сшивание. При сшивании присоединившегося
циануратного радикала радикалом
перекиси в молекуле цианурата еще
остаются 2 двойные связи, насыщением
которых достигается увеличение
числа сшивок, в результате чего заметно
повышается степень сшивания.
СН
■= СН,
-с-
+н2с=.-сн ch2r-c-ch2-ch
СН2
СН2 СН2
N 0/ J сн2
СН
1
сг'ч)с/
N
L
"N
С
!
о
I
сн
2 О
I |
сн=сн2 сн2-СН^Сг
Интересно
использование для сшивания СКЭП
некоторых полимеризующихся мономеров,
которые, принимая участие в образовании
поперечных связей, одновременно
подвергаются* полимеризации, образуя
пространственную структуру типа «сетка
в сетке». Ввиду того, что свободные
радикалы атакуют в первую очередь
двойные связи, которые более
реакционноспособны, чем атомы водорода
насыщенной цепи полимера, можно
предположить, что первой стадией
реакции будет инициирование полимеризации
мономера перекисью. Радикалы мономера
могут
рекомбинировать с макрорадикалами
каучука, предотвращая их
диспропорционирование.
Возможно
также присоединение макрорадикалов
этиленпропиленового
эластомера к двойным связям мономера.
Таким
образом, происходит образование
собственной' пространственной сетки
мономера, связанной с пространственной
сеткой каучука, в результате чего
переплетение цепей дополнительно
увеличивает густоту пространственной
сетки.
о
о
N
\
N\
N
С
Относительное
удлинение, %
Прочность
на разрыв, кгс/см'2
Колич.
кислоты,
г
Твер
дость
по
ШОРу
Непредельные
соединения
Без
кислоты
Малеиновая
кислота
Итаконовая
кислота
Ангидрид
цит-
роновой кис
лоты
Кротоновая
кислота
Акриловая
кислота
75
150 103
90
75
95
660
550 510
580
510
450
51
55 54
9
10
11,5
6,7
11,2
52
СН
32
56 67
54
56 65
К
числу таких мономеров относятся стирол,
дивинилбензол, акриловая кислота,
диметакрилат этилена и др. Перед
сшиванием полимеризующий мономер
выполняет функции пластификатора,
а после вулканизации действует как
активный наполнитель (табл.64).
2. Обртговние
комплекса 2(С1) + 2(S)
->
S2C1S
i;2ci2
+ reci3~re:'3.s2ci2
(СП
+ I
eC!3-S2Cl2
-+
FeCl3-SCl2
+
S2C12
2(C1)
+
FeCI3-SCl2
FeC)3-SCl4
5
(CI)
+
2(S)
+
FeCl3
-»
FeCl3-SCl4
+
~
S2C12.
3. Образование
активных центров за счет отрыва
атомов
водорода от полимера активным
промежуточным комплексом
FeCl,-SCl4
+
2РН - FeCl3-SCl2
+ 2Р*
+ 2НС1 FeC)3-SCl24-
2РН
- FeCl2-SCl
+
2Р* + 2HCI
2Р*
— Р—р
2Р*-+-
S2-
P-S-S-P. В
табл. 65 приведены физико-механические
свойства резин из СКЭП в зависимости
от вулканизующего агента.
Таблица
65
Другие
вулканизующие агенты
Помимо
органических перекисей имеются и
другие соединения, способные
вулканизовать СКЭП. Наибольший интерес
представляют полигалоидалифатические
соединения, например, октахлорпропан,
перхлор-За,4,7а-тетрагидро-4,7-метанинден,
перхлор-1,1 -бис-(2,6-циклопентен),
галогенированный фульфа-лен [329—331]. В
качестве активаторов вулканизации
применяют металлосодержащие соединения,
например, карбоксилаты железа
(таллат, стеарат, нафтенат, 2-этилгексанат,
оксалат и др.), а
также
алюминия и железа (безводные или
содержащие кристаллизационную
воду).
Вей
[332] для вулканизации этиленпропиленового
эластомера применял октахлорциклопентадиен
(т-ра пл. —40°С, т-ра кип. 283°С) и
галогенированные алициклические
соединения, пер-хлор-За,4,7а-тетрагидро-4,7-метанинден.
Вулканизаты с окта-хлордихлороктадиеном
проявляют лучшую адгезию к
металлу
по сравнению с перекисными вулканизатами.
Как мы уже отмечали, при вулканизации
перекисью дикумила нельзя применять
кислые наполнители, в то время как
использование этих наполнителей при
вулканизации с октахлорциклопентадиеном
не представляет никаких затруднений.
После
изучения реакций, протекающих в
модельной системе, состоящей из декана,
октахлордициклопентена, серы и окиси
железа, Вей с сотрудниками предложили
механизм вулканизации галоидалкилами
на примере октахлорпентадиена в
присутствии серы и FeCl3:
1.
С5С18—
3(C)
+
6 (С1) 4- СС1 as
СС1
(дихлорацетилен осмо-ляется)
В
результате многочисленных исследований
Вей приходит к выводу, что активные
вулканизующие полигалоидалифатические
соединения должны быть полностью
галогенированы и содержать не более
одной углеродной связи на кольцо или
открытую Цепь, причем активность
галоидсодержащих вулканизующих агентов
снижается в ряду Cl>Br>J>F.
Эффективными
вулканизующими агентами для СКЭП
являются также трихлорметансульфонилхлорид,
трихлормеламин, хинон-Ы-хлоримид
[333].
Свойства
вулканизатов СКЭП с различными
вулканизующими агентами (вяс.
ч.)
(время
вулканизации 30
мин
при
160°С)
Этиленпрош-ieiK
в>г
каv1ук
Имеются
также сообщения об использовании в
качестве вулканизующих агентов
полисульфонезидов общей формулы R
(SC2N3)X[335),
а
также соединений, содержащих N-галоид-ную
группу [329, 332,]например, тетрахлорбензогуамин,
гек-еах торуеламин и др.
100
100
100
100
100
Печная
сажа НАг Сера
Окись
цинка Трихюрметансуль^о-п'л-
хлорид
Трихлорчеламин п-Бензохинонхлорпм:;-,
2,6-Дихлорхинонхлоримид 2.6-Дибромхинонхлоримпд
Предельная прочность,
кгс/см'2
Относительное
удлинение, %
15".
251
550
50
2.5 5
169
458
50
2 5
126
700
50
2 5
185
400
50
130
580
