
- •73.Фарм. Контроль качества воды очищенной и для иньекций.
- •75) Бария сульфат для рентгеноскопии.
- •76)Магния оксид и магния сульфат. Получение, свойства, контроль качества, хранение и медицинское применение.
- •81)Натрия гидрокарбонат (NaHco3 )
- •82). Кислота борная и натрия тетраборат. Получение, св-ва, контроль качества, хранение и медицинское применение.
- •84) Железа хлорид и меди сульфат
- •Меди сульфат. Получение, свойства, контроль качества, хранение и медицинское применение.
- •85)Вазелин.Получение,св-ва,контроль качества,хранение и мед.Применение.
- •87) Раствор формальдегида(формалин).Получение,свойства,контроль качества,хранение и мед.Применение
- •88)Моносахарид: глюкоза.Получение,свойства,контроль качества,хранение,мед. Применение
- •89) Кислота аскорбиновая Получение, контроль качества, хранение и мед. Применение.
- •90)Капльция глюконат, Получение, св-ва, контроль качества, хранение и мед. Применение.
- •91) Глицин
- •92) Ментол. Получение, свойства, контроль качества, хранение и медицинское применение.
- •93) Лекарственные в-ва группы фенолов: фенол, резорцин.
- •94) Производные п-аминофенола: парацетамол.
- •97) Сложные эфиры пара-аминобензойной кислоты: бензокаин, прокаина гидрохлорид.
- •98) Нитрофенилалкиламины: хлорамфеникол и его эфиры.
- •99) Сульфаниламид (стрептоцид) и сульфаниламиды, замещ. По амидной группе.
- •100) Нитрофурал (Nitrofural, Фурацилин)
- •101) Рутозид тригидрат (# рутин)
- •102) Метамизол-натрий. Получение, св-ва, контроль кач-ва, хранение и мед. Применение.
- •104) Папаверина гидрохлорид:.
- •105) Кофеин.Получение,св-ва,контроль качества,хранение и мед.Применение.
- •106) Аминофиллин. Получение, св-ва, контроль качества, хранение и мед.
- •107) Кислота фолиевая (Acidum folicum, Folic acid)
- •108) Рибофлавин (# витамин в2) Ribofl avinum riboflavin
82). Кислота борная и натрия тетраборат. Получение, св-ва, контроль качества, хранение и медицинское применение.
Источниками получения кислоты борной и натрия тетрабората являются природные минералы, которые либо сами содержат борную к-у (сассолин) и натрия тетраборат (бура, кернит), либо разрушаются с их образованием. При обработке минералов минеральными к-ми образуется к-та борная,а при действии карбонатом натрия – натрия тетраборат. Основным промышленным способом получения к-ты борной является разложение буры или борокальцита горячим р-ром хлороводородной к-ты
![]()
![]()
Фильтрат охлаждают, и выделившиеся кристаллы к-ты борной перекристаллизовывают из воды.
Натрия тетраборат получают действием р-ов карбоната натрия (при нагревании) на к-ту борную или минерал борокальцит:
![]()
![]()
К-та борная – бесцветные, блестящие, жирные на ощупь чешуйки или мелкокристаллический порошок без запаха.
Натрия тетраборат – бесцветные, прозрачные, легко выветривающиеся кристаллы или белый кристаллический порошок.
Оба препарата растворимы в воде и глицерине. В кипящей воде их растворимость значительно улучшается. К-та борная р-ма в спирте, нария тетраборат в нем практически не р-м.
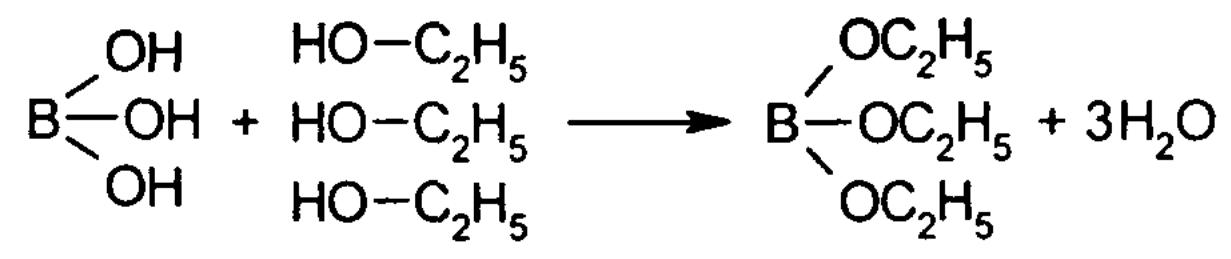
Подлинность препаратов бора можно установить по р-ции образования борноэтилового эфира, который горит пламенем, окаймленным зелёным цветом:
Н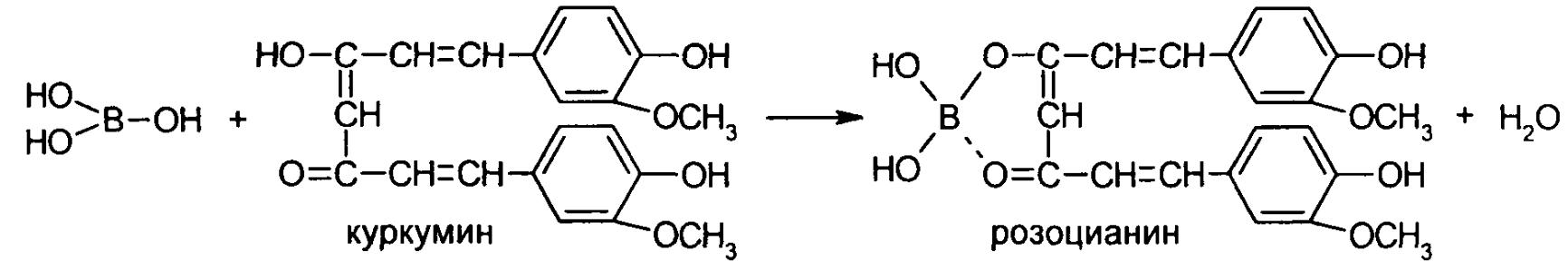 айболее
часто препараты идентифицируют с помощью
куркумовой бумаги, которая после
смачивания р-ом препарата и соляной
к-ты окр. В розовый или буровато-красный
цвет, переходящий после обработки в
зеленовато-черный.
айболее
часто препараты идентифицируют с помощью
куркумовой бумаги, которая после
смачивания р-ом препарата и соляной
к-ты окр. В розовый или буровато-красный
цвет, переходящий после обработки в
зеленовато-черный.
Для качественных р-ций могут быть также использованы р-р кармина в конц. Серной к-те (фиолетовое окр.), р-р хинализарина в конц.серной к-те (синее окр.), р-р ализаринового красного в конц. Сер. К-те(красное окр.),р-р пирокатехинового фиолетового(красное окрашивание),р-р иода + разв. Соляная к-та(синее окр.)
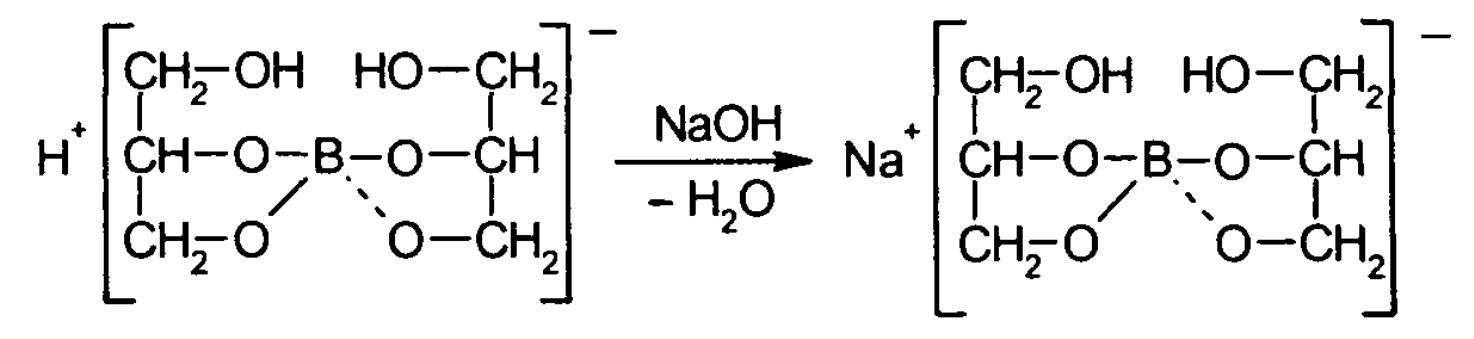
Для количественного определения используют способность к-ты борной образовывать с глицерином сильную одноосновную диглицериноборную к-ту,которую можно оттитровать щелочью,используя фенолфталеин в кач-ве инд.
Количественное определение к-ты борной проводят в сеси 1:4 свежепрокип. Воды и нейтрализованного по фенолфталеину глицерина.Для контроля поноты образования натриевой соли диглицериноборной к-ты к концу титровния добавляют дополнительную порцию глицерина.Сохранение розовой окраски свидетельствует о достижении эквивалентной точки, если окраска исчезает вновь добавляют глицерин и продолжают титрование пока окраска не перестанет исчезать. Количественное определение натрия тетерабората выполняют методом нейтрализации(инд. метиловый оранжевый),используя для этого р-цию взаимодействия с соляной к-той
![]()
Препараты соединений бора хранят в защищенном от света месте, в хорошо укупоренной таре. К-ту борную и натрия тетраборат применяют в качестве наружных антисептических ср-в в виде водных 1-4%-ных р-ов.
83). ЦИНКА ОКСИД (Zinci oxidum) ZnO ОПРЕДЕЛЕНИЕ. Содержит не менее 99,0 % и не более 100,5 % ZnO в пересчете на прокаленное вещество. СВОЙСТВА. Мягкий белый или бледновато-желтовато-белый аморфный порошок, не содержащий твердых частиц. Поглощает из воздуха диоксид углерода. Практически нерастворим в воде и 96 % спирте. Растворяется в разведенных минеральных кислотах, в уксусной кислоте, в растворах гидроксидов щелочных металлов. ПОЛУЧЕНИЕ. 5ZnSO4 + 5Na2CO3 + 3H2O = 2ZnCO3*3Zn(OH)2 ↓ + 5Na2SO4 + 3CO2↑; 2ZnCO3*3Zn(OH)2 =t°=5ZnO + 2CO2↑ + 3H2O. ПОДЛИННОСТЬ. 1. Желтеет при сильном нагревании. Желтая окраска исчезает при охлаждении. 2. (после растворения в HCl) а) Zn2+ + S2- = ZnS↓ белый; б) Zn2+ + K+ + [Fe(CN)6]4- = Zn3K2[Fe(CN)6]2 ↓ белый; в) Zn2+ + 2OH- = Zn(OH)2↓белый. ИСПЫТАНИЯ. 1. Щелочность. 2. Карбонаты и вещества, нерастворимые в кислотах. 3. Мышьяк (Не более 0,0005 %). 4. Кадмий(0,001 %). 5. Железо (0,02%). 6. Свинец (0,005%). 7. Потеря в массе при прокаливании. Не более 1,0 %. 8. Ост. кол-ва орг. р-лей. 9. Микробиол. чистота. КОЛИЧ. ОПРЕДЕЛЕНИЕ. Комплексонометрически в слабощел. среде. ХРАНЕНИЕ в хорошо укупор. таре (защищ. от углекислоты воздуха). ПРИМЕНЕНИЕ. Обладает слабым дезинфицир. и вяжущим действием. Примен. в виде присыпок, в составе мазей и паст.
ЦИНКА
СУЛЬФАТ
(Zinci sulfas hexahydricus) ZnSO4 · 6H2O ОПРЕДЕЛЕНИЕ.
Содержит
не менее 99,0 % и не более 104,0 % ZnSO4·6H2O.
СВОЙСТВА.
Белый
или почти белый кристаллический порошок
либо бесцветные прозрачные кристаллы.
Выветривается на воздухе. Очень легко
растворим в воде, практически нерастворим
в 96 % спирте. ПОЛУЧЕНИЕ.
Zn
+ H2SO4
= ZnSO4
+ H2↑.
ПОДЛИННОСТЬ.
1. Р-и на сульфат-ион![]() белый.
2. На ион цинка (см. выше). ИСПЫТАНИЯ.
1. Прозрачность. 2. Цветность. 3. pH.
4. Хлориды (0,03%). 5. Железо (0,01%). 6. Ост. кол-ва
орг. р-лей. 7. Микробиол. чистота. КОЛИЧ.
ОПРЕД.
(см. выше). ХРАНЕНИЕ.
Сп. Б. В воздухонепрониц. контейнере
(защ. от выветривания). ПРИМЕНЕНИЕ.
Антисептич.
и вяжущее ср-во. Прим. при конъюнктивитах
(глазные капли), при ларингитах. Может
назначаться внутрь в качестве рвотного
средства (0,1-0,3г), врд 1г.
белый.
2. На ион цинка (см. выше). ИСПЫТАНИЯ.
1. Прозрачность. 2. Цветность. 3. pH.
4. Хлориды (0,03%). 5. Железо (0,01%). 6. Ост. кол-ва
орг. р-лей. 7. Микробиол. чистота. КОЛИЧ.
ОПРЕД.
(см. выше). ХРАНЕНИЕ.
Сп. Б. В воздухонепрониц. контейнере
(защ. от выветривания). ПРИМЕНЕНИЕ.
Антисептич.
и вяжущее ср-во. Прим. при конъюнктивитах
(глазные капли), при ларингитах. Может
назначаться внутрь в качестве рвотного
средства (0,1-0,3г), врд 1г.
