
- •1 Частина
- •2 Частина
- •3 Частина
- •3.2 Дано: Розв'язання
- •3.3 Дано: Розв'язання
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •5. Обчислюємо масу суміші:
- •3 Частина
- •3 .2 Дано: Розв'язання
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •5. Обчислюємо масу суміші:
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •5. Обчислюємо масу суміші:
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •5. Обчислюємо масу суміші:
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
- •1 Частина
- •2 Частина
- •3 Частина
2 Частина
2.1 |
|
А |
2 |
Б |
4 |
В |
1 |
Г |
5 |
2.2
Na2SO3 + 2НСl = 2NaCl + Н2О + SO2;
2Na+ + S + 2H+ + 2Сl– = 2Na+ + 2Сl– + H2O + SO2;
2H+ + S = H2O + SO2.
2.3
Д ано: Розв’язання
m(СН3Сl) = 101 г; 1 Обчислюємо кількість речовини СН3Сl:
m(Сl2) = 35,5 г. M(СН3Сl) = 50,5 г/моль;
V (CH3Cl + Сl2) – ? v(CH3Cl) = m(CH3Cl): М(СН3Сl) = 101 г : 50,5 г/моль =
= 2 моль.
2. Визначаємо об’єм СН3Сl:
V(CH3Cl) = v(CH3Cl) • VM = 2 моль • 22,4 л/моль = 44,8 л.
3. Знаходимо кількість речовини Сl2:
v(Cl2) = т(Сl2) : М(Сl2) = 35,5 г : 71 г/моль = 0, 5 моль.
4. Визначаємо об’єм Сl2:
V(Cl2) = v(Cl2) • VM = 0,5 моль • 22,4 л/моль = 11,2 л.
5. Обчислюємо об’єм суміші:
V(CH3Cl + Сl2) = V(CH3Cl) + V(Cl2) = 44,8 л + 11,2 л = 56 л.
Відповідь: V(CH3Cl + Сl2) = 56 л.
2.4
Д ано: Розв’язання
m(K2SO4) = 43,5 г. 1. Обчислюємо кількість речовини K2SО4:
v (K+) — ? M(K2SO4) = 174 г/моль;
v(K2SО4) = m(K2SО4) : M(K2SО4)= 43,5 г : 174 г/моль = 0,25 моль.
2. Визначаємо кількість речовини К+. Електролітична дисоціація K2SО4 відбувається згідно з рівнянням:
K2SО4 2К+ + S .
Як видно з рівняння реакції:
v(K2SО4): v(K+) = 1:2, звідки:
v(K+)= 2v(K2SО4) = 2 • 0,25 моль = 0,5 моль.
Відповідь: v(K+) = 0,5 моль.
3 Частина
3.1
2КІ + Сl2 = 2КСl + I2;
електроліз розплаву: 2КСl = 2К + Cl2↑;
Н2 + Сl2 = 2НСl;
HCI + AgNO3 = AgCl↓ + HNO3.
3.2
(С6Н10О5)n + nH2O → nC6H12O6;
C6H12O6 → 2C2H5OH + 2CO2;
C2H5OH + CuO → CH3CHO + Cu + H2O;
CH3CHO + Ag2O → CH3COOH + 2Ag↓.
3.3
Д ано: Розв’язання
m пp.((CH3COO)2Ca) = 45,03 г; 1 Обчислюємо масу солі (CH3COO)2Ca, яка η((СН3СОО)2Са) = 95 % = 0,95. б могла утворитись теоретично:
m (СН3СООН) — ?
η((CH3COO)2Ca)
=
 ;
;
звідки
mтеор.((СН3СОО)2Са)
=
 =
=
 = 47,4
(г).
= 47,4
(г).
2. Обчислюємо масу кислоти, що прореагувала:
х 47,4 г
2СН3СООН + Са(ОН)2 → (СН3СОО)2Са + 2Н2O.
2 · 60 г 158 г
М(СН3СООН) = 60 г/моль;
М((СН3СОО)2Са) = 158 г/моль.
Під час взаємодії 120 г СН3СООН утворюється 158 г (СН3СОО)2Са, а під час взаємодії x г СН3СООН — 47,4 г (СН3СОО)2Са.
Складаємо пропорцію:
х : 120 = 47,4 : 158.
120-47,4
Звідки х
=
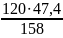 =
36 (г).
=
36 (г).
Відповідь: m(СН3СООН) = 36 г.
13 ВАРІАНТ.
1 Частина
1.1 |
1.2 |
1.3 |
1.4 |
1.5 |
1.6 |
1.7 |
б |
б |
в |
б |
б |
Б,г |
Г,д |
1.8 |
|
А |
3 |
Б |
4 |
В |
5 |
Г |
2 |
2 Частина
2.1 |
|
А |
5 |
Б |
2 |
В |
3 |
Г |
4 |
2.2
K2S + 2НСl = 2КСl + H2S;
2K+ + S2– + 2H+ + 2Сl– = 2K+ +2Сl– + H2S;
2Н++ S2– = H2S.
2.3
Д ано: Розв’язання
w(K3PO4) = 84,8 г; 1. Обчислюємо масу розчину:
m(Н2O) = 315,2 г m(р–ну К3РO4)= m(К3РO4) m(Н2O)=84,8г +315,2г =400г.
w (K+) —?
2. Обчислюємо кількість речовини К3РO4:
v(K3PO4) = m(К3РO4): М(К3РO4) = 84,8 г : 212 г/моль = 0,4 моль.
3. Обчислюємо кількість речовини йонів К+ у розчині:
К3РO4 3К++ Р ;
v(K+) = 3v(K3PO4) = 3·0,4 моль = 1,2 моль.
4. Знаходимо масу йонів К+ у розчині:
m (К+) = v(K+) · М(К+) = 1,2 моль · 39 г/моль = 46,8 г.
М(К+) = М(К) = 39 г/моль.
5. Визначаємо масову частку йонів К+ у розчині:
w(K+) = m(K+) : m(р-ну К3РO4) = 46,8 г: 400 г = 0,117 = 11,7 %.
Відповідь: w(K+) = 11,7 %.
2.4
Д ано: Розв’язання
w(O2) = 6,4 г; 1. обчислюємо кількість речовини O2:
m(СО2) = 4,4 г. v(O2) = т(O2) : М(O2) = 6,4 г: 32 г/моль = 0,2 моль.
V (O2 + СO2) —? 2. Визначаємо об’єм O2:
V(O2) = v(O2) • VМ = 0,2 моль • 22,4 л/моль = 4,48 л.
3. Знаходимо кількість речовини СO2:
v(CО2) = m(СO2) : М(СO2) = 4,4 г: 44 г/моль = 0,1 моль.
4. Визначаємо об’єм СO2:
V(CO2) = v(CO2) • VM = 0,1 моль • 22,4 л/моль = 2,24 л.
5. Обчислюємо об’єм суміші:
V(O2 + СO2) = V(O2) + V(CO2) = 4,48 л + 2,24 л = 5,6 л.
Відповідь: V(O2 + СO2) = 5,6 л.
