
- •1.Основные требования, предъявляемые к химическому оборудованию при проектировании.
- •2.Технология аммиака
- •3.Способы получения хлорида калия.
- •4 Сырьевые материалы в технологии кальцинированной соды (карбонат натрия)
- •5 Расчет авд на устойчивость
- •1. Основные требования к выбору конструкционных материалов. Виды конструкционных материалов.
- •2. Основные стадии в производстве неконцентрированной азотной кислоты и их характеристика.
- •1 Получение no
- •2 Окисление no до no2
- •3 Абсорбция no2 растворами hno3
- •4 Очистка хвостовых газов от оксидов азота
- •3 Суммарная и электродные реакции при электролизе воды
- •4 Основные сырьевые материалы в производстве минеральных удобрений
- •5 Виды уплотнений в авд
- •1 Технология конверсии со
- •2 Цикл низкого давления с турбодетандером
- •3 Способы защиты от коррозии.
- •4 Пневмотранспорт
- •5 Особенности конструкции корпусов аппаратов высокого давления. Свыше 10 мПа или 1 атм. Маленький диаметр и большая длина (20-25 м), для того чтобы сохранить объём аппарата.
- •1 Виды коррозии. Водородная коррозия и способы защиты от водородной коррозии.
- •2 Классическая схема производства контактной серной кислоты. Существует два метода
- •3 Принцип поляризации электродов при электрохмических реакциях
- •4 Транспортные средства для перемещения сыпучих материалов.
- •5 Сырье для производства азотной кислоты.
- •1 Классификация сырьевых источников в технологии неорганических материалов
- •2. Основные стадии производства аммиачной селитры (нитрат аммония) и их краткая характеристика.
- •3. Установка пневмотранспорта. Схемы установок. Назначение.
- •4. Особенности расчёта авд
- •5. Механизм электродных процессов
- •1 Классификация минеральных удобрений:
- •2 Технологическая схема производства концентрированной азотной кислоты методом прямого синтеза
- •4 Основные технологические стадии в производстве кальцинированной соды аммиачным способом
- •5 Элеваторы.
- •1 Самопроизвольные и принудительные окислительно-восстановительные реакции, их использование
- •2. Технологическая схема производства аммофоса.
- •3 Особенности механического расчета авд
- •4 Виды конструкционных материалов. Стали
- •5 Сырье для производства серной кислоты
- •1 Методы очистки технологических газов. Классификация и краткая характеристика.
- •2 Технологическая схема производства камерного суперфосфата
- •3 Элеваторы.
- •4 Компрессоры. Типы. Степень сжатия.
- •5 Суммарная и электродные реакции при получении хлора и щелочи
- •1. Технологическая схема получения карбамида (полный жидкостный рецикл)
- •2.Принципиальная схема установки для производства разбавленной серной кислоты
- •3. Виды конструкционных материалов. Чугун
- •4. Поршневые насосы. Компрессоры
- •5. Тонкая очистка технологческого газа от оксидов углерода (метанирование)
- •1 Суммарная и электродные реакции при производстве цинка
- •2. Типовая технологическая схема получения нитроаммофоски
- •3 Конструкции аппаратов колонного типа.
- •4 Законы фарадея
- •5 Колонные аппараты тарельчатого типа. Гидродинамические режимы работы контактного устройства.
- •1.Основные требования, предъявляемые к химическому оборудованию при проектировании.
- •1. К технологическим относятся:
- •2.Конструктивние:
- •2.Физико-химические основы процесса конверсии аммиака
- •3 Особенности конструкции аппаратов высокого давления. Свыше 10 мПа или 1 атм. Маленький диаметр и большая длинна( 20-25 м) ,поэтому увеличивается объём аппарата.
- •4. Технологическая схема производства метанола
- •5 Метод получения глубокого холода, основанный на Джоуль-Томсоновском эффекте понижения температуры.
- •1 Физико-химические основы производства двойного суперфосфата камерным и бескамерным способом.
- •2. Основные технологические стадии в производстве серной кислоты
- •3. Машины для транспортировки жидкостей т газов
- •4 Виды коррозии.
- •5.Основные виды содопродуктов
2 Технологическая схема производства концентрированной азотной кислоты методом прямого синтеза
Прямой синтез HNO3 основан на взаимодействии жидких оксидов азота с водой и газообразным кислородом под давлением до 5 МПа по уравнению суммарной реакции
2N2O4 + O2 + 2Н2O → 4HNO3 + 78,8 кДж.
100%-ный диоксид азота при атмосферном давлении и температуре 21,5 °С полностью переходит в жидкое состояние. При окислении аммиака полученный NO окисляется в NO2, содержание которого в газовой смеси составляет примерно 11%. Перевести диоксид азота такой концентрации в жидкое состояние при атмосферном давлении не представляется возможным, поэтому для сжижения оксидов азота применяют повышенное давление. Применяют метод сжижения диоксида азота, основанный на растворимости NO2 в концентрированной азотной кислоте. Концентрированная азотная кислота обладает способностью поглощать NO2 из разбавленных нитрозных газов с образованием соединения HNO3·NO2 (нитроолеум). В результате его разложения образуется 98%-ная азотная кислота (товарный продукт) и концентрированный диоксид азота, который при двухступенчатом охлаждении переходит в жидкое состояние. На первой ступени для охлаждения применяют воду, на второй — рассол при температуре -10...-7 °С. При охлаждении ниже — 10°С диоксид азота выпадает в твердом виде, что может привести к забивке трубок холодильников.
В окислительных башнях не происходит полного окисления оксида азота до NO2, поэтому доокисление газа ведут в отдельной насадочной башне концентрированной азотной кислотой:
NO + 2HNO3 → 3NO2 + Н2O ∆H=73,6кДж.
Степень превращения NO в NO2 достигает 98—99%, но одновременно исходная концентрированная азотная кислота разбавляется примерно до 70—75% HNO3.
Полученные жидкие оксиды азота вступают во взаимодействие с разбавленной азотной кислотой и при действии кислорода под давлением 5 МПа и температуре 80 °С образуют концентрированную азотную кислоту.
Т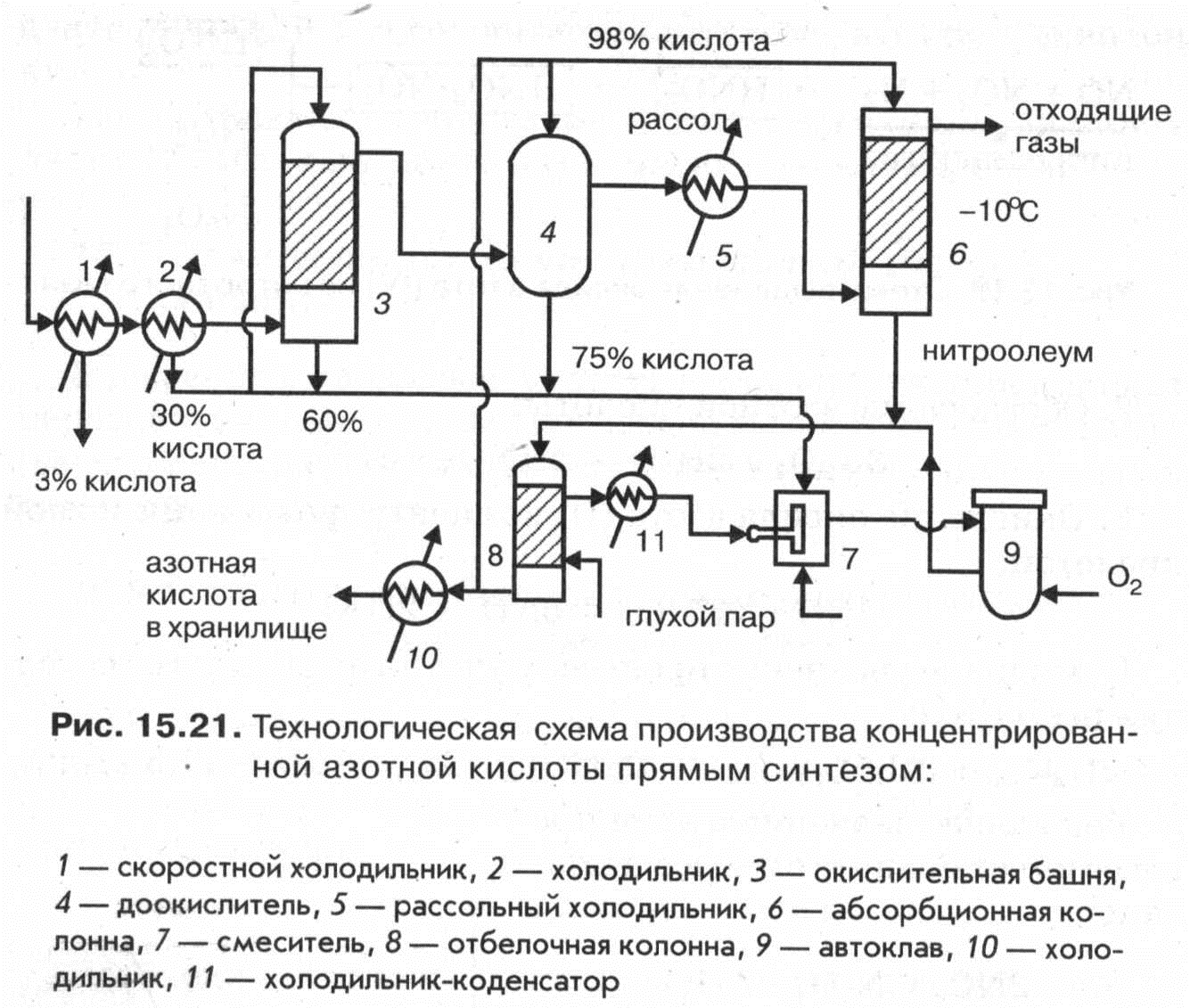 ехнологическая
схема производства концентрированной
азотной кислоты прямым синтезом из
жидких оксидов азота представлена на
рис. 7. Она включает операции: охлаждение
нитрозных газов в котле-утилизаторе и
холодильнике-конденсаторе, окисление
оксида азота (II) до оксида азота (IV),
доокисление оксида азота (II) азотной
кислотой, охлаждение нитрозных газов
в рассольном холодильнике, поглощение
оксида азота (IV) азотной кислотой,
обезвреживание отходящих газов, выделение
оксида азота (IV) из раствора в азотной
кислоте (нитроолеума), охлаждение оксидов
азота водой и рассолом, приготовление
смеси жидкого тетроксида азота и азотной
кислоты, окисление тетроксида азота
кислородом до азотной кислоты, десорбция
избытка тетроксида азота из азотной
кислоты.
ехнологическая
схема производства концентрированной
азотной кислоты прямым синтезом из
жидких оксидов азота представлена на
рис. 7. Она включает операции: охлаждение
нитрозных газов в котле-утилизаторе и
холодильнике-конденсаторе, окисление
оксида азота (II) до оксида азота (IV),
доокисление оксида азота (II) азотной
кислотой, охлаждение нитрозных газов
в рассольном холодильнике, поглощение
оксида азота (IV) азотной кислотой,
обезвреживание отходящих газов, выделение
оксида азота (IV) из раствора в азотной
кислоте (нитроолеума), охлаждение оксидов
азота водой и рассолом, приготовление
смеси жидкого тетроксида азота и азотной
кислоты, окисление тетроксида азота
кислородом до азотной кислоты, десорбция
избытка тетроксида азота из азотной
кислоты.
Нитрозный газ поступает в скоростной холодильник 1, где охлаждается до 40°С, причем из него выделяется 3% -ная азотная кислота, и затем в холодильник 2. Образовавшаяся в нем 30% -ная азотная кислота направляется в смеситель 7, а нитрозные газы в окислительную башню 3, орошаемую для охлаждения азотной кислотой. Из окислительной башни нитрозные газы поступают в доокислитель4, орошаемой 98% -ной азотной кислотой и затем, после охлаждения до -10°С в рассольном холодильнике 5, в абсорбционную колонну 6 для поглощения оксида азота (IV) и получения нитроолеума. С этой целью колонна орошается 98% -ной азотной кислотой. Непоглощенные газы из верхней части колонны направляются в систему очистки выхлопных газов. Образовавшийся в абсорбционной колонне нит-роолеум подается на десорбцию оксида азота (IV) в отбелочную колонну 8, куда вводится пар. Отбеленная азотная кислота концентрацией 98% охлаждается в холодильнике 10 и поступает в хранилище. Газообразные оксиды азота из отбелочной колонны охлаждаются и конденсируются в холодильнике-конденсаторе 11у охлаждаемом рассолом до -10°С и поступают в смеситель 7, в котором из них и смеси кислот образуется смесь: 68- 80% N204, 26-10,5% HN03 и 6-9,5% Н20. Эта смесь подается в автоклав 9, куда под давлением 5 МПа поступает кислород. Концентрированная азотная кислота отбирается из нижней части автоклава и соединившись с нитроолеумом из абсорбционной колонны 6 подается в отбелочную колонну 8.
