
- •Курсовая работа по дисциплине «Микробиологические методы контроля»
- •Минск 2013 Реферат
- •Содержание
- •Введение
- •1 Основная часть
- •1.1 Характеристика потерь сельскохозяйственного сырья и пищевых продуктов от микробиологической порчи
- •1.1.1 Уровень загрязненности сельскохозяйственного сырья и пищевой продукции микроорганизмами
- •1.1.2 Потери сельскохозяйственной продукции в процессе хранения
- •1.1.3 Способы защиты продукции от микробиологической порчи
- •1.2 Микробиологическая безопасность пищевых продуктов и ее характеристика
- •1.2.1 Показатели микробиологической безопасности пищевых продуктов
- •1.2.2 Требования нормативной документации к микробиологической безопасности продукции
- •1.2.3 Способы повышения микробиологической безопасности пищевых продуктов
- •1.3 Клетки микроорганизмов и их лизис
- •1.3.1 Строение клеточных стенок бактерий
- •1.3.2 Лизис клеточных стенок бактерий с сохранением и подавлением жизнеспособности клеток
- •1. Гомогенизация
- •2. Растирание клеток
- •3. Обработка ультразвуком
- •4. Френч-прессование
- •5. Ферментативный лизис клеток
- •1.3.3 Строение клеточных стенок гриба и их разрушение
- •1.4 Протопласты микроорганизмов
- •1.4.1 Методы получения протопластов микроорганизмов и оценки их выхода
- •1.4.2 Свойства протопластов микроорганизмов
- •1.4.3 Методы слияния протопластов клеток
- •1.4.4 Ревертация протопластов к клеточным формам
- •2 Экспериментальная часть
- •2.1 Материалы и оборудование
- •2.1.1 Микроорганизмы и питательные среды для культивирования микроорганизмов
- •2.1.2 Выделение чистых культур микроорганизмов, устойчивых и чувствительных к тяжелым металлам
- •2.2 Методы анализа
- •2.2.2 Метод получения протопластов микроорганизмов и оценки их выхода
- •2.2.3 Метод регенерации протопластов и оценка выхода регенерантов
- •2.2.4 Характеристика жизнеспособности протопластов и клеток редуктазным методом
- •2.2.5 Характеристика ростовой активности микроорганизмов
- •2.2.6 Определение тяжелых металлов методом комплексонометрии
- •2.2.7 Определение сорбции тяжелых металлов микроорганизмами
- •2.3 Результаты и их обсуждение
- •2.3.1 Получение устойчивых и адаптированных форм микроорганизмов к тяжелым металлам
- •2.3.3 Характеристика сорбции тяжелых металлов протопластами и клетками микроорганизмов
- •Заключение
- •Список использованной литературы
2.2.3 Метод регенерации протопластов и оценка выхода регенерантов
В гипертонической среде ММ9 колонии образуют клетки, на которые не воздействует лизоцим, а также протопласты, которые смогли в присутствии осмотического стабилизатора регенерировать клеточную стенку. Подсчитывают количество колоний и рассчитывают исходную концентрацию клеток в культуре, концентрацию протопластов и концентрацию регенерировавших протопластов.
Концентрация протопластов рассчитывается как разность между концентрацией исходных клеток (Кисх) и концентрацией клеток, которые не попали под воздействие лизоцима (Косм).
Концентрация протопластов, которые регенерировали клеточную стенку, рассчитывается как разность между концентрацией клеток двух типов на гипертонической среде (Крев) и величиной Косм.
Эффективность реверсии протопластов в клеточные формы (ЭР) ― это отношение концентрации протопластов, которые смогли регенерировать клеточную стенку, к общей концентрации протопластов:
(2)
2.2.4 Характеристика жизнеспособности протопластов и клеток редуктазным методом
Развивающиеся живые микроорганизмы вырабатывают фермент редуктазу, которая восстанавливает метиленовую синь в её бесцветное лейкосоединение.
Оценку редуктазной активности измеряли по следующей схеме:
1. отмеряли 1 мл раствора микроорганизмов в питательном бульоне и 1 мл раствора протопластов, полученных ферментативным лизисом, разбавляли их 9 мл воды;
2. получали по три разведения по схеме: 0,5 мл полученных растворов и 4,5 мл физраствора;
3. в полученные пробы добавляли 1 мл метиленового синего и засекали время, за которое содержимое обесцветиться.
2.2.5 Характеристика ростовой активности микроорганизмов
Для определения ростовой активности проводили эксперимент в следующей последовательности:
1. отбирали 1 см3 микробной суспензии каждой из культур, приготовленных на основе физраствора, переносили в стерильную пробирку и заливали 9 см3 питательного бульона. Оставляли приготовленный раствор в термостате при 37°С на два часа;
2. измеряли оптическую плотность полученного раствора с периодичностью 1 час, в течение которого культура выдерживалась в термостате.
Ростовая активность микроорганизмов при этом проявлялась через увеличение числа клеток и, как следствие, увеличение оптической плотности исследуемых растворов. Характеристика ростовой активности рассчитывалась по формуле:
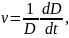 (7)
(7)
где D – оптическая плотность исследуемой суспензии;
t – длительность периода выстойки (1 час).
2.2.6 Определение тяжелых металлов методом комплексонометрии
Метод комплексонометрии основан на титровании раствора соли тяжелого металла раствором ЭДТА. В работе использовали раствор соли CuCl2.
Последовательность операций заключалась в следующем:
1. отбирали аликвотный объем анализируемого раствора соли из мерной колбы, прибавляли 2-3 мл буферного раствора с рН равным 10 (аммиачный буферный раствор: 67 г NH4Clи 570 мл 25%-ного NH3 в 1 л раствора), 15 мл воды, перемешивали и прибавляли на кончике шпателя индикатор эриохром Т черный;
2. смесь титровали 0,05М раствором ЭДТА до изменения окраски из красной в голубую.
Для точности эксперимента титрование проводили 3 раза, принимая за результат среднее арифметическое. Массу определяемого металла рассчитывали по формуле:
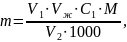 (6)
(6)
где
 -
объем раствора ЭДТА, пошедшего на
титрование;
-
объем раствора ЭДТА, пошедшего на
титрование;
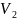 -
объем аликвоты;
-
объем аликвоты;
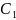 -
молярная концентрация ЭДТА;
-
молярная концентрация ЭДТА;
М – молярная масса определяемого вещества (64 г/моль);
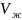 -
объем мерной колбы, из которой отбирали
аликвоту.
-
объем мерной колбы, из которой отбирали
аликвоту.
