
- •Наглядная иммунология
- •Предисловие
- •1. Определение иммунологии
- •2. Естественные и адаптивные иммунные механизмы
- •3. Эволюция иммунных механизмов
- •7. Фагоцитарные клетки. Система мононуклеарных фагоцитов
- •8. Фагоцитоз
- •9. Лимфоциты
- •10. Центральные лимфоидные органы и лимфопоэз
- •11. Периферические лимфоидные органы и рециркуляция лимфоцитов
- •12. Эволюция распознающих молекул
- •13. Главный комплекс гистосовместимости (гкгс)
- •15. Синтез и многообразие антител
- •16. Структура и функции антител
- •17. Распознавание и переработка антигена
- •18. Гуморальный иммунный ответ
- •19. Взаимодействие антигена и антитела и иммунные комплексы
- •20. Клеточный иммунный ответ
- •21. Толерантность
- •22. Идиотипы, антиидиотипы и их сети
- •23. Цитокиновая сеть
- •24. Иммунитет, гормоны, мозг
- •25. Антимикробный иммунитет. Общая схема
- •26. Противовирусный иммунитет
- •27. Иммунитет к бактериям
- •28. Иммунитет к грибам
- •29. Иммунитет к простейшим
- •30. Иммунитет к гельминтам
- •32. Нежелательные проявления иммунитета. Общая схема
- •33. Аллергия и анафилаксия
- •34. Иммунные комплексы, комплемент и заболевания
- •36. Аутоиммунитет
- •37. Отторжение трансплантата
- •38. Иммуносупрессия
- •39. Иммунодефициты
- •40. Вич и спид
- •41. Иммуностимуляция и вакцинация
25. Антимикробный иммунитет. Общая схема
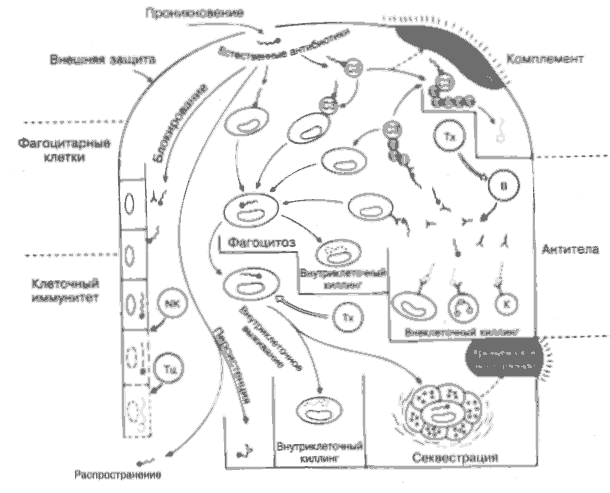
Следует подчеркнуть, что иммунная система высокоэффективна в распознавании чужеродных субстанции, но совершенно беспомощна в определении степени опасности, которую они могут представлять для организма. Кроме того, могут быть нежелательные побочные эффекты, например сильный иммунный ответ против чужеродной, но непатогенной структуры, такой, как пыльца злаковых и др. (рис 33).
Предполагаемые патогенные микроорганизмы, которые преодолевают кожные или слизистые барьеры, встречаются с 4 главными распознающими системами: комплементом (на рисунке вверху справа), фагоцитарными клетками (слева), антителами (справа) и клеточным иммунитетом (слева внизу) и вместе с их часто взаимодействующими эффекторными механизмами. Если отсутствует предварительный контакт с соответствующим антигеном, то антительный и клеточный иммунный ответ начинает действовать через несколько дней после проникновения микроорганизма, тогда как фагоцитарные клетки и комплемент, постоянно присутствующие в организме, — уже через несколько минут. Существуют специализированные естественные факторы (вверху в центре), такие, как лизоцим, интерферон и др., которые действуют более или менее неспецифично и почти как антибиотики (естественные антибиотики).
В общем, комплемент и антитела наиболее активны против микроорганизмов, свободно находящихся в крови или тканях, а клеточный иммунный ответ имеет дело с микроорганизмами, проникшими в клетки. Какой из механизмов окажется эффективным, во многом зависит от поведения микроорганизма. В следующих 5 разделах речь пойдёт о микроорганизмах, которые уклоняются от иммунных механизмов, подавляют их или становятся устойчивыми к ним.
Проникновение. Значительная часть микроорганизмов проникает в организм через раны, укусы. Микроорганизмы, обычно обитающие на коже или слизистых оболочках кишечиика, дыхательного тракта и других тканях, по сути дела находятся вне организма.
Поверхностные барьеры. Кожа и слизистые оболочки защищены кислой рН, ферментами, слизью и другими антимикробными секретами, а также антителами класса IgA (см. ниже).
Естественные антибиотике Выделяемые главным образом макрофагами антибактериальный фермент лизоцим (рис. 27) и противовирусные интерфероны (рис. 23, 26) составляют важное звено естественного иммунитета. Без них инфекционных заболевании было бы значительно больше. Очевидно, что многие другие естественные антибиотики ждут своего открытия. Этот тип защиты явно ограничен в масштабах во избежание повреждений «своих» тканей.
СЗ. Многие микроорганизмы непосредственно активируют СЗ-компонент комплемента по альтернативному пути, что в итоге приводит к их лизису или захвату фагоцитами. Тот же эффект наблюдается при активации СЗ антителами по классическому пути (рис. 5).
Т-хелперы обычно отвечают на несущую детерминанту антигена и стимулируют В-лимфоциты к синтезу антител. Установлено, что бактерии, вирусы, простейшие и гельминты выполняют функцию сильных носителей, хотя существует небольшое количество микроорганизмов, антительный ответ на которые является Т-независимым.
В-клетки. Образование антител В-лимфоцитами является почти универсальной характеристикой инфекции. Они имеют огромное диагностическое значение. Как правило, в иммунном ответе первыми появляются антитела класса IgM, затем — IgG и остальные. Высокий уровень IgM в сыворотке почти всегда указывает на начальную стадию заболевания. В слизистых оболочках наиболее эффективны антитела IgA (рис. 16).
Блокирование. Антитела могут не допустить проникновения микроорганизмов или токсинов в клетку, блокируй их участки, ответственные за связывание с клеткой, как это происходит, например, со столбнячной палочкой и большинством вирусов. IgA действует главным образом по этому механизму в кишечнике.
Фагоцитоз. Значительная часть микроорганизмов фагоцитируется макрофагами или полиморфно-ядерными лейкоцитами. Процесс значительно ускоряется, если микроб, предварительно опсонизированный СЗ или антителом, присоединяется к фагоцитарной клетке соответственно через СЗ- или Fc-рецепторы (рис. 8).
Внутриклеточное разрушение захваченных фагоцитами микроорганизмов осуществляется лизосомальными ферментами. В определённых случаях активация макрофагов Т-клетками необходима для запуска процесса киллинга микроорганизмов (рис. 20).
Внеклеточное разрушение. Моноциты, нейтрофилы и другие киллерные (К) клетки убивают покрытые антителами клетки in vitro без фагоцитоза, но неясно, насколько эта активность развита in vivo.
NK — естественные киллеры. Эти клетки способны быстро убивать многие инфицированные вирусом клетки, но без специфичности,-характерной для Т-лимфоцитов.
Внутриклеточная выживаемость. Некоторые вирусы, бактерии и простейшие могут выживать внутри макрофагов, где они устойчивы к киллерным механизмам. Другие микроорганизмы выживают в клетках мышц, печени, мозга и других органов, где они недоступны для антител и могут быть уничтожены только в результате клеточного иммунного ответа.
Тц — цитотоксический Т-лимфоцит. Вызывает лизис «своих» клеток, изменённых вирусом и другими антигенами, а также ал-логенных, например трансплантированных, клеток (рис. 20).
Тх — Т-хелпер замедленной гиперчувствительности, который через секретируемые цитокины привлекает и активирует моноциты, эозинофилы и другие клетки (рис. 20, 23). Центральная роль Т-хелперов при большинстве инфекции подтверждается тяжёлыми последствиями повреждения их, например, при СПИДе (рис. 40).
Секвестрация. Микроорганизмы, которые не могут быть убиты, например, некоторые микобактерии и недеградируемые вещества, в том числе оболочки стрептококков, участвуют в образовании гранулём макрофагами, часто при помощи реакций кле-точно опосредованного иммунного ответа (рис. 20).
Распространение. Выжившие микроорганизмы должны покинуть один организм и инфицировать другой, что происходит чаще всего при кашле, чихании, укусах насекомых, через фекалии и т.д.
Персистенция. Некоторые микроорганизмы выработали защитные механизмы, позволяющие избегать разрушающего действия иммунных факторов. Они способны длительно находиться в организме носителя, вызывая хронические и трудноизлечимые инфекционные заболевания.
Воспаление. Некоторые микроорганизмы (например, цитопатические вирусы), а также токсины способны разрушать ткани, но это несравнимо с теми повреждениями, которые наносит себе сам организм хозяина в ходе иммунного ответа на инфекцию. Острые и хронические воспаления подробно рассмотрены в других главах (рис. 6, 35). Здесь важно то, что инфекция ставит иммунную систему хозяина перед выбором: уничтожить микроорганизм любой ценой или, позволив ему жить, сберечь свои ткани. Решение этой дилеммы остается за естественным отбором.
