
Алкалоиды групп изохинолина и изохинолинофенантрена: папаверин, морфин, кодеин
ИЗОХИНОЛИНОВЫЕ АЛКАЛОИДЫ,
содержат в молекуле остатки
1,2,3,4-тетрагидроизохинолина, значительно
реже - 3,4-дигидроизохинолина илиизохинолина.
Обнаружены в растениях 30 семейств. Наиб.
богаты ими растения семейства анноновых
(Annonaceae), барбарисовых (Berberidaceae), дымянковых
(Fumariaceae), гернандиевых (Hernandiaceae), лавровых
(Lauraceae), магнолиевых (Magnoliaceae), луносемянниковых
(Menispermaceae), монимисвых (Monimiaceae), маковых
(Papaveraceae), лютиковых (Ranunculaceae).
Изохинолиновые алкалоиды включают
более 1000 представителей.Изохинолиновые алкалоиды содержат
от 10 до 42 атомов С.
Выделяют след. основные группы алкалоидов:
простые изохинолины (напр.,
корипаллин, ф-ла I), 1-бензилизохинолины
(папаверин,
II), апорфины (глауцин, III), проапорфины
(пронуциферин, IV), протоберберины
(берберин),
бензофенантридины (сангвинарин,
V), павины (аргемонин, VI), фталидизохинолины
(наркотин,
VII), спиробензилизохинолины (охотенсимин,
VIII), 2-бензилтетрагидроизохинолины,
1-фенил- и 4-фенилтетрагидроизохинолины,
азофлуорантены (руфесцин, IX),
дибензопирроколины (криптаустолин, X),
трополоизохинолины (имерубрин,
XI). Фенантреновые основания (таликтуберин,
XII), протопиновые основания (протопин,
XIII) и аристолактамы (дорифлавин, XIV) не
имеют изохинолиновой системы, но также
относятся к изохинолиновым алкалоидам,
с к-рыми биогенетически тесно
связаны.



 Среди
изохинолиновых алкалоидов обнаружены
димерные и тримерные основания,
напр., пилоцереин (XV). Наиб.
многочисл. группы апорфинов и
димерных оснований.
Последние включают более 250 алкалоидов,
образующихся в результате
окислит. димеризации бензилизохинолинов
(как, напр., тетрандрин, XVI), бензилизохинолинов
с апорфинами (таликарпин, XVII), проапорфинами,
оксоапрофинами, а также апорфинов
(бисапорфины), апорфинов с павинами
(пенсилпавин, XVIII). Многообразие
димерных алкалоидов обусловлено числом
эфирных мостиков
и их положением в молекуле.
К изохинолиновым алкалоидам относятся
также гликоалкалоиды, у к-рых агликон -
апорфин или бензилизохинолин. Многие
изохинолиновые алкалоиды синтезированы.
В ряде случаев осуществлен взаимный
переход между разл. типами алкалоидов.
Наиб. значение имеюталкалоиды группы
1-бензилизохинолина (XIX)
- предшественники в биосинтезе большинства
изохинолиновых алкалоидов.
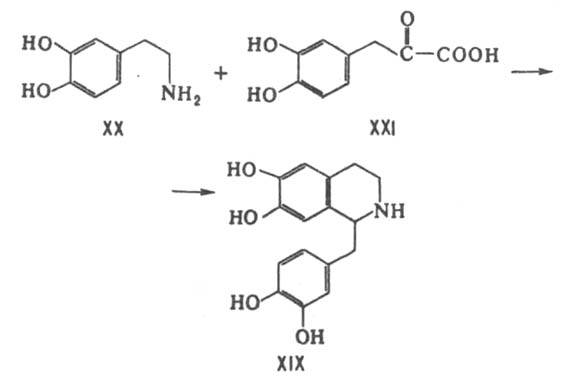
Соед. XIX образуется в
растениях, конденсацией допамина (XX)
и 3,4-дигидроксифенилпировиноградной
к-ты (XXI), образующихся из тирозина. Многие
изохинолиновыеалкалоиды обладают
противомикробной, спазмолитич.,
гипотензивной, желчегонной или
противовоспалит. активностью.
Ряд димерных оснований(напр.,
XVI и XVII) подавляют рост злокачеств. опухолей.
Среди
изохинолиновых алкалоидов обнаружены
димерные и тримерные основания,
напр., пилоцереин (XV). Наиб.
многочисл. группы апорфинов и
димерных оснований.
Последние включают более 250 алкалоидов,
образующихся в результате
окислит. димеризации бензилизохинолинов
(как, напр., тетрандрин, XVI), бензилизохинолинов
с апорфинами (таликарпин, XVII), проапорфинами,
оксоапрофинами, а также апорфинов
(бисапорфины), апорфинов с павинами
(пенсилпавин, XVIII). Многообразие
димерных алкалоидов обусловлено числом
эфирных мостиков
и их положением в молекуле.
К изохинолиновым алкалоидам относятся
также гликоалкалоиды, у к-рых агликон -
апорфин или бензилизохинолин. Многие
изохинолиновые алкалоиды синтезированы.
В ряде случаев осуществлен взаимный
переход между разл. типами алкалоидов.
Наиб. значение имеюталкалоиды группы
1-бензилизохинолина (XIX)
- предшественники в биосинтезе большинства
изохинолиновых алкалоидов.
Соед. XIX образуется в
растениях, конденсацией допамина (XX)
и 3,4-дигидроксифенилпировиноградной
к-ты (XXI), образующихся из тирозина. Многие
изохинолиновыеалкалоиды обладают
противомикробной, спазмолитич.,
гипотензивной, желчегонной или
противовоспалит. активностью.
Ряд димерных оснований(напр.,
XVI и XVII) подавляют рост злокачеств. опухолей.
 Нек-рые
изохинолиновые алкалоиды используют
в медицине, напр. III - противокашлевый
препарат, II - спазмолитик,
(+)-тубокурарин – миорелаксант
Нек-рые
изохинолиновые алкалоиды используют
в медицине, напр. III - противокашлевый
препарат, II - спазмолитик,
(+)-тубокурарин – миорелаксант
ПАПАВЕРИН [6,7-диметокси-1-(3,4-диметоксибензил)изохинолин; ф-ла I], мол. м. 339,45; бесцв. кристаллы; т. пл. 1470C; не раств. в воде, раств. в горячем этаноле и хлороформе. Слабое основание, образует кристаллич. гидрохлорид (т. пл. 2250C, раств. в воде, плохо в этаноле), пикрат (1860C). Папаверин-алкалоид. содержащийся в растениях рода мак (Papaver) семейства маковых, в частности в маке снотворном (P. somniferum). Биогенетич.предшественник папаверина-тетрагидропапаверин (II), к-рый образуется из норретикулина (III). Папаверин выделяют из опия (высохшего на воздухемлечного сока несозревших плодов снотворного мака), содержащего 0,5-1% этого алкалоида. Однако б. ч. последнего получают синтезом из вератрового альдегида (3,4-диметоксибензальдегида) и гипуровой к-ты C6H5C(О)NHCH2COOH.

Папаверин понижает тонус и уменьшает сократит, деятельность гладкой мускулатуры. Применяют (в виде гидрохлорида) как спазмолитич. и сосудорасширяющее ср-во.
МОРФИН, алкалоид, выделенный из снотворного, или опийного, мака (Papaver somniferum); ф-лу см. в ст. Мор-финановые алкалоиды. Представляет собой бесцв. кристаллы, т. пл. 254 °С; [a]D —140° (СН3ОН); плохо раств. в воде, этаноле, диэтиловом эфире, СНСl3, бензоле, лучше-в тепломметаноле. Из водно-этанольного р-ра кристаллизуется с одной молекулой Н2О, к-рую теряет при 100 °С.
Морфин получают из опия-сгущенного млечного сока, вытекающего из надрезов на недозрелых головках снотворного мака, культивируемого для этой цели. Содержание морфина в опии колеблется от 10 до 20% (по массе).
Осуществлен полный лаб. синтез морфина. В растении он образуется из тирозина (ф-ла I) через ретикулин (II), салутаридин (III), тебаин (IV) и кодеин(V):

Морфин-наркотич. анальгетик, оказывает сильное болеутоляющее, а также противошоковое действие. В больших дозах-снотворное. Угнетает дыхат. центр, вызывает эйфорию, при его повторном применении быстро развивается болезненное пристрастие (морфинизм). Эти св-ва морфина ограничивают в ряде случаев его использование. Применяют морфин при травмах и заболеваниях, сопровождающихся сильными болевыми ощущениями.
КОДЕИН, алкалоид,
выделенный из снотворного, или опийного,
мака (Papaver somniferum). Представляет собой
бесцв. кристаллы без
запаха, горького вкуса; т. пл. 155°С,
[a]D -134°
(CH3OH);
раств. в этаноле (1:9,5),
СНСl3 (1:0,5), бензоле (1:13),
плохо - в диэтиловом
эфире (1:50),
практически не раств. в воде (1:150
при 25 °С). Кодеин извлекают из опия
(высохшего на воздухе млечного
сока несозревших плодов снотворного
 мака),
в к-ром содержится от 0,2 до 0,8% алкалоида.
значит. кол-во кодеина
получают метилированием морфина. Биосинтез кодеина
в растениях аналогичен биосинтезу морфина. Кодеин
по характеру действия близок морфину,
но его болеутоляющее действие выражено
слабее; уменьшает возбудимость кашлевого
центра.
мака),
в к-ром содержится от 0,2 до 0,8% алкалоида.
значит. кол-во кодеина
получают метилированием морфина. Биосинтез кодеина
в растениях аналогичен биосинтезу морфина. Кодеин
по характеру действия близок морфину,
но его болеутоляющее действие выражено
слабее; уменьшает возбудимость кашлевого
центра.
