
- •1.2 Материальный баланс.
- •1.3 Уравнения рабочих и равновесных линий.
- •1.4 Различные модификации уравнений массоотдачи и массопередачи.
- •1.4.1 Уравнения массоотдачи и массопередачи в локальной форме.
- •Соответственно. Используя допущение об отсутствие сопротивления переносу вещества со стороны межфазной поверхности равновесии на границе раздела фаз, запишем:
- •1.4.2 Интегральная форма уравнений массоотдачи и массопередачи
- •1.4.3 Объёмные коэффициенты массоотдачи и массопередачи.
- •1.4.4 Число и высота единиц переноса
- •1.5 Аналогия тепло - и массообмена.
- •1.6 Упрощенные модели массоотдачи.
- •1.7. Классификация и основы расчета массообменных аппаратов.
- •1.7.1 Технологический расчет аппарата с непрерывным контактом фаз
- •Используя величину удельной поверхности контакта фаз вначале можно определить рабочий объем аппарата:
- •1.7.2 Технологический расчет аппарата со ступенчатым контактом фаз.
- •2. Абсорбция.
- •2.1. Равновесие при абсорбции. Закон Генри.
- •2.2. Материальный баланс и расход абсорбента
- •2.3 Тепловой баланс абсорбции.
- •2.4 Кинетика абсорбции.
- •2.5 Конструкции абсорберов.
- •Плёночные абсорберы.
- •Насадочные абсорберы.
- •Выбор насадки.
- •Тарельчатые абсорберы.
- •Распыливающие аппараты.
- •3. Перегонка жидкостей.
- •3.1. Равновесие в системах жидкость – пар.
- •3.2 Простая перегонка(дистилляция).
- •Однократная дистилляция.
- •Постепенная дистилляция.
- •Материальный баланс постепенной дистилляции.
- •3.4.Ректификация.
- •3.4.1. Материальный баланс непрерывной ректификации бинарных смесей.
- •Материальный баланс колонны по всему потоку:
- •Материальный баланс по нк:
- •Уравнения рабочих линий.
- •Выбор флегмовога числа.
- •3.4.2. Тепловой баланс ректификационной колонны.
- •3.5 Периодическая ректификация
- •3.6. Ректификация многокомпонентных смесей.
- •3.7. Экстрактивная и азеотропная ректификация.
- •3.8. Ректификационные установки.
- •4. Экстракция.
- •4.1.Жидкостная экстракция
- •4.1.1 Равновесия в системе жидкость – жидкость.
- •4.1.2 Материальный баланс процесса жидкостной экстракции. Однократная (одноступенчатая) экстракция.
- •4.1.3 Кинетика жидкостной экстракции.
- •4.1.3 Основные способы проведения жидкостной экстракции. Однократная (одноступенчатая) экстракция.
- •Многоступенчатая экстракция с перекрестным током растворителя.
- •Многократная экстракция с противоточным движением растворителя.
- •Непрерывная противоточная экстракция.
- •4.1.4. Классификация и конструкции экстракторов
- •4.1.4.1. Ступенчатые экстракторы
- •4.1.4.2 Дифференциально-контактные экстракторы. Экстракторы без подвода дополнительной энергии.
- •Экстракторы с подводом дополнительной энергии.
- •4.2. Экстрагирование в системе твердое тело – жидкость (выщелачивание).
- •4.2.1 Экстрагирование растворенного вещества.
- •4.2.2 Экстрагирование твердого вещества.
- •4.2.3. Способы и схемы экстрагирования.
- •5. Сушка.
- •5.1. Параметры влажного воздуха.
- •5.2. Диаграмма состояния влажного воздуха.
- •5.3 Равновесие при сушке.
- •5.4. Формы связи влаги с материалом.
- •5.4.1. Перемещение влаги внутри твердого материала
- •5.5 Материальный баланс конвективной сушки.
- •5.6 Тепловой баланс конвективной сушки.
- •5.7 Кинетика процесса конвективной сушки.
- •5.8. Устройство и принцип действия сушилок.
- •6.1 Адсорбенты.
- •6.2 Равновесие при адсорбции.
- •6.3 Материальный баланс адсорбции.
- •6.4. Кинетика периодической адсорбции.
- •6.5. Непрерывная адсорбция
- •6.6. Десорбция
- •6.7. Устройство и принципы действия адсорбционных аппаратов.
- •7. Кристаллизация.
- •7.1 Равновесие при кристаллизации.
- •7.2. Кинетика процессов кристаллизации.
- •7.3. Материальный и тепловой балансы кристаллизации. Материальный баланс.
- •7.4. Конструкции кристаллизаторов.
- •8. Мембранные процессы.
- •8.1. Классификация методов мембранного разделения. Типы мембран.
- •8.2. Механизм и кинетика мембранных процессов.
- •8.2.1. Баромембранные процессы.
- •8.2.2. Диффузионно-мембранные процессы.
- •8.2.3. Элетромембранные процессы.
- •8.2.4. Термомембранные процессы.
- •8.3. Конструкции мембранных аппаратов.
7.3. Материальный и тепловой балансы кристаллизации. Материальный баланс.

Рис.7.5. Схемы материальных и тепловых балансов кристаллизации:
а – изогидрическая кристаллизация, б – изотермическая кристаллизация.
Материальный баланс процесса кристаллизации по общим потокам веществ может быть представлена в виде:
![]() (7.4)
(7.4)
![]() -
расход начального раствора,
-
расход начального раствора,
![]() -
расход конечного (маточного) раствора,
-
расход конечного (маточного) раствора,
- расход кристаллов (кристаллической фазы),
- поток выпаренной воды.
Баланс по безводному веществу имеет вид:
 (7.5)
(7.5)
хн – начальная концентрация растворенного вещества в растворе,
![]() – конечная
концентрация растворенного вещества
в растворе (маточный раствор).
– конечная
концентрация растворенного вещества
в растворе (маточный раствор).
Здесь
![]() - расход кристаллической фазы в пересчете
на растворенное вещества. Определяем
как:
- расход кристаллической фазы в пересчете
на растворенное вещества. Определяем
как:
![]() (7.6)
(7.6)
где
М- молекулярная масса кристалла без
растворителя,
![]() -
молекулярная масса кристалла с учетом
растворителя. Например, сульфат меди
кристаллизуется при Т=50
-
молекулярная масса кристалла с учетом
растворителя. Например, сульфат меди
кристаллизуется при Т=50
![]() как
как
![]() , а при более высоких Т как
, а при более высоких Т как
![]() .
.
Решая совместно уравнения (7.4) – (7.6) получим расход кристаллической фазы:
 (7.7)
(7.7)
Если кристаллическая фаза не включает растворителя тогда 𝝀=1:
 (7.8)
(7.8)
При изотермической кристаллизации происходит удаление влаги из насыщенного раствора. Поэтому концентрации начального и маточного раствора равны. Тогда получим:
![]() (7.9)
(7.9)
При
изогидрической кристаллизации
![]() ,
и уравнение (7.8) примет вид:
,
и уравнение (7.8) примет вид:
 (7.10)
(7.10)
Тепловой баланс.
Тепловой баланс процесса изогридической кристаллизации может быть записан на основе схемы тепловых потоков, представленных на рис.7.5, в виде:
![]() (7.11)
(7.11)
Здесь
![]() -
расход охлаждающей воды,
-
расход охлаждающей воды,
![]() -
теплота кристаллизации,
-
теплота кристаллизации,
![]() -
потери теплоты в окружающую среду, Н
– энтальпия, индексы: н – начальный, к
– конечный, ох – охлаждающий, т – твердый
(кристалл).
-
потери теплоты в окружающую среду, Н
– энтальпия, индексы: н – начальный, к
– конечный, ох – охлаждающий, т – твердый
(кристалл).
Уравнения (7.11) и (7.4) дают возможность определить расход охлаждающей воды на процесс изогидрической кристаллизации:
 (7.12)
(7.12)
Тепловой баланс изотермической кристаллизации может быть записана основе схемы тепловых потоков, представленных на рис.7.5, в виде:
![]() (7.13)
(7.13)
Здесь
-
расход греющего пара;
![]() ,
,![]() и
и
![]() -
энтальпии греющего пара, конденсата
греющего пара, вторичного пара
соответственно.
-
энтальпии греющего пара, конденсата
греющего пара, вторичного пара
соответственно.
Совместное решение уравнений (7.13) и (7.4) позволяет определить расход греющего пара:
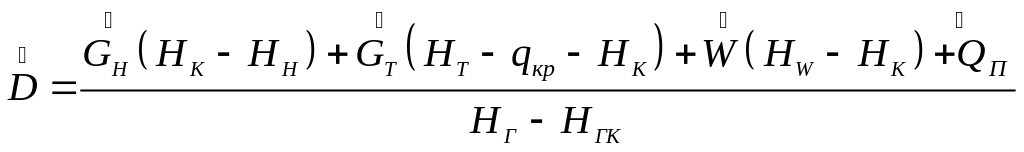 (7.14)
(7.14)
В большинстве случаев при кристаллизации тепло выделяется. В практике кристаллизации теплоту кристаллизации обычно принимает равной по величине и противоположной по знаку теплоте растворения.
