
- •Раздел 1. Общая биохимия Тема: Введение. Химический состав организма человека.
- •1. Введение в биохимию.
- •2 . Химический состав организма человека и его особенности.
- •2. Сухой остаток:
- •3. Свойства внутренней среды организма.
- •4. Понятие об обмене веществ. Роль обмена веществ в организме
- •Тема: Ферменты
- •1. Ферменты как биологические катализаторы.
- •2. Классификация ферментов.
- •3. Строение и механизм действия ферментов.
- •4. Специфические свойства ферментов.
- •Тема: Витамины
- •1. Витамины и их биологическая роль.
- •2. Классификация витаминов.
- •3. Особенности строения водо и жиро растворимых витаминов.
- •4. Понятие о механизмах действия витаминов.
- •Тема: Гормоны
- •1. Гормоны и их биологические свойства.
- •2. Классификация гормонов.
- •1. Биохимические изменения:
- •2. Физиологические изменения
- •3. Морфологические изменения
- •Тема: Биоэнергетика
- •1. Биоэнергетические процессы, основы жизнедеятельности организма.
- •2. Биологическое окисление веществ в организме.
- •3. Ферменты биологического окисления.
- •4. Биохимические механизмы биологического окисления в митохондриях.
- •Тема: Обмен углеводов
- •1. Биологическая роль углеводов.
- •2. Классификация углеводов.
- •Углеводы
- •3. Переваривание и усвоение пищевых углеводов.
- •4. Превращения углеводов в ткань.
- •5. Регуляция обмена углеводов.
- •Тема: Обмен липидов
- •1. Биологическая роль липидов.
- •2. Классификация липидов.
- •3. Переваривание и усвоение пищевых жиров.
- •4. Превращение липидов в тканях.
- •Тема: Белки
- •1. Биологическая роль белков.
- •2. Классификация белков.
- •3. Переваривание и усвоение пищевых белков
- •4. Превращение белков и аминокислот в тканях.
- •Раздел 2. Биохимия спорта Тема: Биохимия мышечной ткани.
- •1. Биологическая роль и строение мышечных волокон (клеток).
2. Классификация ферментов.
Классификация ферментов предусматривает особенности их влияния на химические процессы. В названиях ферментов может быть названия типа химической реакции или вещества на которое действует фермент. В рациональных названиях ферментов присутствует окончание «–аза».
Выделяют 6 классов ферментов:
Оксидоредуктазы – катализируют окислительно-восстановительные реакции.
а. дегидрогеназы б. оксидазы
Трансферазы – катализируют перенос групп атомов между молекулами.
Гидролазы – катализируют гидролиз веществ (распада сложных веществ на простые).
Изомеразы – катализируют реакции образования изомеров.
Синтетазы – катализируют реакции синтеза веществ.
Лиазы – катализируют реакции распада веществ с разрывом углеродной цепи.
3. Строение и механизм действия ферментов.
Молекулы ферментов обладают сложным строением. В строение молекулы 4 основных структуры:
1. Первичная
2. Вторичная
3. Третичная
4. Четвертичная
Активный центр – это участок на поверхности молекул, обладающий сложным строением и обеспечивающий взаимодействие ферментов с определённым субстратом (вещество на которое действует фермент). Под действие активного центра в молекуле субстрата ослабляются связи, поэтому на химическую реакцию требуется меньший расход энергии. Таким образом механизм действия ферментов связан со снижением энергетического барьера реакции.
При взаимодействии фермента субстрата обязательно образуется промежуточный фермент субстратный-комплекс. Под действием активного центра в молекуле субстрата этого комплекса ослабляются определённые химические связи и происходит химическая реакция, с меньшей затратой энергии чем при обычных условиях в клетке без ферментов.
Энергия активации (энергетический барьер реакции) – это количество энергии необходимой для протекания химической реакции в данных условиях клетки. Из всех молекул субстратов при обычных условиях умеют необходимый энергетический уровень (примерно 15-20%), поэтому с участием ферментов энергетический барьер реакций снижается и в ней могут участвовать недостаточно активные молекулы.
1.
Спонтанная реакция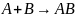 – 100ккал.
– 100ккал.
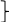 2.
С участием фермента
2.
С участием фермента
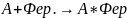 - 30ккал 45 ккал
- 30ккал 45 ккал
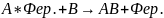 - 15ккал
- 15ккал
Принцип взаимодействие фермента субстрата определяется соответствием структуры поверхности активного центра фермента поверхности молекулы субстрата.
Механизмы взаимодействия условно обозначают как принцип «ключ-замок».
На ряду с общими свойствами белков, ферменты обладают определёнными специфическими свойствами. Активность ферментов зависит от этих свойств, а так же и от особенностей воздействия других веществ на активный центр и белковую часть молекулы фермента.
Ферментов сложного строения (ферментах протеидах) белковая часть молекулы называется апоферментом, не белковая часть такого фермента – коферментом. В состав коферментам могут входить: витамины, пигменты, ионы металлов и другие вещества. Без кофермента, такой фермент не проявляет каталитических способностей.
Активаторы – это вещества повышающие активность ферментов (ионы и соли лёгких металов, витамины, гормоны, метаболиты).
Ингибиторы – это вещества понижающие активность ферментов (ионы и соли тяжёлых металлов, гормоны, метаболиты).
