
- •3.1. Методы восстановления посадок
- •3.2. Классификация способов восстановления деталей
- •3.3. Пластическое деформирование
- •3.4. Ручная сварка и наплавка
- •3.5. Механизированная сварка и наплавка
- •3.5.1. Дуговые способы наплавки
- •3.5.2. Бе3дуговые способы наплавки
- •3.6. Восстановление деталей напылением
- •3.7. Восстановление деталей гальваническими покрытиями
- •3.9. Применение полимерных материалов
- •3.10. Особенности обработки резанием восстанавливаемых деталей
3.7. Восстановление деталей гальваническими покрытиями
Более 85 % деталей тракторов и автомобилей и 95 % деталей двигателей выбраковывают при износе не более 0,3 мм. Их целесообразно восстанавливать гальваническими покрытиями. Рассмотрим преимущества такого способа восстановления перед другими:
отсугствие термического воздействия на детали, вызьтвающего в них нежелательные изменения структуры и механических свойств;
получение с большой точностью заданной толщины покрытий, что приводит к снижению до минимума припуска на последующую механическую обработку и ее трудоемкости или вовсе исключению обработки;
осаждение покрытий с заданными непостоянными по толщине физико-механическими свойствами;
одновременное восстановление большого числа деталей (в ванну загружают десятки деталей), что снижает трудоемкость и себестоимость единицы изделия;
возможность автоматизации процесса.
Общие сведения по электрохимии. Рассмотрим некоторые понятия.
Электродные потенциалы. Если врастворитель (кислоту, щелочь) или в раствор какой-либо соли опустить металлический стержень (например, медный стержень в раствор серной кислоты), то металл будет растворяться и переходить в раствор, образуя положительно заряженные ионы. По мере увеличения концентрации ионов в растворе металл растворяется слабее. При достижении определенной концентрации раствор становится насыщенным и устанавливается подвижное равновесие: какие-то ионы металла переходят в раствор, и в то же время такое же количество ионов из раствора оседает на металле.
Переход ионов в раствор нарушает электрическую нейтральность металла и раствора. Вследствие электростатического притяжения между ионами в растворе и избьиточными электронами на поверхности металла на границе металл—раствор возникает двойной электрический слой с определенной разностью потенциалов (напряжением), которую называют электродным п о т е н ц и а л о м и измеряют в вольтах. Потенциал, соответствующий равновесию между металлом и раствором его соли, называют равновесным.
Значение электродного потенциала зависит от концентрации ионов металла в растворе. Потенциал металла, помещенного в раствор, содержащий 1 моль-ион/л данного металла, называют нормальным или стандартным. Металлы, размещенные в порядке возрастания их нормальных потенциалов, образуют электрохимический ряд напряжений.
Э л е к т р о л и з. Ионы, образовавшиеся в результате электролитической диссоциации, движутся в электролите беспорядочно. Если же в него на некотором расстоянии один относительно другого поместить два токопроводящих электрода, присоединенньих к источнику постоянного тока, то под действием электрического поля ионы будут двигаться направленно. В цепи возникнет электрический ток (рис. 3.34). Электрод, присоединенный к отрицательному полюсу источника тока, называют като дом, а электрод, присоединен- ный к положительному полюсу, — анодом. Положительно заряженные ионы (ионы металлов и водорода) перемещаются к катоду и поэтому их называют катионами, отрицательно заряженные ионьг (ионъi металлоидов и кислотных остатков) — к аноду и называют анионами.
Достигнув поверхности электродов, ноны разряЗкаются, превращаясь в нейтральные атомы или группы атомов. На катоде выделяются металлы и водород, а анод растворяется, и на его поверхности выделяется кислород. На электродах происходят также дополнительные процессы.
При протекании тока через ванну в связи с его различным механизмом прохождения на границах раздела между проводниками первого и второго родов (электроды и электролит) происходят химические реакции: на катоде — реакция восстановления, связывающая электроны, а на аноде — реакция окисления, осво бождающая электроны. Химический процесс, протекающий на электродах при прохождении через электролит электрического тока, называется электролизом. Устройства, в которых за счет внешней электрической энергии совершаются химические превращения веществ, называют электролизерами или гальваническими ваннами.
При гальваническом покрытии деталей в качестве электролита обычно применяют раствор соли осаждаемого металла (в электролит вводят также некоторые компоненты, улучшаюшие свойства покрытий, увеличиваюшие электропроводность электролита и т. д.). Катодом служат предварительно очищенные и подготовленные детали, подлежащие покрытию, а анодом — пластины из осаждаемого металла. Иногда используют аноды из металла или сплава, которые в данном электролите не растворяются (свинец), а такжс нерастворимые аноды из графита. На таких анодах обычно выделяется кислород.
Электролиз сводится в основном к тому, что находящиеся в электролите ионы металла разряжаются на катоде, переходя в атомарное состояние, и осаждаются на нем. Атомы образуют кристаллическую решетку, покрывая поверхность детали слоем металла. Анод растворяется (в случае электролиза с растворимым анодом), образуя новые ионы металла взамен выделившихся на катоде, тем самым поддерживая концентрацию электролита.
Количественно процесс электролиза подчиняется двум законам, открытым Фарадеем, названным впоследствии законами Фарадея:
масса вещества, выделившегося на катоде или растворившегося на аноде, прямо пропорциональна силе тока и времени его прохож-. дения, т. е. прямо пропорциональна количеству прошедшего через электролит электричества;
при прохождении одного и того же количества электричества через разные электролиты массы выделившихся или растворившихся веществ пропорциональньи их химическим эквивалентам.
Фарадей установил, что для выделения одного моль-эквивалента* любого вещества необходимо пропустить через электролит Р= 96 500 Кл (кулонов) электричества. Это число названо постоянной Фара дея.
Масса вещества, выделившегося на катоде или растворившегося на аноде при прохождении через электролит единицы количества электричества, называют электрохимическим эквивалентом. Для каждого вещества это постоянное значение, зависящее от природы вещества и определяемое делением его химического эквивалента на постоянную Фарадея.
Оба закона Фарадея в общем виде выражают формулой
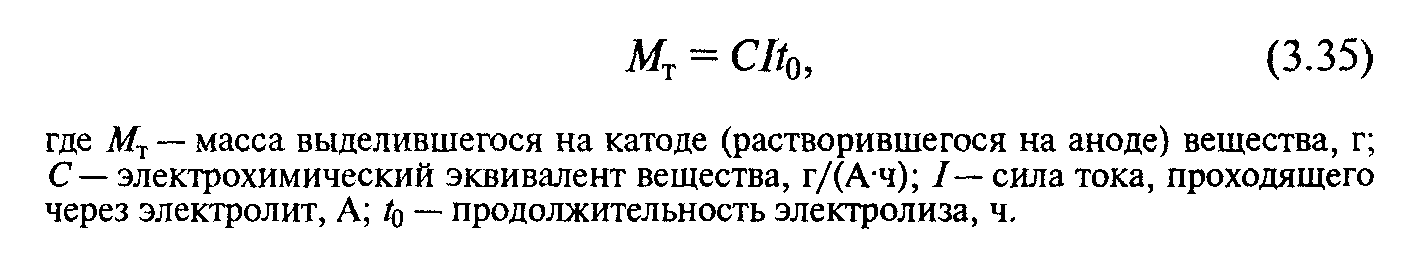
При электролизе одновременно с осаждением металла на катоде выделяется водород, а также протекают и другие побочньие процессы, на что затрачивается часть электрического тока. Поэтому действительная масса осажденного металла будет меньше теоретической, рассчитанной по закону Фарадея. Отношение практически полученного на катоде количества металла М к теоретически возможному называют катодным выходом металла по току, который выражают в процентах, т. е.
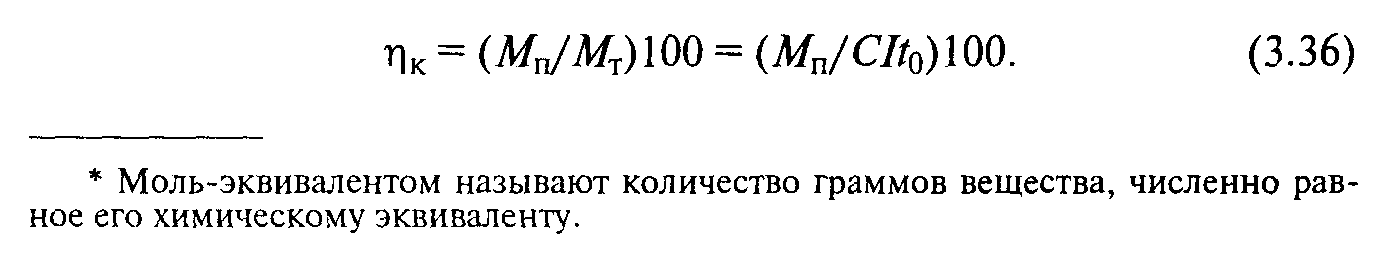
Это важнейший показатель электролиза. Его физический смысл заключается в том, что он представляет собой коэффициент использования электрического тока (иногда его называют КПд ванны, что неверно, так как кпд характеризует использование энергии, а не тока). Например, при хромировании т 10...18 %, а при Жедезнении т’= 85...95 %. Это означает, что при хромировании лишь 10... 18 % затраченного на электролиз электричества полезно используется на осаждение металла, тогда как при железнении — 85...95%.
Отношение количества металла, практически растворенного на аноде, к теоретически возможному называют анодным выходом по току.
Условия электролиза обусловливаются составом и концентрацией электролита и режимом процесса. Последний характеризуется тремя основными показателями: кислотностью электролита (в г/л или в единицах водородного показателя рН); температурой электролита (в °С); катодной плотностью тока (в А/дм2).
Зная законы Фарадея и режим электролиза, можно найти среднюю толщину осажденного на катоде покрытия в зависимости от продолжительности электролиза и, наоборот, определить время, необходимое для получения покрытия заданной толщины:
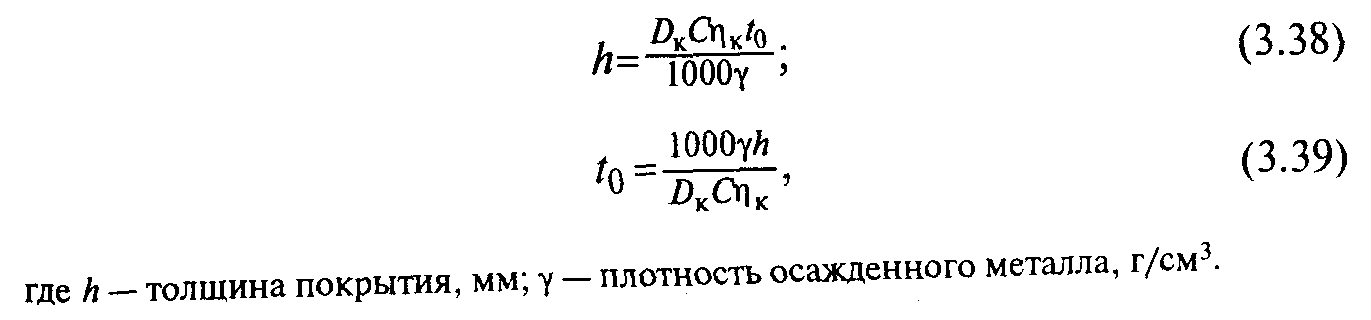
Поляризация электродов. Электролиз происходит тогда, когда к электродам от внешнего источника тока приложено некоторое напряжение, сдвигающее их потенциалы от равновесного значения. Разность между потенциалом электрода под током и его равновесным потенциалом называют электродной поляриза цией (перенапряже нием).
При электролизе изменяется концентрация ионов у электродов:
концентрация катионов у катода становится меньше, а у анода больше, чем в основном объеме электролита, т. е. обедшiется прикатодный слой электролита и обогащается прианодный. Электродный потенциал зависит от концентрации ионов у поверхности электрода. В связи с ее увеличением или уменьшением изменяется и значение потенциала, т. е. возникает кон центра ционная поляризация электрода.
Ноны переносятся из глубины электролита к поверхности катода путем диффузии, конвекции и миграции. Факторы, ускоряющие перемещение ионов в электролите и уменьшающие изменение их концентрации у электродов (перемешивание, повышение температуры электролита и др.), снижают концентрационную поляризацию.
Поляризация, возникающая при электролизе в результате затруднения (замедленного) протекания электрохимических реакций (разряда ионов и образования нового вещества), называют химической. Она зависит от природы разряжающегося иона, состава и температуры электролита, природы и состояния поверхности катода и характерна для металлов группы железа (железо, никель и кобальт).
Суммарная поляризация катода или анода складывается из концентрационной и химической и называется соответственно катодной или анодной поляриза цией.
Рассеивающая способность электролитов. Одно из требований, предъявляемых к гальваническим покрытиям, — их равномерная толщина на всей поверхности изделия. Однако их получение связано с определенными трудностями. Даже на плоских катодах, расположенных на одинаковом расстоянии от анодов, покрытие распределяется неравномерно: на углах и краях толщина больше расчетной, на средней части меньше. Особенно явно это наблюдается на профилированных изделиях с большими выступами и углублениями.
Равномерность распределения толщины покрытия зависит от природы электролита. Она различна для изделий одной и той же форм ы, но покрываемых в разных электролитах. Свойство электролита давать равномерные по толщине покрытия называют его рассеивающей способностью.
На толщину покрытий большое влияние оказывает взаимное расположение катода и анода. Для улучшения равномерности используют следующие приемы:
устанавливают дополнительные и фигурные аноды (рис. 335, а и д), повторяющие форму покрываемых изделий так, чтобы расстояния между всеми участками катода и анода были примерно равными.
Помимо рассеивающей способности различают еще так называемую кроющую способность электролита. В отличие от первой она не дает представления о равномерности толщины покрытия, а лишь характеризует свойство электролита покрывать всю поверхность катода, в том числе различные углубления.
Свойства гальванических покрытий. Эти свойства определяются структурой покрытий. Под структурой понимают размер и форму кристаллов (крупнокристаллическая и мелкокристаллическая, волокнистая, слоистая, столбчатая и др.). Определенную ориентацию кристаллов в покрытии называют текстурой. Часто кристаллы называют зернами (структура мелкозернистая, крупнозернистая).
Выщеление металла при электролизе рассматривается как процесс кристаллизации (электрокристаллизации). Металл выделяется на катоде в особых условиях, отличных от кристаллизации из расплавленного состояния. Поэтому и свойства электроосажденных металлов отличаются от свойств тех же металлов, полученных металлургическим путем. Так, для многих металлов, в том числе для железа и хрома, характерны повышенная твердость и хрупкость.
Электрокристаллизация складывается из двух одновременно протекающих процессов: образования центров кристаллизации (кристаллических зародьтшей) и роста кристаллов. Каждый из них проходит с определенной скоростью, зависящей от условий электролиза. В зависимости от соотношения скоростей образования этих центров и роста кристаллов изменяются структура покрытий и связанные с нею физико-механические свойства. При преобладании первого процесса образуется мелкокристаллическая структура, второго — меньше новых центров, но усиливается рост кристаллов. Возникает крупнокристаллическое покрытие.
Наиболее ценными техническими свойствами характеризуются мелкокристаллические покрытия. Поэтому необходимо знать условия получения последних при электролизе. Установлено, что повышение катодной поляризации всегда способствует увеличению скорости зарождения новых кристаллов и образованию мелкокристаллических покрытий. Поляризация, а следовательно, и структура покрытий зависят от условий электролиза: состава, концентрации,
температуры и кислотности электролита, плотности тока, вида тока (постоянный или переменный), перемешивания и др.
Чтобы уменьшить размеры кристаллов, следует в электролиты, содержащие простые соли, вводить различные органические вещества (желатин, фенол, сахарин, декстрин и др.). С этой же целью, а Также для повышения электропроводности и рассеивающей способности электролитов в них добавляют соли (например, сернокислый натрий — в электролит при цинковании).
На структуру покрытий влияет режим электролиза. Повышение плотности тока и понижение температуры электролита приводят к снижению размеров кристаллов. Однако увеличивать плотность тока можно лишь до определенного значения. При высоких его плотностях прикатодный слой быстро обедняется разряжающимися ионами металла. Это способствует осаждению напряженных, хрупких и некачественных покрытий с большим количеством децдритов (наростов) на выступающих участках. Чем ниже концентрация и температура электролита, тем меньше допустимая плотность тока.
Чтобы повысить производительность процесса без снижения качества покрытий, необходимо увеличить допустимую плотность тока за счет роста концентрации и температуры электролита, а также его принудительным интенсивным перемешиванием (циркуляцией).
Снижение кислотности электролита ухудшает качество покрытий: они становятся темными, хрупкими и шероховатыми. Это объясняется тем, что в прикатодном слое образуются гидроксидью металлов, которые включаются в покрытие. Особенно заметно влияние кислотности на структуру и свойства покрытий при осаждении таких металлов, как железо, никель и кобальт.
Последние могут достигать больших значений и превышать прочность на разрыв самого покрытия, В этом случае в покрытии появляются трещины и оно становится пористым. Чем больше напряжения, тем мельче и чаще встречаются трещины.
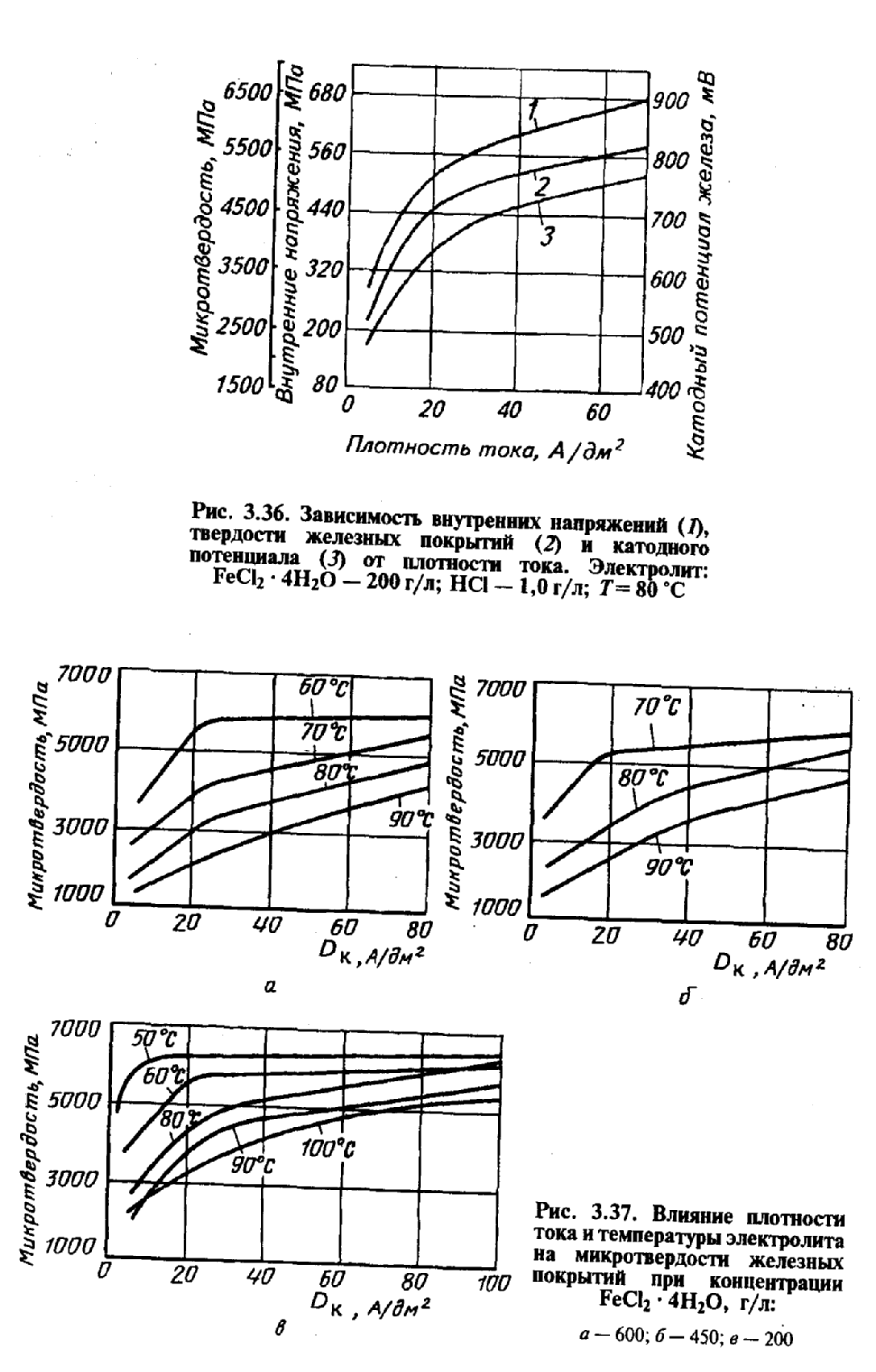
Важнейшая характеристика свойств гальванических металлов — твердость, которая наиболее доступна для изучения и вто же время тесно связана с другими свойствами. Чем больше катодная плотность тока, тем выше катодная поляризация, внутренние напряжения и твердость железных покрытий (рис. 3.36). Чем жестче режим электролиза, чем меньше размеры кристаллов и тем больше твердость покрытия (рис. 3.37).
Наилучшая износостойкость у покрытий с высокой твердостью и одновременно достаточной пластичностью. Из рисунка 3.38 видно, что оптимальное значение твердости железных покрытий различно в зависимости от материала соединенной при трении детали.
При хромировании в зависимости от условий электролиза в широких пределах изменяются структура, твердость, внешний вид и другие свойства покрытий. С уменьшением температуры (рис. 3.39) электролита и повышением плотности тока увеличивается твердость покрытий, а их внешний вид изменяется от молочного до блестящего и серого цвета. Наибольшей износостойкостью характеризуются блестящие хромовые покрытия. У молочных покрытий наибольшие пластичность и защитные свойства, и их относят к менее напряженным и твердым.
Технология нанесения гальванических покрытий. Технологический процесс состоит из трех групп операций: подготовки деталей к наращиванию нанесения покрытия и последующей обработки.
Подготовка деталей. Сцепление металла покрытия с металлом детали ОбуслОвливается их межмолекулярным взаимодействием. Межмолекулярные силы заметно проявляются только в ТОМ случае, если расстояние между атомами составляет не более 5-10 мКм.
Покрываемым поверхностям придают необходимую шероховатость. С них удаляют различные загрязнения, жировые и оксидные пленки. Металл осаждается на активном чистом катоде, свободном от чужеродных частиц. В результате покрытие физически сращивается с основным металлом настолько прочно, что не отслаивается от детали даже при ее разрушении и работает как одно целое с основным металлом. Нарушение технологии подготовки уменьшает его сцепляемость и может привести к отслаиванию от детали.
Механическая обработка предназначена для удаления с покрываемой поверхности следов ИЗНОСА и придания ей требуемой шероховатости. В Процессе восстановления детали обычно шлифуют до шероховатости соответствующей 6...7-му классу, или зачищают шкуркой (при небольших равномерных износах).
Промывки органическим растворителем (бензином, керосином и др.) применяют тогда, когда необходимо дополнительно очистить деталь от грязи и масла, скопившихся в углублениях, отверстиях и т. д.
Изоляция поверхностей деталей, не подлежащих покрытию, токонепроводящими материалами служит для сохранения геометрических размеров поверхностей, предотвращения потери электроэнергии и металла. Ее выполняют с помощью постоянных изоляторов (коробки, трубки, шайбы и т. д.) или изоляционных материалов (тонкой резины, листового целлулоида, изоляционной ленты, пленочных полимерных материалов, церезина, пластизоля и др.).
Монтаж деталей на подвеску выполняют для их завешивания в ванну с электролитом. Конструкция подвески должна создавать надежный электрический контакт с покрываемыми деталями и штангой ванны, детали располагают вертикально или наклонно для удаления водорода с поверхностей.
При химическом методе детали погружают в горячий щелочной раствор и вьщерживают в нем определенное время.
Продолжительность процесса (5... 60 мин) зависит от температуры раствора и степени загрязнения изделий. Для обезжиривания сталей и чугуна рекомендуется применять раствор, содержащий до 50 г/л едкого натра, по 15.. .35 г/л тринатрийфосфата и кальцинирова иной соды и 3...5 г/л синтанола ДС-ю. В растворы добавляют 3...5 г/л жидкого стекла или метасиликата натрия. Примерная щелочность раствора (рН) при обезжиривании черных металлов до 12.

К разновидности химического обезжиривания относят обезжиривание венской известью, которая представляет собой смесь оксидов кальция и магния с добавлением 1...1,5 % едкого натра. Ее разводят водой до кашицеобразного состояния, наносят на поверхность и протирают деталь волосяной щеткой. Это трудоемкая операция, но она дает хорошие результаты, особенно в условиях небольших предприятий.
Сущность электрохимического обезжиривания заключается в том, что изделия, погруженные в щелочной раствор, включают в цепь электрического тока в качестве катода или анода. На поверхности электродов бурно выделяются пузьтрьки газа (водород на катоде, кислород на аноде). Они облегчают эмульгирование жиров и масел, механически разрывают и удаляют их пленки, ускоряя тем самым в несколько раз процесс. Скорость последнего мало зависит от концентрации и температуры раствора (60... 80 °С) и определяется плотностью тока, которая обычно составляет 3... 10 А/дм2. Чем больше жировых загрязнений на поверхности деталей, тем больше должна быть плотность тока.
Для обезжиривания черных металлов рекомендуется применять раствор, содержащий по 20.. .40 г/л едкого натра, тринатрийфосфата и кальцинированной соды. В него можно вводить 3...5 г/л жидкого стекла или метасиликата натрия. Электрохимическое обезжиривание ведут на катоде или аноде. На первом вьщеляется в 2 раза больше газа, чем на втором, т. е. производительность обезжиривания на катоде выше, чем на аноде.
Однако при обезжиривании на катоде поверхность детали насыщается водородом (водород проникает внутрь металла). В результате увеличивается ее хруггкость и снижается усталостная прочность. Кроме того, ухудшается сдепление покрытий с поверхностью и даже может произойти их отслоение.
После обезжиривания детали тщательно промывают сначала горячей (70.. .80 °С), а затем холодной водой. Если она равномерно растекается и смачивает всю поверхность детали, а не собирается каплями, то качество обработки хорошее.
Травление предназначено для удаления оксидных пленок и дефектного слоя с покрываемых поверхностей, выявления кристаллической структуры и повышения активности металла. Его проводят химическим и электрохимическим методами.
Химическое травление черных металлов выполняют в водном растворе серной или соляной кислоты или в их смесях. Обычно применяют 15.,.25%-й раствор серной или 10...20%-й раствор соляной кислоты. При травлении в растворе серной кислоты его часто агревают до 50.. .60 °С. Продолжительность процесса (30 мин и более) зависит от состояния поверхности детали, концентрации и температуры раствора.
На ремонтных предприятиях этот способ чаще всего служит при подготовке метизов и других мелких деталей к цинкованию и очистке наплавочной проволоки от ржавчины.
Чтобы ускорить процесс и повысить прочность сцепления гальванических покрытий, следует применять электрохимическое травление. Его скорость увеличивается в десятки раз, а расход кислоты уменьшается. Для травления черных металлов обычно используют растворы кислот, чаще серной, и солей соответствующих металлов. детали завешивают в ванну и включают в качестве катода или анода в электрическую цепь.
Наиболее распространено анодное травление, происходящее за счет электрохимического растворения металла, химического растворения и механического отрывания оксидов от его поверхности Выделяющимся на аноде кислородом.
В ремонтном производстве такое травление применяют для восстановления изношенньих деталей железнением и хромированием.
Через некоторое время после начала травления напряжение на ванне повышается, а сила тока снижается. Это объясняется переходом металла из активного состояния в пассивное (пассивирование поверхности) и сопровождается бурным выделением кислорода. Пузырьки последнего срывают травильный шлам, и обрабатываемая поверхность становится чистой с отчетливо выявленной кристаллической структурой и специфическим микрорельефом.
Качество обработки контролируют визуально: для правильно протравленных деталей характерна светло-серая матовая поверхность без блеска, темных пятен и следов травильного шлама.
Для деталей большой массы и сложной конфигурации, изготовленных из высоколегированных сталей и особенно закаленных до высокой поверхностной твердости, при таком травлении не всегда достигается хорошая прочность сцепления. Поэтому применяют двойное травление: сначала в растворе хлористого железа (электролите железнеяня), а затем в 30%-м растворе серной кислоты. Стальные детали травят в ванне железнения при анодной плотности тока 40... 80 А/дм2 в течение 2.. 5 мин (в зависимости от состояния поверх-. ностидеталей), а чугунные при 15...20 А/дм2 в течение 1...2 мин.
При анодном травлении стали в хлористом электролите на ее поверхности не образуется пассивная пленка. В результате достигается более глубокое и равномерное протравливание деталей, чем при травлении в растворе серной кислоты. Однако после этого на обрабатываемой поверхности остается темный рыхлый слой шлама. Его удаляют анодньим травленчем (очисткой) в 30%-м растворе сернои кислоты при плотности тока 50...70 А/дм2 в течение 0,5...1,0 мин. На поверхности образуется пассивная пленка.
Перед анодной очисткой детали промьтвают холодной водой, чтобы удалить с них и подвесных приспособлений остатки хлористого электролита. Накопление ионов хлора (активаторов) в сернокислом электролите нарушает процесс анодной очистки, препятствуя образованию пассивной пленки и удалению шлама. Детали снимают со штанг ванны при выключенном токе, иначе ухудшается сцепляемость покрытий и увеличивается количество браковаяяых изделий. То же самое происходит, если оставить детали в ванне после травленчя.
Перед хромированием детали подвергают анодному травлению в растворе, содержащем 100...150 г/л хромового ангидрида и 2...3 г/л серной кислоты, или непосредственно в электролите для хромирования. Стальные детали обрабатывают при анодной плотности тока 25.. .40 А/дм2 в течение 30.. .60 с (чем более углеродистая и легированная сталь, тем меньше время травления), а чугунные — при 20.. .25 А/дм2 в течение 5... 10 с. Температура электролита 50.. .60 ос.
Нанесение покрытий. В ремонтном производстве из гальванических покрытий чаще всего применяют железнение и реже — хромирование, цинкование и никелирование.
Железнение характеризуется хорошими технико-экономическими показателями: исходные материалы и аноды дешевые и недефицитньте; высокие выход металла по току (85... 95 %) и производительность — скорость осаждения железа составляет 0,2.. .0,5 мм/ч; толщина твердого покрытия 0,8... 1,2 мм; возможность в широких пределах регулировать свойства покрытий (микротвердость 1600... 7800 МПа) в зависимости от их назначения обусловливает универсальность процесса; достаточно высокая износостойкость твердых покрытий, не уступающая износостойкости закаленной стали; покрытия хорошо хромируются, что позволяет при необходимости повышать износостойкость деталей нанесением более дешевого, чем хромовое, комбинированного покрытия (железо + хром).
Железнение используют в случаях:
при восстановлении малоизношенных деталей (наращивании до номинальяого или ремонтного размера) автомобилей, тракторов, сельскохозяйственных машин, различного оборудования;
исправлении брака механической обработки;
упрочнении рабочих поверхностей деталей из малоуглеродистой и среднеуглеродистой сталей, не прошедящих в процессе изготовлении термической обработки.
Металлы группы железа в соединениях могут быть двух- и трехвалентными. ЭлектроосаЖдение происходит из растворов двухвадентных соединений. Находящиеся в электролите двухвалентные ионы металла легко окисляются до трехвалентных кислородом воздуха. При наличии таких ионов снижается выход металла по току и ухудшаются свойства покрытий.
По составу (по виду аниона соли железа) элеКтролить[ делят на три группы: хлористые, сернокислые и смешанные (сульфатно-хлористые).
По температурному режиму электролиты делят на горячие и холодные. Первые используют при температуре 60...90 °С, позволяющей проводить Железнение с большой плотностью тока и высокой производительностью. Однако они менее удобны в эксплуатации — требуются большой расход энергии на нагрев и поддержание высокой температуры, их частая корректировка, мощная вентиляция и др. Вторые (электролиз ведется без нагрева) лишены указанных недостатков, но допускается использовать Меньшие плотности тока и поэтому холодные электролиты менее производительны.
Однако высокая стоимость аскорбиновой кислоты препятствует ее широкому применению.
Хромирование служит ддя получения мелкозернистых покрытий микротвердостью 4000...12 000 МПа с низким коэффициентом трения и высокой сцепляемостью. Хром химически стоек против воздействия многих кислот и щелочей, жароустойчив, что обеспечивает деталям высокую износостойкость даже в тяжелых условиях эксплуатации, превышающую в 2...5 раз износостойкость закаленной стали. Наибольшая износостойкость покрытия получается при твердости 7000.. .9200 МПа.
Однако хромирование — энергоемкий, дорогой и малопроизводительный процесс. Его используют для следующих целей:
защитнО-декоративное хромирование арматуры автомобилей, велосипедов, мотоциклов, вагонов и т. д.;
увеличение износостойкости и ресурса пресс-форм, штампов, измерительных и режущих инструментов, трущихся поверхностей деталей машин (поршневых колец, штоков гидроцилиццров, плунжеров топливных насосов) и др.;
восстановление малоизношенньгх ответственных деталей автомобилей, тракторов и различного оборудования;
повышение отражательной способности при изготовлении зеркал, отражателей и рефлекторов.
Для этого процесса в отличие от других характерны следующие особенности.
1. Главным компонентом электролита служит хромовый ангидрид (ОО), образующий при растворекии в воде хромовую кислоту (Сг03 + Н20 = Н2СгО4). Главный компонент при других процессах — соль осаждаемого металла. Хром осаждается лишь при наличии в электролите определенного количества посторонних анионов, чаще всего сульфатов (О). Он шестивалентен в электролите. На Катоде осаждается двухвалентный металлический хром. Механизм его осаждения есьма сложен и еще недостаточно изучен.
2. Большая часть тока расходуется на побочные процессы, в том Числе на разложение воды и обильное выделение водорода, в результате чего выход хрома по току мал (10...40 %). С увеличением Концентрации и температуры электролита выход по току уменьшается, тогда как при осаждении других металлов, наоборот, увеличиВается.
3. Хромовый анод растворяется при электролизе с анодным выходом по току, в 7.. .8 раз превышающим выход по току на катоде. В результате концентрация ионов хрома в электролите непрерывно возрастает. Применяют нерастворимые аноды, изготовленные из свинца или из сплава свинца с 6 % сурьмы. При использовании нерастворимых анодов электролит постоянно обедняется и его необходимо периодически контролировать и корректировать, добавляя хромовый ангидрид.
Для хромирования применяют простые сульфатные электролиты 1,2 и 3, состоящие из хромо вого ангидрида, серной кислоты и воды (табл. 3.17).

На процесс большое влияние оказывает соотношение между концентрациями хромового ангидрида СтО3 и серной кислоты Н2О4. Для осаждения покрытий хорошего качества и с наибольшим выходом по току необходимо, чтобы оно было равным 100 (допускается изменение от 90 до 120). С этой же целью в электролите должно быть 1.. .2 % (от количества СтОз) ионов трехвалентного хрома, который получают проработкой электролита током плотностью 4.. .6 А/дм2 при температуре 45.. .50 °С и соотношении.
Малоконцентрированный (разведенный) электролит отличается лучшей рассеивающей способностью и более высоким выходом по току. Покрытия, полученные в нем, характеризуются наибольшей твердостью и износостойкостью. Однако электролит нуждается в частом добавлении СтО3, и его применяют при износостойком хромировании и восстановлении изношенньих деталей.
Концентрированный электролит отличается низким выходом потоку и плохой рассеивающей способностью. Вместе с тем он обладает большей стабильностью по концентрации СтО3 и соотношению СтО3 : Н2О4, не требует высокого напряжения на ванне. Внем осаждаются плотные и менее напряженные покрытия. Этот электролит используют при защитно-декоративном хромировании деталей СЛОЖНОЙ конфигурации.
С помощью электролита получают как твердые износостойкие покрытия, таки покрытия с хорошими защитнодекоративными свойствами. Его обычно называют универсальным или стандартным.
Введенные в электролит соли в количествах, превышающих СВОЮ растворимость, будут находиться в небольшом избытке на дне ванны в виде твердой фазы. Содержание ионов в растворе при изменении концентрации СтО3 будет постоянным за счет частичного растворения этого избытка.
К достоинствам такого электролита по сравнению с сульфатными относят следующие: стабильность состава, что уменьшает частоту его корректировки; колебания температуры электролита и плотности тока меньше отражаются на внешнем виде покрытий и выходе по току; хорошая рассеивающая способность и более высокие свойства покрытий; большой выход по току (18.. .20 %) позволяет в 1,3... 1,5 раза увеличить производительность хромирования.
Однако саморегулирующийся электролит более сложен по составу, чувствителен к хлоридам и характеризуется большой агрессивностью. Последняя приводит к тому, что участки деталей, которые не покрываются хромом (вследствие низкой плотности тока на них, экранирования и т. д.), растворяются в электролите, даже будучи катодно поляризованными. Поэтому такой электролит не получил широкого применения.
Саморегулирующийся холодный электролит имеет высокие выход по току (35...40 %) и скорость осаждения хрома (0,18...0,50 мм/ч), примерно в 10 раз превышающую скорость осаждения из обычных электролитов при хорошем качестве покрытий. Однако для поддержания температуры 18...25 °С при плотности тока до 300 А/дм2 требуется МОЩНЫЙ холодильный агрегат.
Обычные хромовые покрытия плохо смачиваются маслами и прирабатываются. Чтобы повысить износостойкость деталей, работающих при больших давлении и температуре и недостаточной смазке, следует применять пористое хромирование. Пористый хром представляет собой покрытие, на поверхности которого специально создаются большое количество пор или сетка трещин, достаточно широких для проникновения в них масла. Его можно получить механическим, химическим и электрохимическим способами.
Наиболее широко используют электрохимический способ. Он заключается в том, что покрытие осаждают с сеткой микротрещин. для их расширения и углубления покрытие подвергают анодной обработке в электролите того же состава, что и при хромировании (поверхность трещин активнее и растворяется гораздо быстрее других участков хрома). В зависимости от режима хромирования и анодного травления можно выполнить канальчатую иточечную пористость.
Для образования пористых покрытий деталь хромируют в универсальном электролите при плотности тока 40.. .50 А/дм2, а затем переключают полярность ванны и проводят анодное травление при той же плотности. Канальчатую пористость получают при температуре электролита 58...62 ос и продолжительности травления 6...9 мин, а точечную — 50.. .52 ос и 10...12 мин. На анодное травление оставляют припуск 0,01...0,02 мм на диаметр.
Пористое хромирование поршневых колец увеличивает их износостойкость в 2...3 раза, а износостойкость гильзы — в 1,5 раза.
Цинкование чаще всего применяют в ремонтном производстве для защиты от коррозии крепежных деталей и восстановления посадочных поверхностей малонагруженных деталей.
Кислые электролиты характеризуются плохой рассеивающей способностью, а покрытия, полученные в них, — меньшей коррозионной стойкостью, чем в щелочных. В то же время они устойчивы, допускают применение высокой плотности тока при выходе цинка по току, близком к 100 %. Ими покрывают простые малорельефные изделия.
Щелочные цинкатные (I”Г 2), аммиакатные (I 3) и другие электролиты просты по составу и дешевы. У них высокая электропроводность и хорошая рассеиваюшая способность. Основной недостаток аммиакатных электролитов — наличие в сточной воде солей аммония, которые затрудняют ее нейтрализацию и недопустимы по требованиям санитарии (допускается не более 2,5 мг/л).
Обработка деталей после покрытия. После нанесения покрытия детали промывают водой и подвергают нейтрализации в щелочных растворах для удаления следов электролитов и предупреждения коррозии. Например, после хромирования их нейтрализуют в растворе альцинированной соды (20.. .70 г/л) при 15... 30 осн течение 15.. .30 с. Особенно тщательно необходимо обрабатывать детали, покрываемьте в хлористых электролитах, так как оставшиеся ионы хлора вызывают интенсивную коррозию покрытия во влажной атмосфере. для этого их промывают и нейтрализуют в 10%-м растворе щелочи при температуре 60...80 ос в течение 5... 10 мин.
Чтобы повысить коррозионную стойкость цинковых покрытий, их необходимо пассивировать, обрабатывая в растворах хромовой КИСЛОТЫ ИЛИ ее солей. В результате на поверхности цинка образуется хроматная пленка радужных отгенков (от светло-желтого до розового и фиолетового).
Термическая обработка служит для сушки ИЛИ улучшения свойств покрытий. Детали сушат в сушильном шкафу при 50... 100 ос в течение 5...10 мин. Температура сушки оцинкованнъ деталей после паСсивирования не должна превышать 50.. .60 ос.
При электролизе вьщеляется водород, который внедряется в покрытие, что увеличивает хрупкость, снижает усталостную прочность детали и сцепляемость покрытия. Поэтому ответственные хромированные детали, работающие при больших динамических нагрузках или же требующие повышенной точности и стабильности размеров (плуижерные пары), обезводороживают, нагревая их при температуре 180...23О С в течение 2...3 ч. Железофосфорные и никельфосфорньие покрытия подвергают термообработк при температуре 400 ос в течение 1,0...1,5 ч для повышения твердости, износостойкости и сцепляемости.
При механической обработке мягкие покрытия точат, а твердые — шлифуют или хонингуют.
Способы нанесений гальванических покрытий. Рассмотрим некоторые из них.
Ванные способы. Детали помещают в электролит находящийся в какой-либо емкости (в Стационарных ваннах, Колоколах, КОЛОКОЛЬНЫХ и барабанных Ваннах).
В нее входят: нагревательное устройство (при необходимости); бортовые отсосы для удаления вредных испарений; катодные и анодньие штанги, подсоединенные к источнику тока, для завешивания деталей и анодов. Внутреннюю поверхность ванны футеруют кислотостойкими материалами.
Мелкие детали (например, метизы при цинковании) покрывают во вращающихся колоколах и барабанах из токонепроводящего кислотостойкого материала.
Колокол имеет форму усеченного конуса. Он приводится во вращение с частотой 8... 15 мин. Ток к деталям (катоду), насыпанным в корпус, подводится с помощью металлических щеток или опусканием в него стержня или провода с грузом, контактирующим с деталями. Анод представляет собой пластину, опускаемую в корпус на переносном штативе.
Детали загружают в колокол с электролитом, в который помешают анод, включают механизм его вращения и источник тока. При вращении детали пересыпаются, контактируют с катодом и между собой. Некоторые из них временно могут оказаться не под током. По окончании электролиза КОЛОКОЛ наклоняют над баком с сеткой. детали попадают в сетку, а электролит стекает в бак, откуда он снова заливается в колокол.
К недостаткам колокольных ванн относят: быстрый нагрев электролита, низкую производительность и значительные потери электролита.
Б е з в а н н ы е с п о с о б ы. При восстановлении корпусных и других крупных деталей площадь наращиваемых поверхностей мала по сравнению со всей площадью. Поэтому их наращивают безванньтми способами: проточным, струйньим, электроконтактным идр.
Принцип такого нанесения заключается в том, что у поверхности, подлежащей покрытию, с помощью несложных устройств создают местную электролитическую ячейку (ванночку), в которую подают элетсгролит, а деталь и анод подключают к источнику тока.
При проточном способе электролит прокачивают насосом с определенной скоростью через пространство между покрываемой поверхностью и анодом (например, через отверстие в корпусе коробки передач). Наибольшая скорость осаждения металлов достигается при скорости протекания электролита более 1 м/с, создающей турбулентный режим течения. Плотность тока может быть увеличена в 5...1О раз (при железнении —до 200...30О А/дм2 и более).
При струйном способе электролит подают струями в межэлектродное пространство через отверстия насадка. Последний одновременно служит анодом З (рис. 3.43, а) и местной ванночкой. Для получения равномерного покрытия деталь вращается с частотой до 20 мин. Этого можно достичь и при Неподвижной детали, если отверстия в аноде, через которые поступает электролит, выполнить под углом 30.. .40° к радиальному направлению (рис. 3.43, 6).
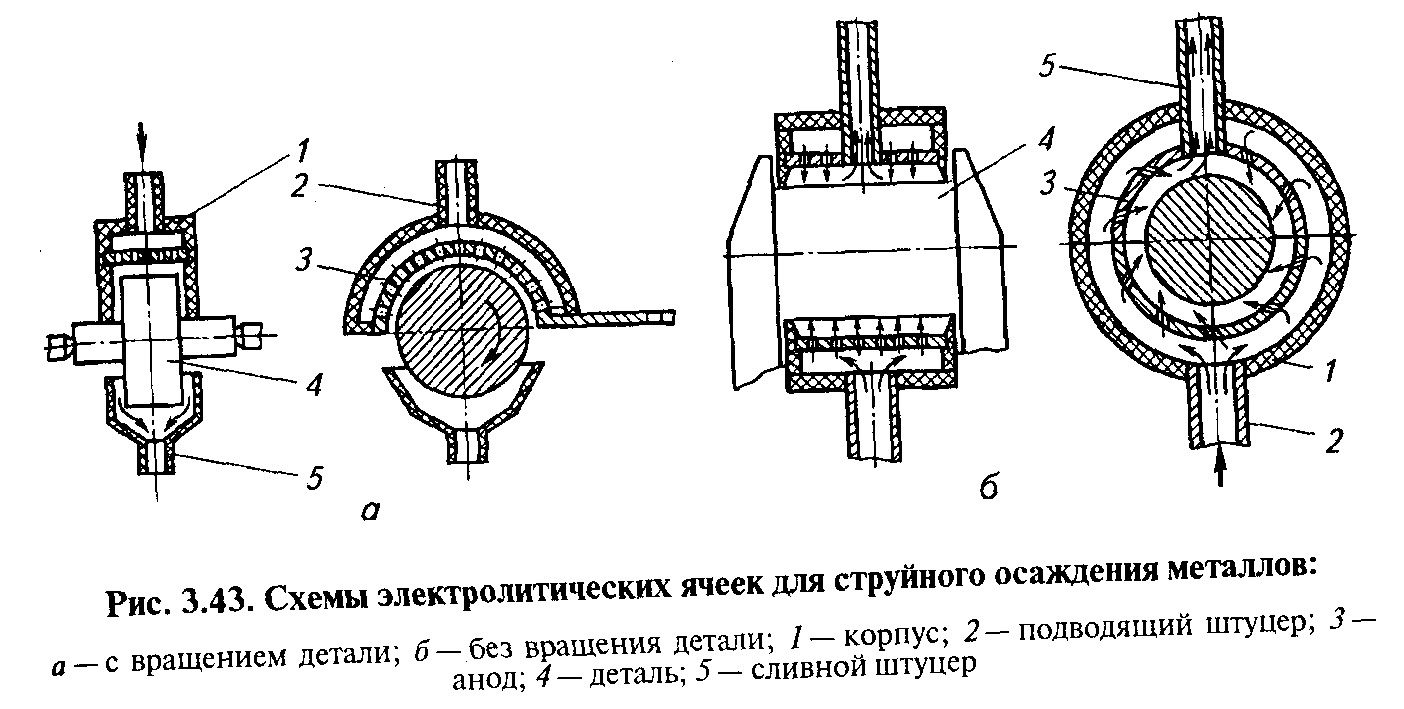
При проточном и струйном способах за счет уменьшения обед- нения прикатодного слоя электролита создаются условия, позволяющие в 2... 3 раза повысить производительность процесса. Эти способы обеспечивают более высокое Качество покрытий и лучшую равномерность. Первым восстанавливают посадочные поверхности корпусных деталей (блоков цилиндров, корпусов коробок передач и др.), а вторыми — крупные валы, например коленчатые.
В ремонтном производстве применяют также местное осаждение при неподвижном электролите.
Отверстие герметизируют СНИЗУ, заливают в него электролит 2 (рис. 3.44), устанавливают анод З и подключают к источнику тока. Само отверстие СЛУЖИТ ванночкой. Этот способ часто применяют для восстановления посадок под подшипники в корпусных деталях.


Электролиз происходит в очень маленьком объеме электролита без регулирования температуры. В результате он обедняется, перегревается и усиленно испаряется. Поэтому местным железнением трудно получить высококачественные покрытия толщиной более 0,3 мм. для увеличения объема электролита и улучшения условий электролиза устанавливают стакан бп кольцо 4.
Сущность электроконтактного способа (электронатирания) заключается в том, что электроосаждение металла происходит при прохождении постоянного тока через маленькую ванночку. Последняя образуется в зоне контакта покрываемой детали 7(рис. 3.45) с анодом З, обернутым адсорбирующим, пропитанным электролитом материалом. деталь и анод перемещаются одна относительно другого (деталь вращается при неподвижном аноде, или наоборот), т.е. возникает трение анода по детали.
Чаще используют нерастворимые аноды, представляющие собой угольный стержень, плотно обернутый адсорбирующим материалом (обычной или стеклянной ватой, губкой в суконном чехле, фетром, войлоком, капроном). Обертку называют анодньтм тампоном. Он непрерывно смачивается электролитом, который поступает к нему через шланг от сосуда, расположенного над установкой. Электролит стекает затем в емкость, находящуюся под деталью.
К недостаткам этой установки относят перегрев и испарение электролита в тампоне, возникновение загазованности и быстрое изнашивание тампона, что снижает производительность процесса и качество покрытий. для их устранения заменяют скольжение анодного тампона по детали его качением (рис. 3.46). За счет большей площади контакта анодного устройства с деталью увеличиваются допустимая плотность тока и производительность процесса. Благодаря такому устройству значительно улучшается равномерность распределения тока по окружности катода по сравнению с обычным тампоном трения скольжения. Поэтому предложено режим электролиза характеризовать средней плотностью тока, равной отношению силы проходящего тока ко всей площади покрываемой поверхности, а не к площади контакта.
Пути совершенствования технологии гальванических покрытий. Наряду с изложенными ранее достоинствами гальванические способы имеют и существенные недостатки, что ограничивает их применение. К главным из них относят:
сложность и недостаточная надежность технологического процесса, приводяшие к снижению производительности труда и нестабильным результатам по сцепляемости покрытий с деталями;
при потреблении большого количества чистой воды и образовании такого же количества загрязненных стоков значительно повышаются себестоимость восстановления, что приводит к строительству очистных сооружений, которые по стоимости и занимаемой площади сопоставимы с такими же показателями самого гальванического цеха;
сравнительно низкая производительность обусловлена многооперационностью процесса и недостаточной скоростью осаждения металлов;
качество покрытий не всегда соответствует предъявляемым требованиям.
Сложились два основных направления развития технологии гальванических покрытий.
Первое н а п р а в л е н и е повышение производительности процесса. Прежде всего этого можно достичь за счет увеличения скорости осаждения покрытий, которую определяют из формулы (3.38), поделив обе части равенства на :
![]()
Поскольку С и ‚ для каждого металла постоянные, то скорость осаждения можно повысить увеличением либо iч, либо д либо одновременно т и д. Повышение скорости осаждения покрытий за счет увеличения выхода метала по току важнейшее направление работ по совершенствованию хромирования с низким значением выхода по току. для железнения и других процессов последний составляет 85 % и более, и за счет его дальнейшего увеличения скорость осаждения покрытий существенно повысить нельзя. Поэтому для повышения производительности процессов необходимо увеличивать плотность тока.
Чтобы улучшить процесс нанесения покрытий с высокими качествоми и производительностью, следует совершенствовать и разрабатывать новые электролиты и технологические приемы.
Разработка НОВЫХ ЭЛЕКТРОЛИТОВ для одних процессов (хромирование) приводит к увеличению плотности тока и выхода хрома по току и тем самым росту производительности процесса, а для других — это основной путь повышения качества покрытий.
Например, при использовании саморегулирующихся электролитов хромирования (см. табл. 3 17) можно увеличить выход по току до 35.. .40 % и плотность тока до 100.. .300 А/дм2, в результате чего производительность процесса возрастает в 10 раз и более по сравнению с хромированием в универсальном электролите.
Чтобы повысить износостойкость и улучшить другие свойства покрытий, следует наносить на детали различные сплавы металлов. Например, сплав железо — фосфор с содержанием фосфора до 7...10 % можно получить из электролита 1 (см. табл. 3.16) при введении в него 10...20 г/л гипофосфита натрия. В исходном состоянии его микротвердость 7000.. .8000 МПа. Термообработка покрытий из сплава Ге—Р при температуре 350. .400 °С в течение 1 ч способствует образованию фосфидов железа (Ее Р) и увеличению микротвердости до 15 000... 160 000 МПа. Их износостой кость более чем в 2 раза превышает износостойкость закаленной стали 45 и не уступает износостойкости хромовых покрытий.
При восстановлении деталей, работающих в тяжелых коррозиОННыХ условиях, применяют железоникелевые покрытия. для их получения в электролит железнения добавляют 20. ..30 г/Л хлорида никеля.
К перспективным относят композиционные электрохимические покрытия (КЭП), образованные введением в электролиты мелкодисперсных порошков полимеров, оксидов металлов (А1203 и др.) и т.д. Например, в электролит железнения I 1 (см. табл. 3.16) вводят 40.. .50 г/л порошка поливиниЛХЛорида или 30...40 Г/Л полиамида. Износостойкость таких покрытий при трении скольжения в 2... 3 раза выше износостойкости обычных железных покрытий.
Разработка новых технологическ приемов приводит к увеличению производительности процесса за счет уменьшения и ощелачивания прикатодного слоя электролита. К таким приемам относят проточное, струйное, электроконтактное осаждение перемешивание электролита применение периодических токов (нестационарный электролиз) и др.
Предложено создавать турбулентное движение электролита у поверхности катода за счет введения в межэлектродное пространство вращающейся пластмассовой перфорированной перегородки. При вращении последней со скоростью 2.. .3 м/с катодная плотность тока в процессе железнения достигает 150...200 А/дм2, а скорость осаждения покрытий — 1,5. ..2 ММ/ч. Кроме того, за счет вращающейся перегородки уменьшаются деидритообразование и шероховатость покрытий, улучшается их равномерность.
При гальваномеханическом способе осаждения покрытий можно резко повысить производительность. Его отличительная особенность состоит в том, что при электролизе по покрываемой поверхности постоянно перемещается инструмент в виде абразивных брусков. Происходит незначительный съем уже осажденного металла, но в результате активирования покрываемой поверхности и перемешивания электролита плотность тока, например, при хромировании может быть увеличена до 1000 А/дм2, а скорость осаждения покрытий — в 20. ..50 раз и достигать 3,6 мм/ч. Важно, что выход хрома потоку достигает 50...55 %.
При использовании периодических токов (реверсивного, асимметричного, импульсного и др.) вместо постоянного в несколько раз повышается производительность процесса и улучшаются свойства покрытий. Сущность способа заключается в том, что ток, изменяясь по определенному закону, периодически меняет свое направление. деталь попеременно становится то катодом, то анодом, а катодное осаждение металла на детали периодически прекращается и заменяется его кратковременным частичным растворением. Вместе с последним разрушается образовавшаяся пассивная пленка, а прикатодный слой электролита обогащастся катионами металла.
Наиболее простая форма периодического тока — реверсивный ток, получаемый изменением направления ПОСТОЯННОГО. Например, хромировать на реверсивном токе можно в универсальном Электролите при температуре 50... 60 °С, плотности ПРЯМОГО И обратного токов 60... 140 А/дм2, времени прохождения ПРЯМОГО Тока 1... 5 мин и обратного — 1.. .5 С.
При ХОЛОДНОМ железнении оптимальными считают = 20... ЗО А/дм2 и 36...10. Кислот- ность электролита рИ 0,5.. .0,9, температура не регламентируТся. Процесс характеризуется повышенным детндритообразованием, особенно в случае применения тиристорного источника тока. Чтобы его уменьшить, необходимо начинать железнение на асимметричном переменном токе, обеспечивающем повышенную сцепляемость покрытий при холодном электролите, а затем переходить на постоянный ток.
В технологию восстановления деталей гальваническвми покрытиями входят электрохимическое обезжиривание и химическая нейтрализация в щелочных растворах. При этом используют вредные для здоровья химикаты, затрачивают значительное время (20... 30 мин), расходуют большое количество чистой воды, которую затем необходимо очищать.
Разработан способ механизированного обезжиривания деталей венской известью и последующей промывки с замкнутым циклом водоиспользования, а также безреагентной нейтрализации деталей после железнения с одновременной промывкой в установке для разделения воды с помощью электрического тока на кислую и шелочную. В последнем случае также обеспечивается замкнутый цикл водоиспользования.
Таким образом, в перспективе возможно создание малооперационной безотходной технологии железнения с замкнутым циклом водоиспользования.
Техника безопасности. К работе в гальванических цехах и отделениях допускаются лица в возрасте не моложе 18 лет, прошедшие медицинский осмотр, специальное обучение и инструктаж по технике безопасности.
Рабочих гальванических цехов обеспечивают спецодеждой: резиновыми сапогами, перчатками, прорезиненньими фартуками, халатами и очками. В обеденньтй перерыв и после окончания рабочего дня спецодежду нужно хранить в шкафу. Запрещается уносить ее домой. Кроме того, нельзя хранить пищевые продукты, принимать пищу и курить в рабочем помещении, засасывать растворы ртом через шланги или стеклянные трубки, ремонтировать оборудование при включенной силовой сети, допускать посторонних лиц на рабочие места. Приточно-вытяжная вентиляция должна быть исправной. Ее разрешается включать не позже чем за 15 мин до начала работы, а выключать не раньше чем через 15 мин после окончания смены.
Приготовлять, корректировать и фильтровать электролиты нужно при включенной вентиляции. При разбавлении кислот надо обязательно лить кислоту вводу, а не наоборот.
При попадании кислоты, щелочи или электролита на открытые участки тела или в глаза пораженные места необходимо немедленно обмьтть струей воды, затем пораженные кислотой или кислым электролитом места следует промыть 2.. .3%-м раствором питьевой соды, а пораженные щелочью — 1%-м раствором уксусной кислоты и снова промыть водой.
Мероприятия по охране окружающей среды. Перед спуском в канализацию загрязненньте сточные воды необходимо обезвредить. К наиболее сильным ядам относят ионы цианида и шестивалентного хрома, а также опасны в больших количествах ионы тяжелых металлов (меди, цинка, железа, кадмия и др.).
Сточные воды перед спуском в канализацию должны иметь рИ 7,5...8,5, т.е. четко выраженную щелочную реакцию. Для очистки сточньтх вод при меняют химический, биохимический, ионообменный и другие методы. Наиболее прост химический метод, заключающийся в обезвреживании ядовитьгх вредных веществ добавлением в сточную воду химических реактивов.
Хромсодержащие сточные воды очищают в два этапа: сначала восстанавливают в кислой среде шестивалентный хром до трехвалентного (i этап), а затем добавлением щелочи до рН 8,0.. .8,5 трехвалентный хром и другие металлы переводят в малорастворимЫие гидроксиды, выпадающие в осадок (i1 этап). На первом этапе в сточные воды добавляют сульфат железа, сульфит или пи росульфит натрия, сернистый газ или сернистую кислоту при рН 2,0.. .2,5. На одну часть (по массе) шестивадентного хрома требуется добавить 7,0...7,5 части восстановителя.
Кислые с т о ч н ы е воды без примесей металлов, а также содержащие соединения тяжелых металлов и трехвалентного хрома, очищаютдобавлением щелочи (известковое молоко, известняк, едкий натр) до рН 7,5.8,5. При этом полностью нейтрализуются свободные кислоты, а тяжелые металлы в виде гидрооксидов выпадают в осадок при последующем отстое. Затем очИщеннуIО воду спускают в канализацию, а осадок фекальнъIМ насосом удаляют из отстойников на иловые площади для обезвоживания.
3.8. ВОССТАНОВЛЕНИЕ ДЕТАЛЕЙ ХИМИКОТЕРМИЧЕСКОЙ ОБРАБОТКОЙ
В процессе химикотермической обработки сталей, при цементании, борировании, азотировании, нитроцементации на их поверхности образуется диффузионный слой с повышенной концентрацией насыщающего элемента (С, В, ) определенного фазового состава и микроструктуры. Одновременно изменяются линейные размеры (до 5...10 % толщины) деталей — увеличивается диаметр валов, уменьшается диаметр отверстий. Восстанавливают детали с небольшими износами.
Диффузионная металлизация — разновидность химико-термической обработки сталей, заключающаяся в насыщении поверхностных слоев изделия различными металлами. Слои насыщаются одновременно или последовательно несколькими элементами. Такое насыщение называют комплексным. В качестве насыщающих элементов применяют хром, титан, вольфрам, никель и другие металлы 1у...уI11 подгрупп периодической системы элементов д. И. Менделеева.
При комплексном насыщении сталей металлами в сочетании с одниМ из таких элементов, как С, В, 14 или i, образуются карбидные, боридные, нитридные или лицидНые покрытия с уникальными физико-механическими, теплофизическими, кристаллохимическими и другими свойствами. С помощью диффузионной меттализацИи достигают большего изменения линейных размеров деталей, чем при химико-термической обработке традиционных видов.
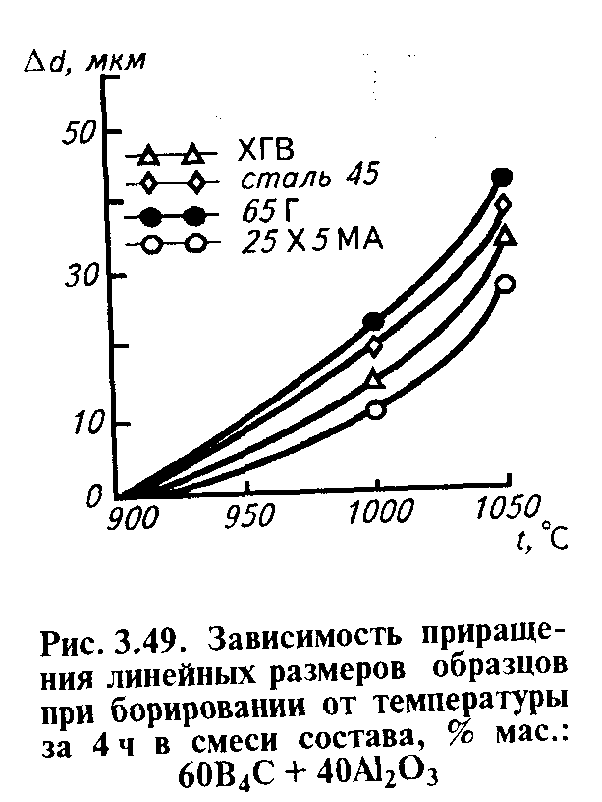
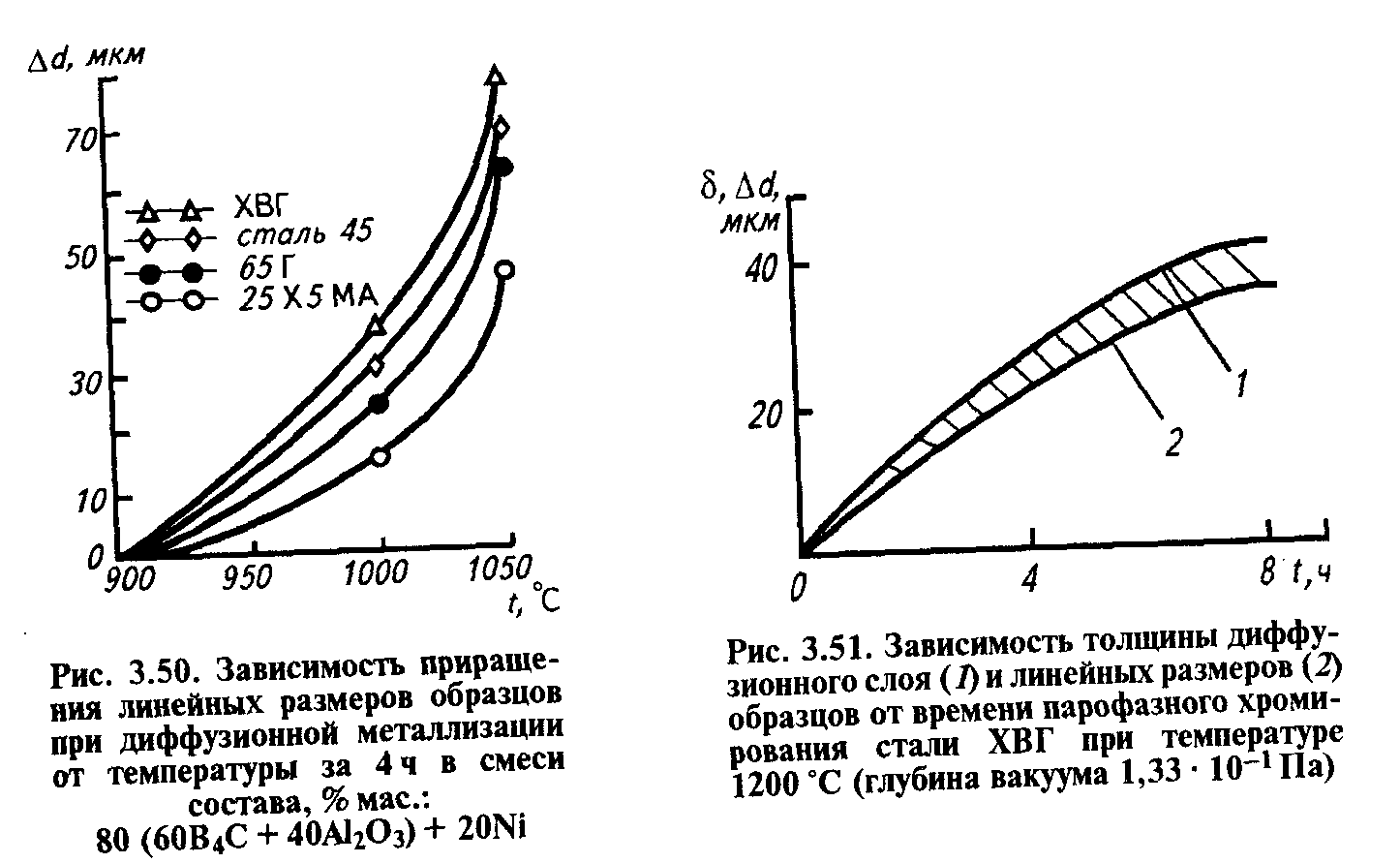
На рисунке 3.49 показано, как изменяются размеры круглых образцов (валов) диаметром 9 мм в зависимости от температуры борирования сталей в порошковой смеси состава, % мас.: 6ОВ4С+ +40А1203 в течение 4 ч (В4С — карбид бора, А1203 — оксид алюминия). При комплексном насыщении тех же сталей бором и никелем из смеси состава, % мас.: 80 (б0В4С+40А12О3)+20i приращение линейных размеров увеличивается в 1,5.. .2 раза (рис. 3.50).
Изменение линейных размеров деталей обычно рассматривают как сумму двух составляющих:
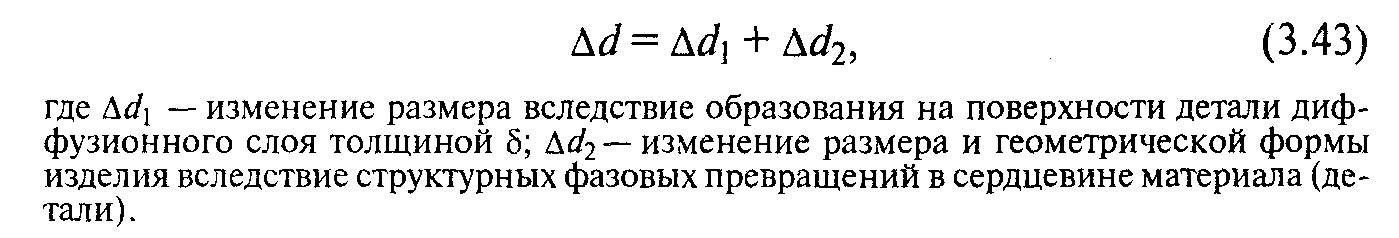
Величина Ай’2 зависит от химического состава стали, вида предварительной термической обработки, скорости нагрева и охлаждения контейнера в процессе диффузионной металлизации, вида и режимов термической обработки после насыщения, исходной формы и геометрических размеров деталей.
Если восстанавливаемые детали были подвергнуты предварительной термической обработке, а после насыщения охлаждались с малой скоростью, то значением Ай2 можно пренебречь.
Толщина диффузионного слоя и связанное с этим изменение размеров деталей зависят от таких факторов, как вид получаемого покрытия, режимы и способы насыщения, свойства насыщаемого металла, и с достаточной степенью точности могут быть определены лишь в результате эксперимента.
Для карбидных покрытий значение Ай находится в пределах (0,85..0,9). Для них характерны небольшие толщины диффузионного слоя. Для комплексных боридных покрытий значение Ай составляет (0,15.. .0,б) и зависит от режимов насыщения (температуры и времени).
На рисунке 3.51 показана зависимость толщины диффузионного слоя и линейных размеров деталей Ай после парофазного хромирования в вакууме от длительности процесса насыщения при постоянной температуре, равной 1200 ос.
Существуют методы диффузионного насыщения из твердой (твердофазный), жидкой (жидкофазный), газовой (газофазный) и паровой (парофазный) фаз. В основу такого деления положена характеристика активной фазы (или среды), содержащей диффундирующий элемент. Наибольшее распространение в производстве нашли газофазный и парофазный методы.
Газофазный метод заключается в насыщении поверхности материала изделия диффундирующим элементом, который входит в состав газа как химического соединения.
В атомарном виде насыщающий элемент образуется в результате химических реакций, происходящих либо в объеме реакциош{ого пространства, либо на поверхности изделия. В качестве активного газа чаще всего применяют галогениды аСыщающИХ элементов, например при хромировании СтСI2, СгГ2, Сг12 и др.
При газовом методе применяют контактный или неконтактный способ. При контактном способе газовая фаза генерируется в непосредственной близости от насыщаемой поверхности, из порошка вещества, содержащего диффундирующиЙ элемент. Например, для хромировання сталей используют порошки хрома или малоуглеродистого феррохрома. Галлоидные газы (Н1, НР, ИЗ, НВг и др.) получают в результате добавления в порошок аммонийной соли (То4Н4СI, ЫН4Р, 14Н4 и др.). При неконтактном способе газовая фаза (галогенид хрома) генерируется на некотором расстоянии от изделия.
Парофазный метод насыщения выполняют контактным и неконтактным способами. При контактном способе частицы (порошок) насыщающего элемента находятся в непосредственном контакте с изделием. При нагреве реакционного пространства упругость паров насьгщающего элемента выше, чем при неконтактном способе, когда частицы асыщающего вещества находятся на некотором расстоянии от обрабатываемой поверхности. При неконтактном способе образуется более качественное покрытие, хотя глубина насыщения меньше.
Большое распространение получило хромирование сталей из паровой фазы в вакууме. При этом облегчаются испарение и перенос хрома к обрабатываемой поверхности. Парофазный метод предотвращает окисление детали, способствует понижению температуры испарения хрома, повышению упругости его паров в реакционном пространстве, что интенсифицирует процесс хромирования.
Контактный способ парофазного или газофазного метода диффузионного насыщения наиболее прост, не требует специального оборудования, обеспечивает достаточно высокое качество покрытий и легко осуществим в производственных условиях.
Основные технологические операции газового способа (например, хромиронания): подготовка насыщающей смеси и изделий; упаковка изделий в контейнер; нагрев контейнера; извлечение контейнера из печи; охлаждение контейнера и его распаковка; очистка поверхности обработанных изделий. Насыщающую смесь готовят из следующих порошков: вещества, содержащего диффундирующийэлемент; инертной добавки, предотвращающей спекание частиц активной составляющей с поверхностью детали и контейнера; активатора, в качестве которого используют аммонийные соли. Инертными добавками служат оксид алюмияия (глинозем), речной песок и шамот.
Все компоненты смеси перед смешиванием просушивают для удаления влаги или прокаливают (глинозем). Их хранят в чистой, плотно закрывающейся таре в сухом месте. Состав смеси может быть различным. Его выбирают исходя из имеющихся рекомендаций. Например, для хромирования углеродистых сталей может быть применена смесь состава, % мас.: хром Х97 — 70, глинозем (А1203) — 27 и хлорид аммония (Н4С1) — 3.
При парофазном хромировании в вакууме контейнер не герметизируют. Его изготавливают из обычной углеродистой стали. Засыпают в контейнер не смесь, а гранулированный хром с размером частиц О,3...0,5 мм.
Для нагрева контейнеров с плавким затвором применяют нагревательные печи сопротивления с окислителъной атмосферой, обесечивающие рабочую температуру в интервале 950... 1200 ос, например печи СНО-4.8.5/13-И1. Контейнеры без плавкого затвора при парофазном методе насыщения нагревают в вакуумных печах СШВ-0,6.2/16-112, СНВЭ-1.3.1/16-ИЗ в зависимости от размера обрабатываемых изделий.
Другие технологические операции диффузионной металлизации по своему содержанию аналогичны процессу цементации сталей.
Диффузионной металлизации подвергают детали из сплавов на основе меди (бронзы, латуни). Широкое распространение нашел способ насыщения поверхности изделий цинком. В этом случае детали укладывают в контейнер и засыпают порошком следующего состава (в массовых частях) порошок цинка — 100, глина огиеугiорная (или оксид алюминия АI2О3) —28 и хлорид аммония 1Н4С1 —7. Цинковьтй порошок просеивают сквозь сито с 650 отверстиями на 1 см2. Перед употреблением инертные добавки просушивают. Детали (например, втулки верхней головки шатуна) упаковывают в контейнер, куда засыпают приготовленную насыщающую смесь.
