
- •Методы проведения полимеризации
- •Полимеризация в массе мономера
- •Полимеризация в растворителе
- •Полимеризация в суспензии
- •Эмульсионная полимеризация
- •Радикальная сополимеризация Характеристика процесса
- •Уравнение состава сополимера
- •Константы сополимеризации, их физический смысл
- •Ионная полимеризация
- •Активные центры ионной полимеризации
- •Катионная полимеризация
- •Инициаторы катионной полимеризации
- •Реакционная способность мономеров
- •Механизм катионной полимеризации
- •Анионная полимеризация
- •Механизм действия анионных инициаторов. В зависимости от типа взаимодействий можно выделить 2 механизма инициирования анионной поликонденсации.
Радикальная сополимеризация Характеристика процесса
Сополимеризация – процесс совместной полимеризации двух или более типов мономеров. Получаемые при этом высокомолекулярные соединения называются сополимерами. Чаще всего для получения сополимеров используют два типа мономеров. В этом случае сополимеризация называется бинарной. Сополимеризация трех мономеров называется терполимеризацией.
В общем виде уравнение бинарной сополимеризации можно записать:
nA + mB → ~A-B-A-A-B-B-B~
где A, B – мономеры типа А и В; n, m – число мономеров соответствующих типов.
Сополимеризацию, как и гомополимеризацию, можно проводить различными способами (в массе, эмульсии, суспензии и растворе).
Причины большого практического значения реакций сополимерзации:
сополимеры часто обладают более ценными техническими свойствами, чем полимеры, образованные одним мономером;
свойства сополимеров сильно зависят от их состава и строения, что дает возможность их широкого варьирования;
изучая сополимеризацию, можно получать точные сведения о реакционной способности мономеров (в отличие от гомополимеризации).
Примеры: сополимер акрилонитрила и винилхлорида, в отличие от гомополимера акрилонитрила, растворим в ацетоне; сополимер акрилонитрила и винилпиридина может окрашиваться; сополимер акрилонитрила и бутадиена приобретает масло- и бензостойкость.
Как и гомополимеризация, сополимеризация проходит в три стадии: инициирование, рост цепи и обрыв цепи, где также возможны различные реакции передачи цепи. При этом все стадии осложнены присутствием в реакционной смеси нескольких типов мономеров, вероятность взаимодействия между которыми определяется соотношением их активностей.
Главный вопрос, возникающий при изучении сополимеризации, – зависимость состава образующегося сополимера от состава смеси мономеров и условий проведения процесса. Решение этого вопроса возможно с помощью анализа уравнения состава сополимера.
Уравнение состава сополимера
Механизм бинарной сополимеризации
Инициирование. Взаимодействие свободных радикалов, образующихся при разложении инициатора, с мономерами обоих типов приводит к образованию активных центров двух различных типов:


Рост
цепи.
Протекает путем последовательного
присоединения молекул мономеров А
и В
к активным центрам
 и
и
 .
В результате генерируются активные
частицы четырех различных типов:
.
В результате генерируются активные
частицы четырех различных типов:
 ,
,
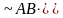 ,
,
 ,
,
 .
.
В бинарной сополимеризации скорость присоединения мономера к растущей цепи зависит только от природы мономера, так как реакционная способность макрорадикала не зависит от его длины и от природы мономерных звеньев, связанных со звеном, на котором расположен радикал.
Таким образом, возможны четыре способа присоединения мономера и, соответственно, четыре скорости:
реакция скорость
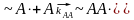



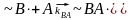
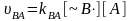


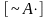 ,
,
 – концентрации макрорадикалов;
– концентрации макрорадикалов;
 ,
,
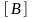 – концентрации мономеров;
– концентрации мономеров;
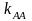 ,
,
 ,
,
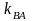 ,
,
 – константы скорости роста цепи, в
которых первая буква индекса соответствует
типу активной частицы, а вторая – типу
мономера;
– константы скорости роста цепи, в
которых первая буква индекса соответствует
типу активной частицы, а вторая – типу
мономера;
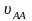 ,
,
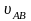 ,
,
 ,
,
 – соответствующие скорости реакций
роста цепи, причем
и
соответствуют скоростям роста цепи при
гомополиконденсации соответствующих
мономеров, а
и
– скорости так называемого «перекрестного»
роста цепи.
– соответствующие скорости реакций
роста цепи, причем
и
соответствуют скоростям роста цепи при
гомополиконденсации соответствующих
мономеров, а
и
– скорости так называемого «перекрестного»
роста цепи.
Реакционная способность мономеров rA и rB определяется отношением константы скорости радикального присоединения данного мономера к мономеру той же природы к константе скорости присоединения данного мономера к мономеру другой природы:
 ;
;
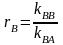 ,
,
rA и rB называются константами сополимеризации.
Случай,
когда
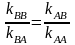 ,
т.е.
,
т.е.
 ,
или
,
или
 ,
называется идеальной
сополимеризацией.
,
называется идеальной
сополимеризацией.
Идеальная сополимеризация – сополимеризация, при которой макрорадикалы обладают одинаковой способностью присоединять оба мономера. Наиболее характерна для ионной полимеризации. При идеальной сополимеризации образуются статистические сополимеры.
Случай,
когда
 ,
называется чередующейся
(альтернантной) сополимеризацией.
,
называется чередующейся
(альтернантной) сополимеризацией.
В
предельном случае, когда
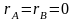 ,
наступает истинное чередование звеньев.
,
наступает истинное чередование звеньев.
На
практике большинство сополимеризующихся
систем занимает промежуточное положение
между предельными случаями чередующейся
(
)
и идеальной (
)
сополимеризации:
 ,
при этом образуется широкий спектр
статистических
сополимеров.
При стремлении произведения
,
при этом образуется широкий спектр
статистических
сополимеров.
При стремлении произведения
 к 0 возрастает стремление к чередованию
и наоборот, чем ближе произведение
к 1, тем выше тенденция к идеальной
сополимеризации.
к 0 возрастает стремление к чередованию
и наоборот, чем ближе произведение
к 1, тем выше тенденция к идеальной
сополимеризации.
Случай,
когда
 ,
соответствует блочной
сополимеризации.
Не характерен для радикальной
сополимеризации.
,
соответствует блочной
сополимеризации.
Не характерен для радикальной
сополимеризации.
Константы сополимеризации:
не зависят от особенностей стадий инициирования и обрыва;
не зависят от характера реакционной среды (в том числе от ее полярности);
мало зависят от температуры, т.к. энергии активации реакций роста и различия между этими энергиями малы;
уменьшаются
при повышении давления в случае
радикальной сополимеризации (уменьшается
селективность процесса, он сдвигается
в сторону идеальной сополимеризации
( ).
).
Важное
значение имеют величины, обратные
константам сополимеризации,
 и
и
 –
относительные
активности мономеров.
Они определяют отношение констант
скоростей реакций взаимодействия
радикала с другим мономером и с
собственным:
–
относительные
активности мономеров.
Они определяют отношение констант
скоростей реакций взаимодействия
радикала с другим мономером и с
собственным:
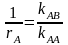 ;
;
 .
.
Это позволяет сравнить активность мономеров по отношению к одному и тому же радикалу.
Из таблицы видно, что к стирольному радикалу все мономеры присоединяются с низкой скоростью, а к винилацетатному – с высокой. С другой стороны, относительная активность винилацетата по отношению ко всем радикалам низка, а стирола – высока. Винилацетат и стирол, резко отличающиеся по активности, практически не сополимеризуются по радикальному механизму.
Таким образом, знание величин и позволяет предсказать ход процесса сополимеризации и состав сополимера.
Относительная активность мономеров при реакции с различными макрорадикалами
Мономер |
Относительная активность мономера к макрорадикалу |
||||
стирола |
метилметакрилата |
акрилонитрила |
винилхлорида |
винилацетата |
|
Стирол |
- |
2,2 |
25 |
50 |
100 |
Метилметакрилат |
1,9 |
- |
6,7 |
10 |
67 |
Акрилонитрил |
2,5 |
0,82 |
- |
25 |
20 |
Винилхлорид |
0,059 |
0,1 |
0,37 |
- |
4,4 |
Винилацетат |
0,019 |
0,05 |
0,24 |
0,59 |
- |
Вывод уравнения состава сополимера
Изменение
концентраций мономеров
 и
и
 в процессе роста цепи при сополимеризации
определяется следующими уравнениями:
в процессе роста цепи при сополимеризации
определяется следующими уравнениями:
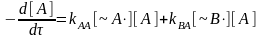 ;
;
 .
.
Разделим эти уравнения одно на другое и получим:
 .
.
Поскольку во время роста цепи осуществляются многократные переходы в и в , быстро устанавливается стационарное состояние, основным условием которого является равенство
 .
.
Из уравнения выразим стационарные условия для :
 .
.
С помощью последнего выражения можно исключить неизвестные значения концентрации макрорадикалов и . После ряда математических преобразований получим

Поскольку
 и
и
 – количества мономеров А
и В,
вступивших в сополимеризацию в данный
момент времени
– количества мономеров А
и В,
вступивших в сополимеризацию в данный
момент времени
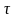 ,
можно считать, что отношение этих величин
характеризует некий «мгновенный» состав
сополимера, т.е. дифференциальный состав
бесконечно малого количества сополимера.
Если обозначить символами a
и b
содержание мономерных звеньев первого
и второго типов в сополимере соответственно,
то уравнение можно переписать в виде
,
можно считать, что отношение этих величин
характеризует некий «мгновенный» состав
сополимера, т.е. дифференциальный состав
бесконечно малого количества сополимера.
Если обозначить символами a
и b
содержание мономерных звеньев первого
и второго типов в сополимере соответственно,
то уравнение можно переписать в виде
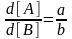
Тогда, подставив в уравнение выражения из формул, получим
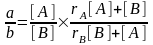
– это уравнение состава сополимера. Оно было выведено в 50-е годы в нескольких странах почти одновременно Майо и Льюисом, Алфреем и Гольдфингером, Сакурадой, Уоллом. Уравнение справедливо только для состава сополимера, полученного в начальной стадии сополимеризации, когда выполняется условие стационарности.
