
- •Хроматографические методы анализа
- •Детектор по электронному захвату (дэз-детектор)
- •Фазы в газовой хроматографии
- •Капиллярная хроматография
- •6) Интересно, что все металлы можно перевести в летучие соединения с помощью органических реагентов:
- •Высокоэффективная жидкостная хроматография
- •Сподвиж.
- •Ионная хроматография
- •Эксклюзивная хроматография
Сподвиж.
т.е. отношение концентраций в
неподвижной и в подвижной фазе должно
быть близко к единице. Обычно считается
удовлетворительным, если Рi
находится в диапазоне от 0,1 до 10. На
практике очень трудно подобрать
индивидуальный растворитель, который
во всех случаях удовлетворял бы этим
требованиям. Чаще всего применяются
бинарные смеси растворителей: вода –
органический растворитель либо полярный
органический растворитель – неполярный
органический растворитель. Например,
нужно разделить гидрофобные органические
вещества. Если взять воду, то коэффициент
распределения будет очень высоким, т.е.
Р
![]() .
А если взять гексан, то, наоборот,
Р
0.
Поэтому для разделения этих веществ
берут смесь вода–метанол и подбирают
такое их соотношение, которое обеспечивает
нужный диапазон коэффициентов
распределения определяемых веществ в
анализируемой смеси. Если окажется,
что метанола недостаточно, и Рi
все равно высокие, то берут
другие растворители, например, пропанол
или изопропанол. Если и этот случай
не удовлетворяет, то берут полярный
органический растворитель и неполярный,
например пропанол – гексан.
.
А если взять гексан, то, наоборот,
Р
0.
Поэтому для разделения этих веществ
берут смесь вода–метанол и подбирают
такое их соотношение, которое обеспечивает
нужный диапазон коэффициентов
распределения определяемых веществ в
анализируемой смеси. Если окажется,
что метанола недостаточно, и Рi
все равно высокие, то берут
другие растворители, например, пропанол
или изопропанол. Если и этот случай
не удовлетворяет, то берут полярный
органический растворитель и неполярный,
например пропанол – гексан.
Разделительная способность жидкостных хроматографических колонок значительно выше, чем газовых. Если в газовых колонках число теоретических тарелок составляет 50, то в этих колонках около 50000, но ниже чем в капиллярных.
В заключении нужно отметить, что метод ВЭЖХ является уникальным в анализе лекарственных препаратов.
Ионная хроматография
Еще один вид хроматографии - это ионная хроматография. Ионная хроматография была открыта американским химиком Смолом в 1975 году, появление ее после ВЭЖХ было очевидным.
В основе ионной хроматографии лежат те же ионообменные материалы, что и в основе классической ионообменной хроматографии.
В ионной хроматографии сочетаются достоинства ВЭЖХ и классической ионообменной хроматографии. Ионообменные материалы, используемые в этом методе, отличаются не только малыми размерами зерен (20 микрон), но и тем, что ионообменные группы расположены не в глубине зерен, а на их поверхности, в районе 1 микрона. Эти материалы обладают малой обменной емкостью.
Давление, применяемое в этих системах, составляет 400 атм, обменная емкость ионита от 0.02 до 0.1 мг-экв /г, в 100 раз меньше, чем у обычного (2-10 мг-экв /г).
Главное достоинство ионной хроматографии – это уникальное детектирование по электропроводности. Именно детектирование по электропроводности (кондуктометрическое детектирование) и обеспечивает широкое распространение этого метода.
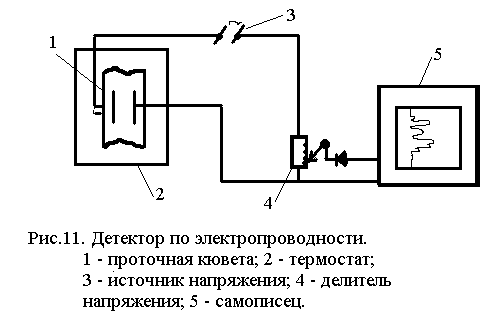
Размер кюветы гораздо меньше, чем она изображена на рисунке. Термостатирование применяется для того, чтобы обеспечить постоянство сигнала. Дело в том, что при изменении температуры удельная электропроводность растворов резко изменяется, она растет с ростом температуры, и наоборот.
Кроме этого детектора в ионной хроматографии может применяться и оптический детектор. Он применяется для окрашенных ионов, но в основном в одноколоночной хроматографии.
В ионной хроматографии используются ионообменные материалы – катиониты и аниониты, содержащие на своей поверхности ионогенные активные группы. Вы знаете, что в основе ионообменного материала лежит сополимер стирола и дивенилбензола. Если много стирола и мало дивенилбензола, то это малосшитый ионит. Если дивенилбензола 10%, то это сильносшитый ионит. Указанный процент показывает число межмолекулярных связей. Если стирол полимеризуется, то образуются длинные цепи, а если вкрапляются молекулы дивенилбензола, то образуются сшитые молекулы, и поэтому ионообменный материал не растворяется в воде.
Катиониты - это -SO3H, -COOH, первичные, вторичные, третичные, четвертичные аммониевые группы, либо первичные, вторичные, третичные аминные группы. Слабоосновной ионит содержит аминогруппы, слабокислый – -СООН группы.
В ионной хроматографии особое значение имеет оригинальный двухколоночный вариант. Этот вариант основан на помещении в цепь динамики элюата дополнительно к разделительной колонке еще и регенеративной колонки. Чтобы понять, зачем это нужно, будем рассуждать.
Допустим, что у нас анионная ионная хроматография, т.е. разделяемые вещества – анионы. Что будет использовано в качестве разделяемого ионообменного материала? Нужно разделить Cl- , Br - , I- . В этом случае используют аниониты. Для разделения катионов используют катиониты. Обычно берут хроматографическую колонку в ОН- - форме и вводят пробы (калиевые соли хлоридов, бромидов, иодидов). Нужен элюент, который бы заставлял двигаться хлориды вниз по колонке. Таким элюентом для анионной хроматографии является щелочь. На выходе из хроматографической колонки будем иметь элюент КОН, затем будут располагаться зоны KCl , KBr, KI. Чья электропроводность выше: КОН либо KCl? Электропроводность КОН в 2,5-3 раза больше за счет подвижности ОН- - ионов. Но надо учесть, что процесс идет на фоне избытка элюента. Если очень мало разделяемых веществ, то элюент остается нетронутым, т.е. мы должны анализировать KCl на фоне КОН. В таких условиях возникают трудности. Надо измерять разницу двух больших величин – электропроводности смеси КОН и KCl и электропроводности чистого КОН. Эту разность в условиях изменения температур стабилизировать трудно. Поэтому после разделительной колонки сразу ставят не детектор, а регенеративную колонку. Регенеративная колонка представляет собой для ионной хроматографии катионит в Н+ - форме. Что здесь происходит? Катион К+ в этом катионите меняется на катион водорода, КОН превращается в воду, KCl в НСl. Фон мы практически убрали, так как вода слабо диссоциирует, а полярный хлоридный сигнал усилили за счет того, что привязали к нему высокопроводящий ион водорода. В этом заключается главная «хитрость» ионной хроматографии. После разделительной колонки ставят детектор, который представляет собой обычную электролитическую проточную ячейку – трубка с двумя электродами. Между электродами прилагают переменное напряжение с частотой 1000 гц, так как при более низкой частоте окислительно-восстановительные процессы начинают мешать. При высокой же частоте проявляется электропроводность, обусловленная анализируемыми ионами. Далее сигнал, чаще всего с помощью ЭВМ, обрабатывается и выдается на самопишущем устройстве в виде хроматограммы.
Есть еще и катионная ионная хроматография. Что используется в качестве материала для разделительной колонки? Катионит в Н+- форме. Элюент – кислота. Регенеративная колонка – анионит в ОН- - форме. В результате будет получаться вода за счет замены аниона Cl- на ОН- и полезный сигнал в виде КОН. Ионная двухколоночная хроматография применима для катионов и анионов, не подвергающихся гидролизу. Анион СО3 2- определить этим методом невозможно, так как он превращается в СО2 . Подобным методом невозможно определить и уксусную кислоту, так как она плохо диссоциирует. Для катионов тяжелых металлов возникает другая проблема. При переводе их в гидроокиси они выпадают в осадок, и сигнал исчезает. Таким образом, этот метод применим только для сильных электролитов, не выпадающих в осадок. Это Cl, I, Br , сульфаты, фосфаты, перхлорат, из катионов - К+, Na+, NH4 + , Ca2+, Ba2+ , Cs2+ , Rb 2+.
Эту хроматографию используют для анализа важных объектов, одним из которых являются природные воды.
Сразу за разработкой ионной двухколоночной хроматографии появился еще один вариант - одноколоночная хроматография со специально подобранными элюентами. В одноколоночном варианте хроматографии разделительная колонка отсутствует. Разделенная смесь сразу детектируется. Для того, чтобы усилить полезный сигнал в одноколоночном варианте хроматографии в качестве элюентов используют вещества, обладающие низкой эквивалентной электропроводностью. В этом случае отмечается простая зависимость: чем больше молекулярная масса катиона и аниона в элюенте, тем ниже будет его удельная электропроводность. Понятно почему: при большой молекулярной массе сопротивление движению частицы за счет растворителя будет больше. Для этой цели выбирают соли сильных органических электролитов. Наиболее часто применяют тартрат метафенилендиаммония:
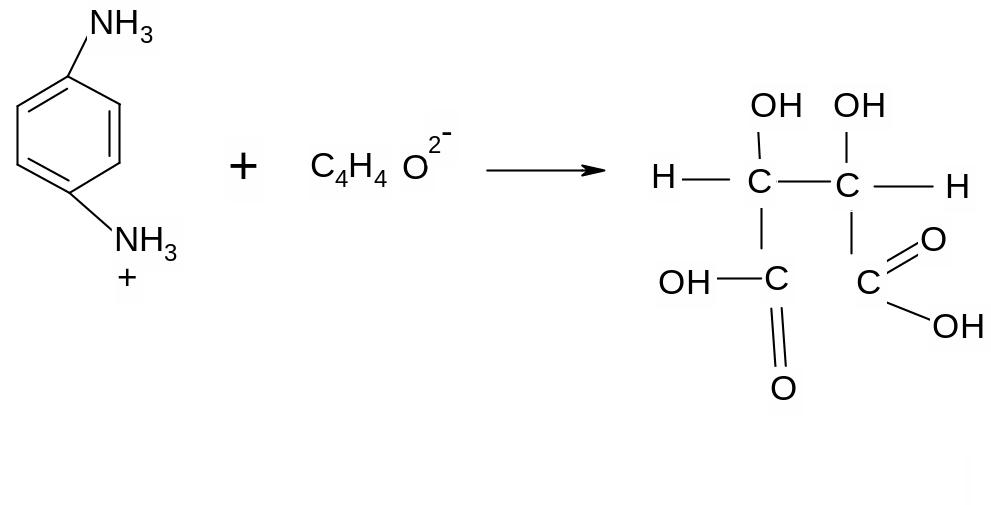
 Второй еще более часто применяемый
электролит -
оксиизобутиратэтилендиаммония:
Второй еще более часто применяемый
электролит -
оксиизобутиратэтилендиаммония:
Используют и другие элюенты, содержащие сульфогруппы, катионы четвертичных аммониевых оснований, но эти вещества на практике применяются редко.
Было предпринято много усилий, чтобы разработать неплохие условия определения веществ с помощью одноколоночной хроматографии. Этот метод получил некоторое распространение в определении тяжелых металлов.
Разберем еще два варианта хроматографии, встречающиеся реже, но имеющие значение в некоторых областях.
Ионпарная хроматография
В методе ионпарной хроматографии используются неподвижные фазы, которые чаще всего применяются для высокоэффективной жидкостной хроматографии. Это, как правило, твердый полимерный носитель либо неорганический носитель с привитой неподвижной фазой.
И![]() онпарная
хроматография применяется, когда
разделяемые вещества гидрофильны.
Это обычно электролиты, например,
алкилсульфаты либо четвертичные
аммониевые соли, соли металлов, т.е.
вещества, содержащие различные катионные
и анионные группировки. Такого рода
соединения не распределяются в неподвижную
фазу. Для этой цели используют реагенты,
которые образуют с разделяемыми
веществами ионные пары. Например,
это имеет место в золотопромышленности,
где надо разделить цианидные комплексы
серебра, меди, цинка, никеля, кобальта.
В качестве реагента используют
катион тетрабутиламмония, который в
водной фазе соединений с цианидными
комплексами металлов не образует.
Однако, на границе вода - неподвижная
фаза образуется ионный ассоциат, который
переходит в неподвижную фазу. Процесс
описывается константой экстракции
ионного ассоциата, которая строго в
согласии с законом действия масс равна
отношению равновесной концентрации
ионного ассоциата к произведению
концентраций ионов в водной фазе.
онпарная
хроматография применяется, когда
разделяемые вещества гидрофильны.
Это обычно электролиты, например,
алкилсульфаты либо четвертичные
аммониевые соли, соли металлов, т.е.
вещества, содержащие различные катионные
и анионные группировки. Такого рода
соединения не распределяются в неподвижную
фазу. Для этой цели используют реагенты,
которые образуют с разделяемыми
веществами ионные пары. Например,
это имеет место в золотопромышленности,
где надо разделить цианидные комплексы
серебра, меди, цинка, никеля, кобальта.
В качестве реагента используют
катион тетрабутиламмония, который в
водной фазе соединений с цианидными
комплексами металлов не образует.
Однако, на границе вода - неподвижная
фаза образуется ионный ассоциат, который
переходит в неподвижную фазу. Процесс
описывается константой экстракции
ионного ассоциата, которая строго в
согласии с законом действия масс равна
отношению равновесной концентрации
ионного ассоциата к произведению
концентраций ионов в водной фазе.


![]()
Например, медь: однозарядный анион Сu(CN)3- экстрагируется в виде ионного ассоциата в неподвижную фазу. Если ионные ассоциаты экстрагируются очень хорошо, то в качестве элюента используют воду либо раствор реагента с небольшой концентрацией.
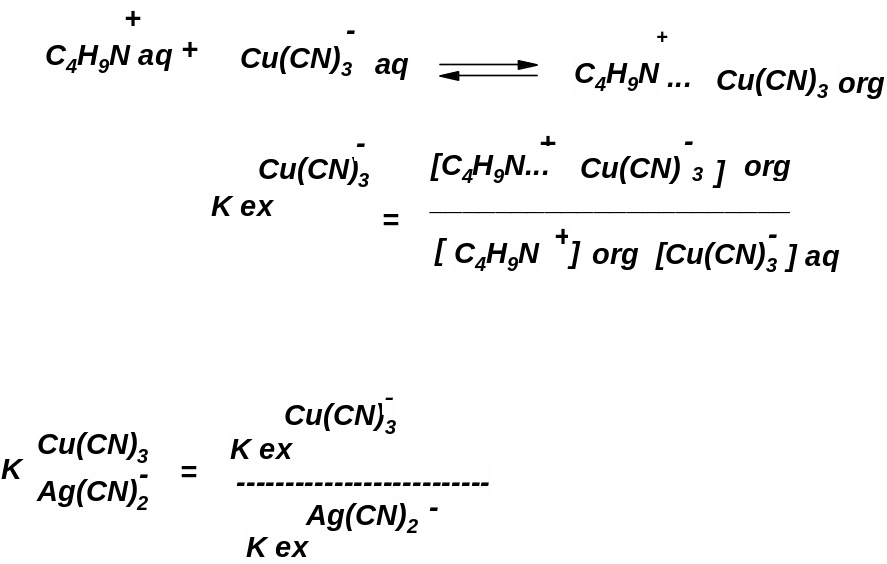
Детектирование осуществляют методом электропроводности либо оптическим методом, если разделяемые вещества поглощают излучение в какой-либо области. Иногда при работе с оптическим детектором в качестве реагента вводят оптическую метку – краситель.
Здесь приведены две хроматограммы, где в качестве реагента используют тетрабутиламмония хлорид, а разделяют замещенные бензойные кислоты. Поскольку бензойные кислоты оптически активны, их удобно разделять таким методом
