
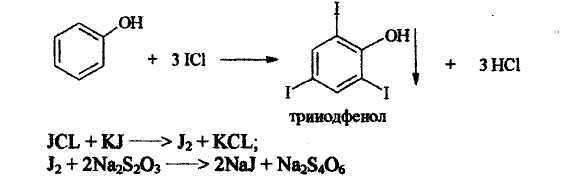
- •Ароматические соединения (арены) фенолы и их производные.
- •Фенол чистый.
- •Реакции по гидроксильной группе
- •Реакции по ароматическому ядру.
- •Резорцин.
- •Парацетамол.
- •Неостигмина метилсульфат (Прозерин).
- •Производные хинона.
- •Фитоменадион (Витамин к2)
- •Менадиона натрия бисульфит (Викасол). Синтетический витамин к.
Ароматические соединения (арены) фенолы и их производные.
Фенолы - производные ароматических углеводородов, которые содержат в молекуле одну или несколько гидроксильных групп, непосредственно связанных с ароматическим ядром.
По числу гидроксильных групп:
Одноатомные фенолы
Двуатомные
Трехатомные
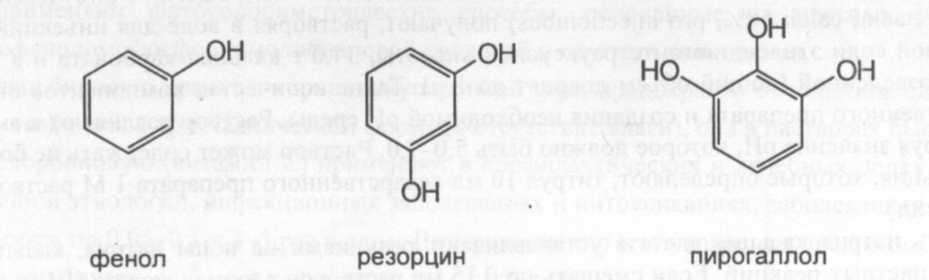
Получение:
Из природных источников
каменноугольная смола
смолы
эфирных масла некоторых растений
Синтетическим путем.
Тимол может быть также получен из м-крезола, который ацилируют, конденсируют с ацетоном и гидрируют:

Фенол и резорцин получают сульфированием бензола, например, получают бензолсульфокислоту и м-бензолдисульфокислоту:
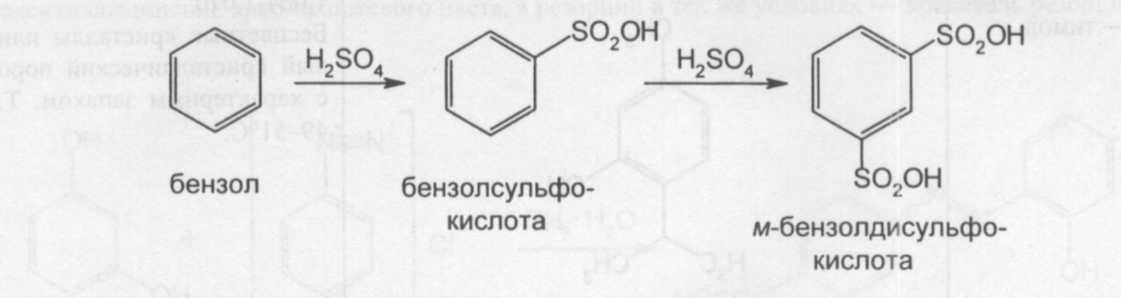
Далее сплавляют бензолсульфокислоту или м-бензолдисульфокислоту со щелочью и нейтрализуют кислотой, получают фенол или резорцин соответственно:
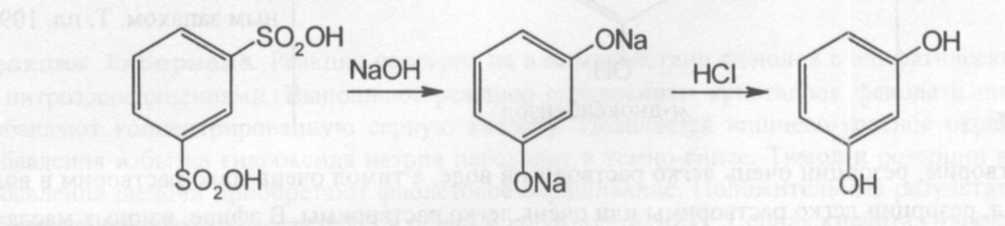
Современный промышленный метод синтеза одновременно фенола и ацетона основан на жидкофазном окислении изопропилбензола до гидропероксида изопропилбензола, который затем расщепляют серной кислотой:
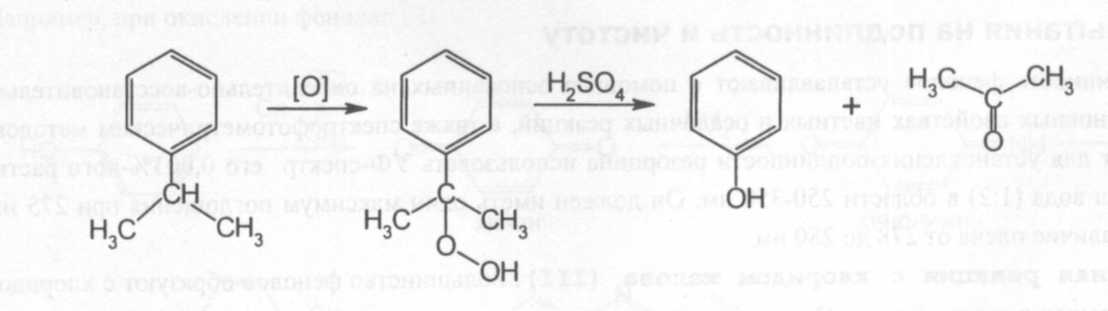
Также фенол получают диазотированием анилина с последующим разложением водных растворов солей диазония при кипячении:
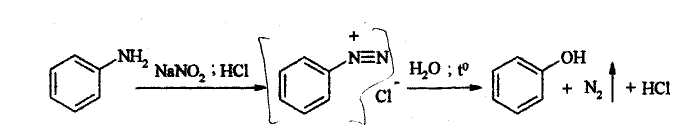
Химические свойства фенолов обусловлены:
Наличием гидроксильной группы с подвижным атомом водорода,
Ароматическими свойствами бензольного ядра.
Pbenoloin purum.
Фенол чистый.
Описание.
Бесцветные, тонкие, длинные игольчатые кристаллы или бесцветная кристаллическая масса своеобразного запаха. На воздухе постепенно розовеет. Ткип. - 178-182°С;
Растворимость.
Хорошо в воде, легко растворим в спирте, эфире, хлороформе, глицерине и жирных маслах, а также в растворах щелочей и растворе аммиака.
Подлинность.
Реакции по гидроксильной группе
При растворении в растворах гидроксидов щелочных металлов образуют феноляты (феноксиды):
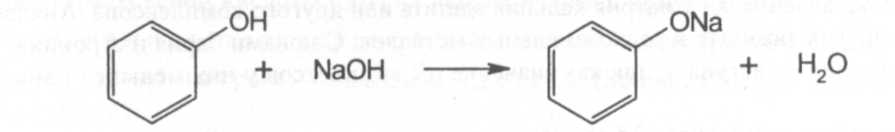
Взаимодействие с галогенпроизводиыми - образование простых эфиров.
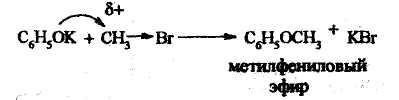
Ацилирование фенолов - образование сложных эфиров (при действии хлорангидридов или ангидридов карбоновых кислот).

Реакции по ароматическому ядру.
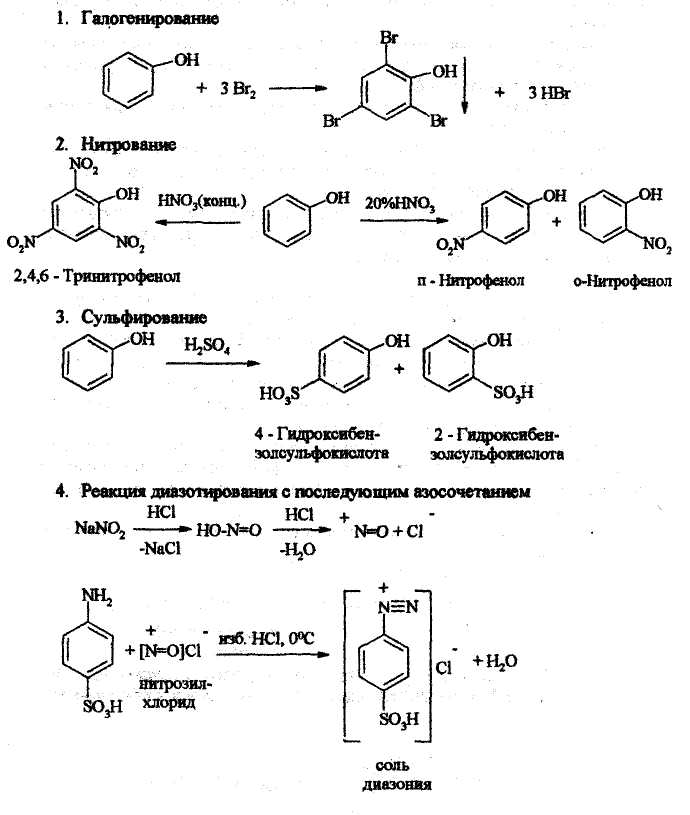
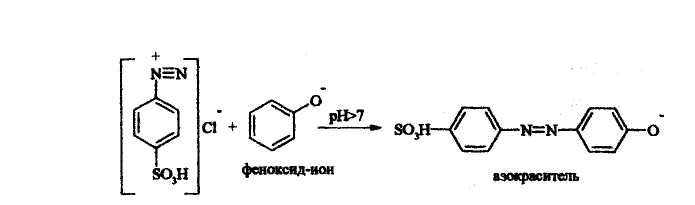
ярко-оранжевый цвет.
5. Реакция конденсации со спиртами, альдегидами, кислотами, ангидридами, хлорангидридами и др.
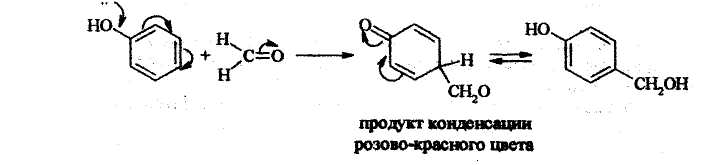
При стоянии раствор буреет вследствие дальнейшего процесса конденсации, приводящего к образованию многократно гидроксиметилированных продуктов:
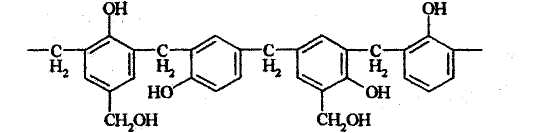
6. Индофеноловая реакция - фенол окисляют и действуют аммиаком:

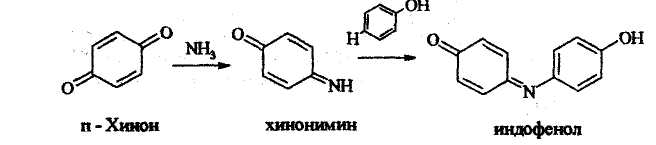
8. Для фенолов, у которых нет заместителей в о- и п- положениях, характерна реакция Либермана, конечным продуктом которой также является индофенол (реакция с ксантином).
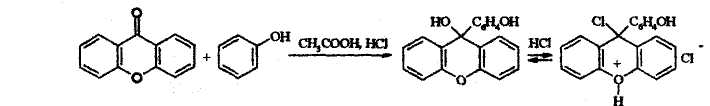
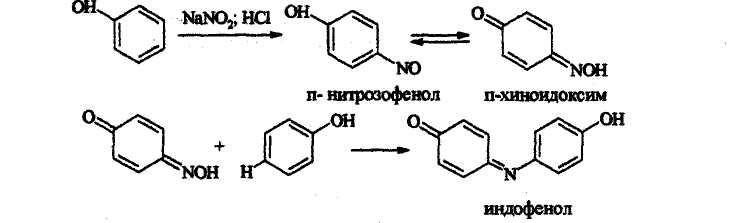
9. Образование антипириновых красителей.
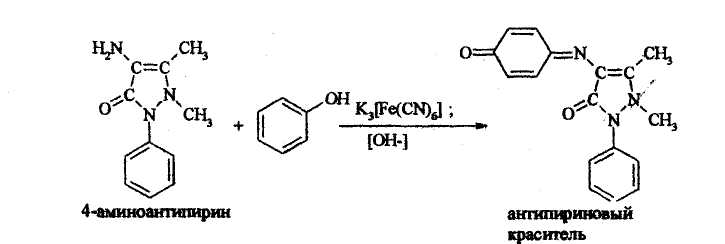
10. Образование фенолфталеина при конденсации с лактонами.
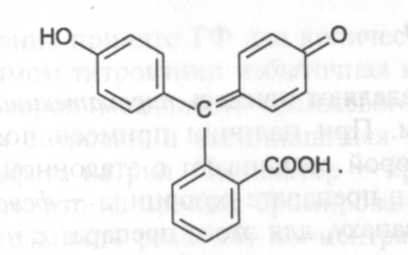
11. Получение ауриновых красителей при нагревании фенолов с хлороформом в присутствии гидроксида натрия.
Вначале фенолят с хлороформом образует дихлорметилфенолят, который гидролизуется в альдегид:

Полученный альдегид конденсируется с избытком фенолята, а затем превращается в ауриновый краситель желтого цвета
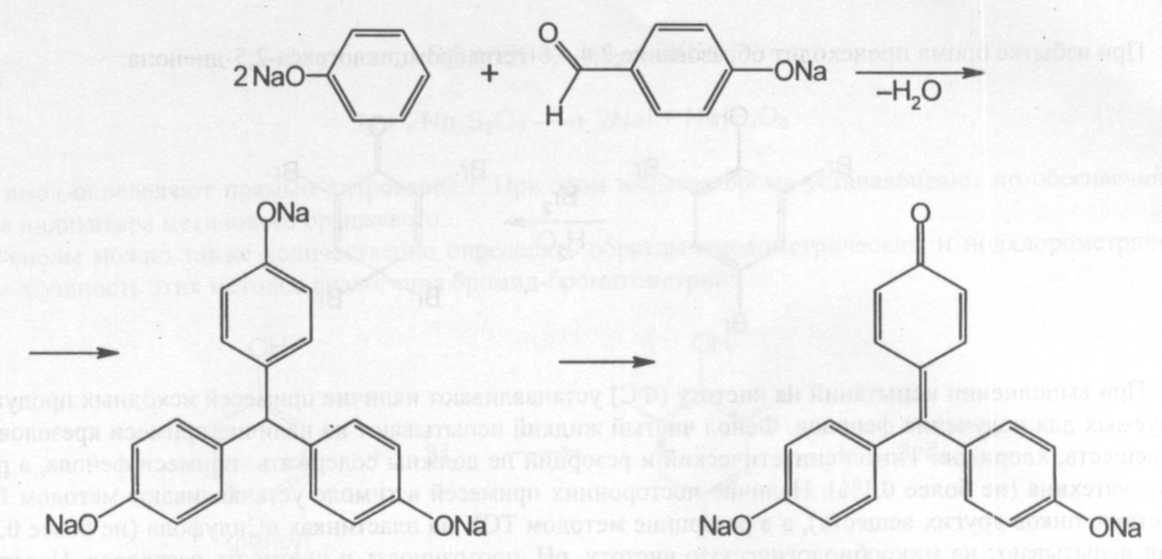
12. Дают синие или фиолетовое окрашивание при взаимодействии с раствором хлорида железа (III).
Чистота.
Определяют зольность, содержание воды, крезолов. Примесь воды и крезолов определяют по появлению мути в 5% водном растворе фенола.
Количественное определение.
Броматометрия.
Определение выполняют обратным титрованием 0,1 н раствором бромата калия в присутствии бромида калия. Z = 1/6
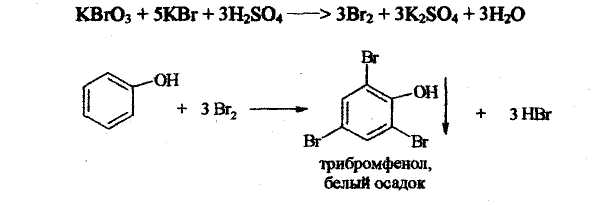
Избыток титрованного раствора приводит к образованию эквивалентного количества брома, который оттитровывают иодометрически:
Br2 + 2KI = 2 KBr + I2
Йодометрический метод.
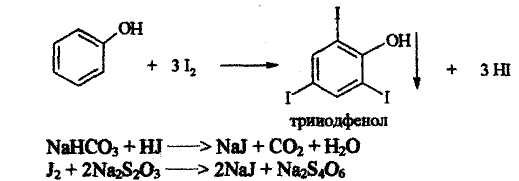
Йодхлорметрический метод.
Спектрофотометрия в видимой области спектра.
При этом используются цветные реакции окисления, сопровождающиеся образованием хиноидных структур и др.
Хранение.
В хорошо укупоренных склянках из темного стекла, залитых парафином, по списку Б.
Применение.
Антисептик. Действие их основано на способности свертывать белки. Также обладают бактерицидным свойством. Фенол (0,1-0,5%) используют в качестве консервантов некоторых лекарственных форм.
Форма выпуска.
3% и 5% растворы фенола в глицерине (ушные капли), 2% мазь.
Тимол.
Thymolum.
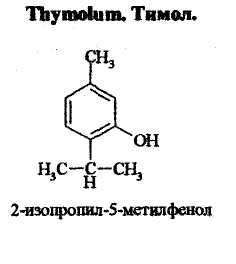
Описание.
Крупные бесцветные кристаллы или кристаллический порошок с характерным запахом и пряно-жгучим вкусом, летуч с водяным паром. Тпл. - 49-51°С.
Растворимость.
Очень мало растворим в воде, легко растворим в спирте, хлороформе, эфире, жирных маслах и ледяной уксусной кислоте, растворим в растворе гидроксида натрия.
Подлинность.
С раствором хлорида железа (III) дает комплекс красно-фиолетового цета.
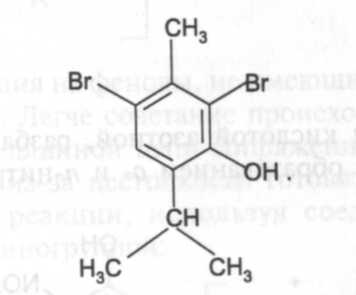
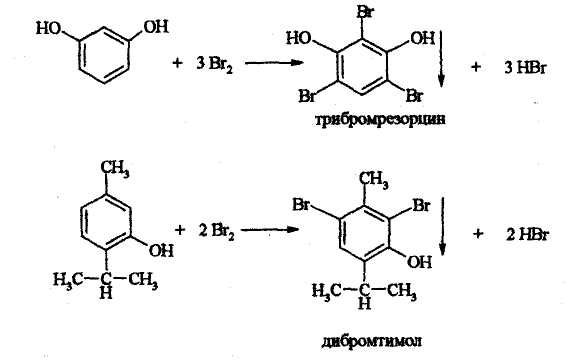
Галогенирование с образованием дибромпроизводного
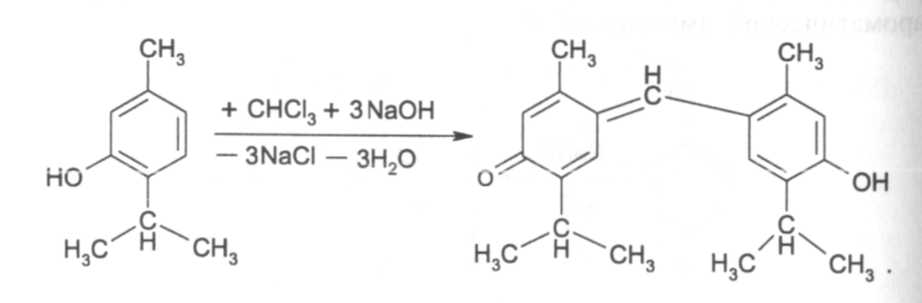
Для тимола предлагается реакция конденсации с хлороформом в щелочной среде. Продукт реакции окрашен в красно-фиолетовый цвет:
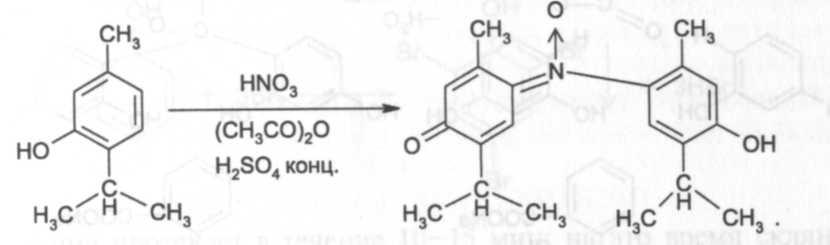
Нитрование тимола в среде уксусного ангидрида и концентрированной серной кислоты с образованием производного индофенола:
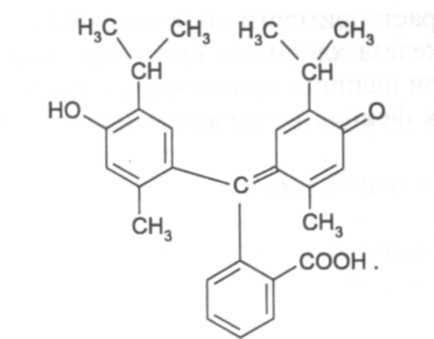
С тимолом образуется тимолфталеин — индикатор, окрашенный в щелочной среде в синий цвет:
Тимол образует ауриновый краситель желтого цвета, переходящего в фиолетовый.
Чистота.
Наличие примеси фенола по реакции с раствором хлорида окисного железа; не должно тотчас появляться фиолотовое окрашивание.
Кислотность или щелочность. Раствор тимола в 50% спирте должен иметь нейтральную реакцию.
Нелетучий остаток должен быть невесомым.
Количественное определение.
Броматометрия. Прямое титрование. При этом избыток брома устанавливают по обесцвечиванию раствора индикатора метилового оранжевого. Z = 1/4
Йдометрия.
Спектрофотометрия.
Хранение.
В хорошо укупоренных склянках из темного стекла, залитых парафином, по списку Б.
Применение.
Антисептик при поносах и метеоризме для уменьшения брожения в кишечнике и
Противоглистное средство.
Наружно употребляется для полосканий полости рта, зева, носоглотки в виде 0,05-0,1% растворов, а также как компонент в зубных порошках.
Консервант некоторых лекарственных форм.
Форма выпуска - порошок.
Resorcinum.
