
- •Тема лекции: «Механизмы защиты организма человека. Врожденный иммунитет»
- •I гр. Нормальные противоэритроцитарные антитела – изогемагглютинины α- и β.
- •II гр. Нормальные противомикробные, противовирусные, противогрибковые, противопротозойные антитела.
- •II стадия – адсорбция чужеродных клеток наповерхности фагоцита.
- •III стадия – поглощение чужеродных клеток фагоцитом и образование фаголизосом
- •1 Стадия – развитие в костном мозге
- •2 Стадия – циркуляция в крови
- •V ст. Формирование фагосомы
- •VI cт. Фаголизосома
- •VII стадия – киллинг или внутриклеточное разрушение чужеродных клеток
- •VIII ст. Заключительная – экзоцитоз продуктов деградации чужеродных клеток
Тема лекции: «Механизмы защиты организма человека. Врожденный иммунитет»
Иммунитет – это способность организма поддерживать постоянство своего макромолекулярного состава путем удаления чужеродных молекул, что обеспечивает устойчивость к инфекционным агентам и резистентность к опухолям (А.А. Ярилин. 2010).
Виды иммунитета:
1. Врожденный (видовой или конституциональный иммунитет) или неспецифический
2. Адаптивный (приспособительный) или специфический.
Врожденный или видовой (конституциональный) иммунитет – это состояние устойчивости к патогенному действию микроорганизмов, обуслов-ленное молекулярными особенно-стями строения организма.
Характеризуется следующими признаками:
Видовой иммунитет генетически детерминирован и передается по наследству.
Обладает специфичностью (устойчивость к одним инфекциям и чувствительность – к другим).
Обладает способностью распознавать группы чужеродных молекул.
В основе защиты может лежать принцип молекулярной комплементарности.
При этом устойчивость к инфекции определяется:
отсутствием рецепторов на поверхности клеток организма человека для адгезии и колонизации
отсутствием структур-мишеней, на которые действуют микробы и их токсины
наличием специальных ферментов, разрушающих микроорганизмы (протеазы, ДНК-азы, РНК-азы и др.)
наличием специальных рецепторов для взаимодействия с патогенами
Система врожденного иммунитета сформировалась у многоклеточных животных и человека более 1,5 млрд. лет назад.
Главные составные врожденного иммунитета:
1 – распознавание чужеродных агентов во внутренней среде организма с помощью рецепторов, специализированных на узнавании «образов» (паттернов) патогенности;
2 – элиминация опознанных чужеродных агентов из организма путем фагоцитоза и расщепления.
В процессе эволюции в организме закреплялись гены, кодирующие молекулы-рецепторы, предназначенные для распознавания не просто «чужого», но заведомо опасного для данного организма.
Эти рецепторы (мембранные или растворимые молекулы) обладают простран-ственным сродством к наиболее общим и связанным с патогенностью молекулярным маркерам чужеродных агентов: компонентам клеточной стенки бактерий, эндотоксинам, нуклеиновым кислотам и т.д.
Каждый рецептор распознает не молекулу, а целую группу чужеродных похожих молекул, служащих «образами» (паттернами) патогенности.
Патоген(паттерн)распознающие рецепторы (ПРР = PRR) представлены:
1 – на поверхности клеток-эффекторов,
2 – в гранулах фагоцитов,
3 – в жидких средах организма.
В организме имеется относительно небольшое количество генов, кодирующие распознавание практически всех патогенов.
В результате распознавания образов патогенности происходит:
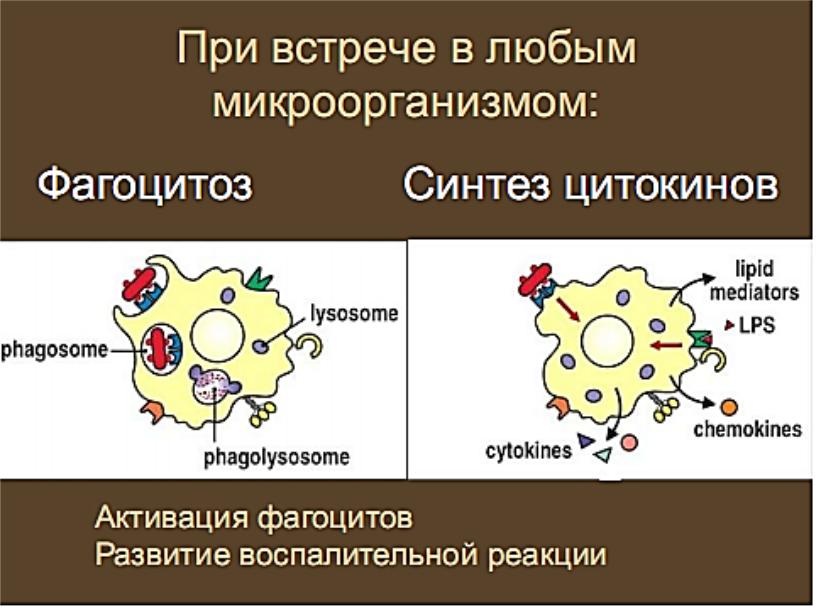
1 – активация клеток-фагоцитов: они убивают и затем элиминируют патогены → внутриклеточный цитолиз;
2 – активация внеклеточных факторов – внеклеточный цитолиз (гуморальные факторы);
3 – активация контактных механизмов – контактный цитолиз.
Во всех случаях окончательное расще-пление убитых патогенов происходит в процессе фагоцитоза !
Более 500 млн. назад у животных, а затем у человека в процессе эволюции сформировался адаптивный (приспособительный) или приобретенный (специфический) иммунитет.
Главные составляющие адаптивного иммунитета:
1 – распознавание антигенов (чужеродных для организма веществ и структур), независимо от их связи с патогенностью, с помощью специальных клонально распределенных на клетках рецепторов;
2 – элиминация распознанных чужеродных агентов;
3 – формирование иммунологической памяти о контакте с антигеном, позволяющей быстрее и эффективнее удалять чужеродные агенты.
Особенности адаптивного иммунитета:
1- специфичность антигенраспознающих рецепторов формируется в процессе дифференцировки клеток;
2 – селекция лимфоцитов для устранения «опасных» для организма клонов клеток (однако риск развития аутоиммунного процессов сохраняется);
3 - наличие феномена иммунологической памяти;
4 – распознавание индивидуальных чужеродных молекул или похожих групп молекул – антигенов (существует около 106 различных антигенов);
5 - при развитии иммунного ответа в специализированных клонах лимфоцитов происходит перестройка их генов, кодирующих антигенраспознающие рецепторы, что приводит к образованию в каждой клетке рецепторов с уникальной специфичностью.
При активации каждая клетка может дать начало клону, все клетки которого будут иметь рецепторы той же специфичности.
6 - каждый антиген распознают не все лимфоциты, а только соответствующие их клоны, имеющие специфические антигенраспознающие рецепторы.
7 – способен защищать организм от агрессии изнутри – от злокачественных новообразований.
Основные свойства врожденного и адаптивного иммунитета
Характеристика |
Врожденный |
Адаптивный |
Условия формирования |
Формируется в онтогенезе вне зависимости от «запроса» - наличия чужеродного агента |
Формируется в ответ на «запрос» - поступление чужеродного агента |
Объект распознавания |
Группы чужеродных молекул, связанных с патогенностью микроорганизмов |
Индивидуальные молекулы (антигены) |
Эффекторные клетки |
Миелоидные (моноциты, макрофаги, гранулоциты, нейтрофилы) NK-клетки |
Лимфоидные (В- и Т-лимфоциты) |
Тип реагирования популяции клеток |
Общий или групповой, заложенный генетически в организме вне зависимости от наличия патогена |
Реакция на антиген в виде выработки клонов, реагирующих с этим антигеном |
Время реализации эффекта |
Немедленно |
Требует времени (адаптивный иммунный ответ) |
Распознаваемые молекулы |
Образы патогенности (паттерны), стресс-молекулы |
Конкретный антиген |
Чем распознает (распознающие рецепторы) |
Патогенраспознающие рецепторы (ПРР=PRR) |
Антигенраспознающие рецепторы (В-клеточные=BCR и Т-клеточные=TCR) |
Распознающие рецепторы |
TLR, NLR, CLR, RIG, DAO, Scavenger-рецепторы, растворимые рецепторы |
BCR (на В-клетках), TCR-γδ (на γδТ-клетках), TCR-αβ (на αβТ-клетках) |
Распределение на клетках |
Все клетки в популяции экспрессируют одинаковые рецепторы |
Клональное – по отдельным клонам клеток |
Угроза аутоагрессии (способность разрушать собственные клетки в организме) |
Минимальная (не способны распознавать собственные молекулы организма) |
Реальная (способны реагировать на собственные молекулы и вызывать повреждение организма человека) |
Наличие иммунологической памяти |
Отсутствует (каждый раз реакции на внедрение чужеродных молекул развиваются как впервые) |
Формируются клоны клеток, сохраняющие память о предыдущей встрече с антигеном, что позволяет им реагировать на повторную встречу значительно быстрее |
Молекулы-мишени иммунитета:
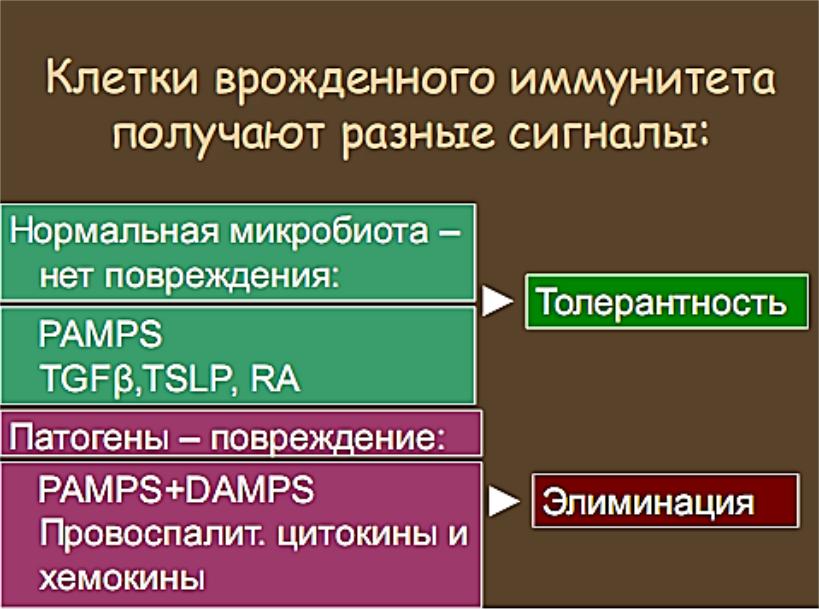
Образы патогенности или патогенассоциированные молекулярные паттерны (РAMP – Pathogen-associated molecular patterns) – группы молекул, отсутствующие в организме-хозяине, но характерные для патогенов (вирусов, бактерий, грибов, простейших, паразитов). РАМР являются знаками опасности, универсальным сигналом о проникновении в организм не просто чужеродного, но биологически агрессивного агента. Рецепторы для РАМР – паттерн(патоген)распознающие рецепторы позволяют распознавать все возможные типы патогенов.
Антигены – высокомолекулярные соединения, способные специфически стимулировать иммунокомпетентные лимфоциты. Распознаются антигенспецифическими рецептора-ми, представленными на лимфоцитах.
Стрессорные молекулы – собственные молекулы организма, экспрессируемые на мембране клеток человека при клеточном стрессе и сигнализирующие об опасности эндогенного происхождения (любое повреждение). Они распознаются рецепторами некоторых разновидностей лимфоцитов (естественные киллеры - NK-клетки, γδТ-лимфоциты). Они занимают промежуточное положение между врожденным и адаптивным иммунитетом.
Родственную группу молекул образуют образы опасности (DАМР-danger-associated molecular paterns) – эндогенные молекулы, сигнализирующие о любом повреждающем воздействии (температурном, лучевом, инфекционном и др.). Некоторые образы опасности (белки теплового шока) распознаются ПРР.
DАМР – это эндогенные эквиваленты РАМР.
Механизмы врожденного иммунитета:
1. Анатомо-физиологические механизмы (барьерная и выделительная функции, воспаление и т. д.)
2. Нормальная микрофлора
3. Гуморальные факторы (лизоцим, бета-лизины, комплемент, интерфероны, фибронектин, белки острой фазы, естественные или нормальныые антитела)
4. Клеточные факторы (фагоцитоз и естественная клеточная цитотоксичность)
Анатомо-физиологические механизмы:
1.Защитная функция кожи.
2.Защитная функция слизистых оболочек.
3. Барьерная функция органов и тканей.
4. Выделительная функция.
5. Температурная реакция.
Нормальная микробиота и иммунная система.
У человека 1013 своих клеток и 1014 клеток различных микроорганизмов = 100 триллионов (на 1 клетку приходится 10 микробов) более 1000 видов
Суммарный геном нормальной микробиоты содержит в 100 раз больше генов, чем геном человека
Масса нормальной микробиоты составляет от 2 до 8 кг
99,9% составляет микробиота толстого кишечника


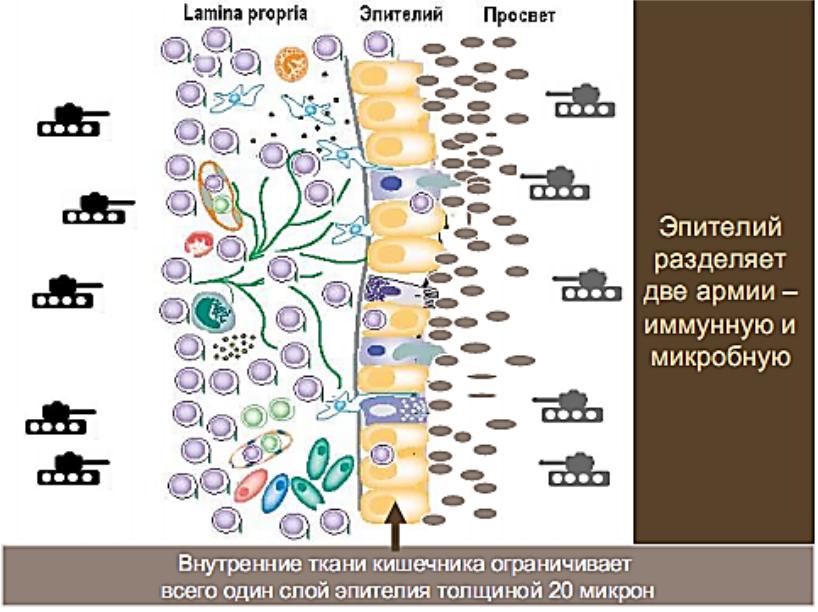


Функции эпителия
Разделительная (предотвращает контакт фагоцитов и НМ)
Иммунорегуляторная: -Участие в создании микроокружения богатого TGF-β, RA и TSLP – индукция Th2 Tregs
Сигнальная -оповещает -привлекает (хемокины)
-активирует (провоспалительные цитокины) клетки врожденного иммунитета о появлении патогенов
Эпителий является не только барьером, но и активным участником врожденного иммунитета.
Нормальная микрофлора
Функции нормальной микрофлоры кишечника:
Колонизационная резистентность,
Иммуномодулирующая функция,
Детоксикационная деятельность,
Витаминообразующая функция,
Переваривание и всасывание пищи,
Регуляция моторной деятельности кишечника.
Гуморальные механизмы
Лизоцим
Бета-лизин
Нормальные антитела
Система интерферонов
Система комплемента
Нормальные антитела или конститутивные иммуноглобулины
существуют в крови и других жидкостях до встречи с антигеном,
относятся к IgG, реже к IgА и IgМ,
способны связывать множество патогенов (экзогенных и ауто АГ)
мишенями для нормальных Ig могут быть другие молекулы:
- другие Ig,
- ТСR,
- молекулы CD4, CD5, HLA-I,
- рецепторы к Fc-фрагментам IgG и др.
Функции нормальных антител:
«первая линия обороны» против инфекций;
удаление из организма отживших клеток и продуктов катаболизма;
представление АГ для Т-лимфоцитов;
поддержание гомеостаза аутоиммунной реактивности;
противовоспалительное действие (нейтрализация суперантигенов, индукция синтеза противо-воспалительных цитокинов, снижение комплементзависимого повреждения тканей и др.).
Выделяют 2 разновидности нормальных антител:
